Lithiumoxid
| Lithiumoxid | |
| |
| Identifikation | |
|---|---|
| Synonymer |
lithin, lithinoxid |
| N o CAS | |
| N o ECHA | 100.031.823 |
| N o EF | 235-019-5 |
| Udseende | pulver |
| Kemiske egenskaber | |
| Brute formel |
Li 2 O [isomerer] |
| Molar masse | 29,881 ± 0,004 g / mol Li 46,46%, O 53,54%, |
| Fysiske egenskaber | |
| T ° fusion | 1.570 ° C |
| Opløselighed | Voldelig hydrolyse til LiOH |
| Volumenmasse | 2013 kg · m -3 |
| Krystallografi | |
| Pearson symbol | |
| Krystalklasse eller rumgruppe | Fm 3 m (n ° 225) |
| Strukturbericht | C1 |
| Typisk struktur | CaF 2 |
| Forholdsregler | |
| WHMIS | |
 E, E : Ætsende materiale ved kontakt med vand danner et ætsende stof: lithiumhydroxid Oplysning ved 1,0% ifølge klassificeringskriterier |
|
| Direktiv 67/548 / EØF | |
 VS Symboler : C : Ætsende R-sætninger : R34 : Forårsager forbrændinger. S-sætninger : S26 : I tilfælde af kontakt med øjnene, skylles straks med rigeligt vand og læge kontaktes. S45 : I tilfælde af et uheld eller hvis du føler dig utilpas, søg straks lægehjælp (vis etiketten, hvor det er muligt). S36 / 37/39 : Bær passende beskyttelsesdragt, handsker og øjen- / ansigtsbeskyttelse. R-sætninger : 34, S-sætninger : 26, 36/37/39, 45, |
|
| Enheder af SI og STP, medmindre andet er angivet. | |
Den oxid af lithium er en kemisk forbindelse med formlen Li 2 O. Det er dannet med små mængder af lithiumhydroxid LiOH når lithium metal brænder i luft og er kombineret med ilt og vand luft:
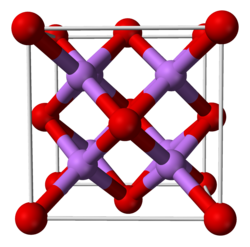
4 Li + O 2→ 2 Li 2 O 4 Li + 2H 2 O + O 2 → 4 LiOHLithiumoxid har i fast tilstand en krystallinsk struktur af antifluorin typen, dvs. en struktur modelleret efter af calciumfluorid CaF 2 men hvor kationer og anioner spille den modsatte rolle. I jorden gas tilstand, Li 2 O molekyle er lineært, i modsætning til de resultater, forudsagt af VSEPR teori (hvorefter Li 2 O molekyle bør have samme form som H 2 O molekyle ), hvilket er i overensstemmelse med en geometri styret af ioniske bindinger.
Li 2 O skyldes den termiske nedbrydning af lithium peroxid Li 2 O 2og angriber silica ved forhøjet temperatur.
Referencer
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- " The Fluorite (C1) Structure " , på http://cst-www.nrl.navy.mil/ (adgang 17. december 2009 )
- " Lithium oxide " i databasen af kemiske produkter Reptox af CSST (Quebec organisation med ansvar for sikkerhed og sundhed), adgang April 25, 2009
