Elimineringsreaktion
I organisk kemi er eliminering (eller β-eliminering ) en organisk reaktion, der transformerer en substitueret alkan ( halogenalkaner , alkoholer osv.) Til et ethylenderivat eller endda til en alken , hvis udgangsmolekylet, ud over den fraspaltelige gruppe , n 'er kun en alkan-type carbonkæde.
Betingelserne er ud over barske betingelser for en nukleofil substitution , en reaktion, der ligner i mange henseender og samtidig: eliminering sker i nærværelse af en stærk base og ved opvarmning af reaktionsblandingen.
Generel ligning
Et af de vigtigste eksempler på eliminering er omdannelsen af en halogenalkan til en alken ; vi taler derefter om dehydrohalogenering :
De mest almindeligt anvendte baser er soda (Na + , HO - ), kaliumchlorid (K + , HO - ), eller endog alkoholat ioner (RO - ) (fremstillet ved omsætning af natrium i en alkohol ROH, vandfri ).
Ligesom for nukleofil substitution er der en monomolekylær eliminering og en bimolekylær eliminering, der almindeligvis er angivet som henholdsvis El og E2.
I den resterende del af denne artikel gives eksemplerne med et halogeneret derivat som reagens.
Monomolekylær eliminering
E1 kinetik
Den monomolekylære eliminationsreaktion udføres i to trin: et monomolekylært trin, der kun involverer molekylet af det halogenerede derivat på reaktantsiden, hvilket er det kinetisk begrænsende trin efterfulgt af et bimolekylært trin. Følgelig afhænger reaktionens kinetik i tilnærmelsen af det kinetisk bestemmende (eller begrænsende ) trin kun af koncentrationen af arten RX.
Reaktionen er derfor kendetegnet ved en kinetik af samlet rækkefølge 1, af delordninger 1 med hensyn til det halogenerede derivat og 0 med hensyn til basen B | : v = k. [RX] , hvor:
- [RX] repræsenterer koncentrationen af halogeneret derivat i mol.L -1
- v repræsenterer hastigheden af eliminationsreaktionen. Det udtrykkes i mol.s -1 .
- k er hastighedskonstanten: det er i virkeligheden, at den kinetisk begrænsende trin (k 1 ). Dens enhed, Ls -1 , er udledt af de to andre termer.
Mekanisme for E1
Reaktionen finder sted i to faser.
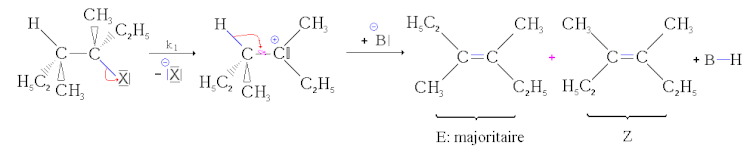
- Første trin: afgang af nucleofuge, dannelse af en carbocation. dette carbocation dannelsestrin er et langsomt, reversibelt trin og pålægger sin hastighed på hele reaktionen.
- Andet trin: syre-base reaktion. Basen river protonen af. Dubletten "foldes" derefter over kulstof-kulstofbinding for at danne en dobbeltbinding . Da kulstof-kulstof enkeltbinding kan rotere, kan der dannes to stereoisomerer. Da denne reaktion er meget hurtigere end den forrige, påvirker dens hastighed ikke den samlede hastighed.

Stereoselektivitet og regioselektivitet
StereokemiSom vist ved mekanismen, fjerner passagen gennem en carbocation, som er en plan struktur, ethvert element af stereospecificitet i modsætning til (se følgende) mekanismen for bimolekylær eliminering.
Men hvis der kan dannes to geometriske stereoomerer, dannes de ikke i samme proportioner. Den mest stabile isomer, det vil sige den med den laveste energi, dannes overvejende (dette er Zaitsevs regel). Det er derfor E-isomeren, der hovedsagelig dannes i fravær af mesomery. På den anden side, hvis dobbeltbindingen af kun et af de to produkter kan delokaliseres af mesomery, er det denne, der hovedsagelig vil blive dannet. Dette kaldes delvis stereoselektivitet.
 Regiokemi
Regiokemi
Når der kan dannes flere konstitutionelle isomerer, dannes den termodynamisk mest stabile alken fortrinsvis. Hvis der kun er alkylgrupper, er dette den mest substituerede alken. Hvis mesomeria kan gribe ind, er det den mest konjugerede alken, der er i flertallet. Dette kaldes regioselektivitet eller Zaïtsevs regel .
Imidlertid dannes den termodynamisk mindre stabile alken undertiden fortrinsvis, dette kaldes Hofmann-eliminering . Dette er især tilfældet, når den anvendte base er overbelastet (f.eks. KtBuO), eller når der f.eks. Er en ammoniumion, der elimineres. (Molekyle, der bærer en amin i nærværelse af MeI i et antal ækvivalenter, der er tilstrækkelige til at danne ammoniumsaltet, derefter anbragt i nærværelse af vådt og opvarmet sølvoxid . Dannelse af alkenet ved eliminering af Hofmann og derfor afgang fra N (Me 3.)
Faktorer, der påvirker reaktionen
Parametrene, der påvirker eliminering af E1, er:
- virkningen af R-: det kinetisk bestemmende trin er dannelsen af carbocation (og ikke dets reaktivitet), og jo mere stabil den er, desto mere foretrækkes reaktionen.
- nukleofuge: spaltningen af den C-forladende gruppebinding er nøgletrinet i mekanismen, afhænger reaktionen stærkt af arten af denne nukleofuge. Jo bedre startgruppen er, jo hurtigere bliver reaktionen. For eksempel til dehydratisering af alkoholer, hvis første trin er protonering af alkoholen til dannelse af en oxonium, og derfor en bedre fraspaltelig gruppe (H 2 O⇒HO - ). En hurtig rangordning af startgrupperne ville være:
(tegnet ">" betyder: "bedste startgruppe end")
Bemærk, at basen ikke påvirker denne type reaktion af rækkefølge 1 og dette, for så vidt den ikke griber ind under det første trin, der bestemmer reaktionens samlede hastighed.
Alkylgruppe af det halogenerede derivatMekanismen passerer gennem et reaktionsmellemprodukt af carbocation-typen. Sidstnævnte er desto mere stabil, jo mere erstattes den. Således skrider reaktionshastigheden (derfor til dannelse af carbocation) fra de primære derivater til de sekundære og derefter til de tertiære. I praksis reagerer kun sidstnævnte og et par sekundære derivater ved denne mekanisme.
NukleofugeJo mere polariserbart RX-linket er, jo lettere er det at bryde. Denne binding har derfor en faldende labilitet ("sprødhed") fra fluor til jod: F> Cl> Br> I.
(symbolet ">" betyder: "hurtigere end")
Opløsningsmiddel- Polaritet: et polært opløsningsmiddel stabiliserer carbocation; det letter således den første reaktion. Hastigheden stiger derfor med opløsningsmidlets polaritet.
- Proticitet: et protisk opløsningsmiddel er mere et handicap: det risikerer faktisk at konkurrere med carbocation under den (stærke) syre-base-reaktion.
Konkurrence
Denne reaktion ikke kun konkurrerer med andre elimination, men også med reaktionerne på nukleofile substitutioner, navnlig med S N 1 . Sidstnævnte forekommer faktisk under lignende forhold (bortset fra opvarmning).
Bimolekylær eliminering
Kinetisk
Den bimolekylære eliminationsreaktion har en kinetik af global orden 2 og delvis orden 1 med hensyn til det halogenerede derivat RX og til basen B: - . Reaktionen finder sted i et enkelt trin, der er bimolekylært, og reaktionens hastighed følger derfor en typelov: v = k. [RX]. [B: - ] .
eller:
- [RX] repræsenterer koncentrationen af halogeneret derivat (udtrykt i mol.L- 1)
- [B: - ] repræsenterer basiskoncentrationen (udtrykt i mol.L -1 )
- v repræsenterer hastigheden af eliminationsreaktionen. Det udtrykkes i mol.s -1 .
- k er hastighedskonstanten. Dens enhed, Ls -1 .mol -1 , er udledt af dem fra de to andre termer.
Mekanisme for E2
Bimolekylær eliminering er en et-trins, bimolekylær reaktion.
Under det samme elementære trin opstår protonens rivning ved basen, dannelsen af dobbeltbindingen og afgang af halogenatomet (nucleofuge) i form af en halogenid. Vi taler om en synkron eller samordnet mekanisme.
Stereokemi
E2 er en stereospecifik reaktion .
Reaktionen finder kun sted, når brint og den fraspaltelige gruppe er i den anti-pleurplanariske position .
Faktorer, der påvirker reaktionen
- Reaktionshastigheden for en E2 varierer kun lidt afhængigt af klassen (primær: I, sekundær: II, tertiær: III) af det betragtede halogenid. Jo højere klassen er, jo hurtigere er reaktionen (III> II> I) af steriske årsager (eliminering gør det muligt at fjerne voluminøse og derfor "voluminøse" substituenter i slutproduktet, der er til stede i det oprindelige produkt, reagenset , da man passerer fra en valensvinkel på 109 ° 28 'i denne, på niveauet med "sp 3 " carbon , der bærer protonen H, i en valensvinkel på 120 °, i slutproduktet, hvor det samme carbon er nu "hybridiseret sp 2 "). En primær halogenalkan foretrækkes generelt i dette tilfælde, men når man er i nærværelse af en sekundær halogenalkan, skelnes reaktionerne af El- og E2-typen ved de potentielle mesomere effekter ("mesomer" -effekt: generelt udtryk, der definerer en elektronisk effekt svarende til til en delokalisering af ladningen, her positiv, på en Aryl-gruppe, for eksempel en umiddelbar nabo, derfor "i α", af den brudte CH-binding, taler man om "deprotonering", af den stærke base). Enhver substituent i carbonkæden, der er i stand til at stabilisere carbeniumionen (C + carbocation ) gennem denne type elektronisk effekt, vil fremme E1-mekanismen.
- Reaktionshastigheden øges med basens styrke, så der kræves en stærk base.
- Nukleofuge-karakteren af den forladende gruppe har også indflydelse på reaktionen, men denne indflydelse er ikke den primære parameter i modsætning til den unimolekylære eliminationsmekanisme (E1).
- For at fremme en reaktionsmekanisme med bimolekylær E2-eliminering er det hensigtsmæssigt at bruge et aprot opløsningsmiddel (DMSO, THF, toluen, n-hexan osv.)
Konkurrence
Denne reaktion konkurrerer ikke kun med E1, men også med nukleofile substitutionsreaktioner, især med S N 2 , hvilket sker under lignende betingelser. Bemærk, at en eliminationsreaktion vil kræve mere energi end en tilsvarende substitutionsreaktion, normalt gennem opvarmning.
Bemærkninger
Den anvendte base er også en nukleofil . Dette forklarer konkurrencen med reaktionerne fra udskiftninger. I slutningen af reaktionen kan man finde, blandede, eliminationsprodukter og erstatningsprodukter.