Svovlmonoxid
| Svovlmonoxid | |
   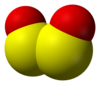 Struktur af svovlmonoxid. (bund: "dimer" peroxid S 2 O 2) |
|
| Identifikation | |
|---|---|
| N o CAS | |
| PubChem | 114845 |
| ChEBI | 45822 |
| SMILE |
O = S , |
| InChI |
InChI: InChI = 1S / OS / c1-2 InChIKey: XTQHKBHJIVJGKJ-UHFFFAOYSA-N |
| Kemiske egenskaber | |
| Brute formel | S O |
| Molar masse | 48,064 ± 0,005 g / mol O 33,29%, S 66,72%, |
| Enheder af SI og STP, medmindre andet er angivet. | |
Den svovlmonoxid er en kemisk forbindelse med formlen SO. Dette molekyle er termodynamisk ustabilt og eksisterer kun som sådan i fortyndet gasform ; den dimeriseres i S 2 O 2i kondenseret tilstand, undertiden kaldet svovlperoxid . Dette er grunden til, at svovlmonoxid er blevet opdaget i rummet, men ikke findes naturligt på jorden .
Den SO molekyle er karakteriseret ved en triplet grundtilstand , ligesom O 2 molekyle, det vil sige, at hvert molekyle har to ikke- parrede elektroner med parallel spin , hver på sin egen atombane . SO binding er 148,1 um i længde , længere end af S 2 O molekyler ( Kl. 146 ) , SO 2 ( 143.1 pm ) og SO 3 ( 142 pm ) .
Molekylet kan exciteres i en singletilstand ved absorption af en infrarød foton . Denne singlet tilstand antages at være mere reaktive end triplettilstanden, som iagttaget for O 2 molekyle..
Svovlmonoxid kan produceres i laboratoriet ved glødeafledning gennem svovldampe blandet med svovldioxid SO 2og kunne påvises ved sonoluminescens i en opløsning af koncentreret svovlsyre indeholdende ædle gasser . En kemiluminescerende svovlmonoxiddetektor er også blevet offentliggjort baseret på reaktionerne:
SO + O 3→ SO 2 *+ O 2, SO 2 *→ SO 2+ h ν .Svovlmonoxid forekommer naturligt i miljøet på Io- satellitten på planeten Jupiter , både i sin atmosfære og i sin eksosfære , og er blevet påvist i atmosfæren i Venus , Comet Hale-Bopp og det interstellære medium .
Noter og referencer
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- (in) Norman N. Greenwood, A. Earnshaw, " Chemistry of the Elements ", Butterworth-Heinemann, 2 e udgave, Oxford, 1997 ( ISBN 0080379419 ) .
- (in) " The temperature of single-bubble sonoluminescence " KS Suslick and Flannigan DJ in The Journal of the Acoustical Society of America , (2004) 116 , 4, 2540.
-
(i) Richard L. Benner, Donald H. Stedman , " Chemical Mechanism og effektivitet af Sulphur Chemiluminescence Detector " , Applied Spectroscopy , Vol. 48, nr . 7,
Juli 1994, s. 14A-21A og 775-903 ( læs online )
DOI : 10.1366 / 0003702944029901 -
(i) Lellouch , " Urey prisen Reading. Ios atmosfære: endnu ikke forstået ” , Icarus , bind. 124, nr . 1,
November 1996, s. 1-21 ( læs online )
DOI : 10.1006 / icar.1996.0186 -
(in) CT Russell og MG Kivelson , " Detection of SO in Io's Exosphere " , Science , bind. 287, nr . 5460,
17. marts 2000, s. 1998-1999 ( ISSN 0036-8075 , læs online )
DOI : 10.1126 / science.287.5460.1998 -
(i) Chan Y. Na, Larry W. Esposito , Thomas E. Skinner , " International Ultraviolet Explorer Observation af Venus SO 2
og SO ” , Journal of Geophysical Research - Atmospheres , bind. 95, n o D61990, s. 7485-7491 ( læs online )
DOI : 10.1029 / JD095iD06p07485 -
(in) DC Lily, DM Mehringer, D. Benford, Gardner, TG Phillips, D. Bockelée-Morvan, N. Biver, P. Colom, J. og D. Crovisier Despois, et al . , “ Nye molekylære arter i komet C / 1995 O1 (Hale-Bopp) observeret med Caltech Ssubmillimeter-observatoriet ” , Jord, måne og planeter , bind. 78, n knogle 1-3,
1998, s. 13-20 ( læs online )
DOI : 10.1023 / A: 1006281802554 -
(i) AC Gottlieb, Gottlieb EW, Mr. Litvak, JA Ball og H. Penfield , " Observationer af interstellare svovlmonoxid " , Astrophysical Journal, del 1 , Vol. 219,
1 st januar 1978, s. 77-94
DOI : 10.1086 / 155757