Palladium (II) acetat
| Palladium (II) acetat | ||
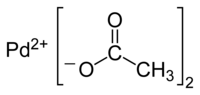
| ||
 | ||
| palladium (II) acetatpulver i trimer form | ||
| Identifikation | ||
|---|---|---|
| Systematisk navn | palladium diethanoat | |
| Synonymer |
palladium diacetat, diacetatopalladium |
|
| N o CAS | ||
| N o ECHA | 100.020.151 | |
| N o RTECS | AJ1900000 | |
| PubChem | 167845 | |
| SMILE |
[Pd + 2]. [O-] C (= O) C. [O-] C (= O) C , |
|
| InChI |
InChI: InChI = 1S / 2C2H4O2.Pd / c2 * 1-2 (3) 4; / h2 * 1H3, (H, 3,4); / q ;; + 2 / p-2 InChIKey: YJVFFLUZDVXJQI-UHFFFAOYSA |
|
| Udseende | rødbrunt (trimer form) eller lyserødt (polymert form) pulver | |
| Kemiske egenskaber | ||
| Brute formel | Pd (CH 3 COO) 2 | |
| Molar masse | 224,51 ± 0,01 g / mol C 21,4%, H 2,69%, O 28,51%, Pd 47,4%, |
|
| Fysiske egenskaber | ||
| T ° fusion | 216,3 til 223,7 ° C | |
| T ° kogning | 204 ° C (nedbrydning) | |
| Opløselighed | 0,92 g · L -1 (vand, 20 ° C ) | |
| Forholdsregler | ||
| SGH | ||
 H318, P280, P305 + P351 + P338 + P310,
H318 : Forårsager alvorlig øjenskade
H318, P280, P305 + P351 + P338 + P310,
H318 : Forårsager alvorlig øjenskade P280 : Bær beskyttelseshandsker / beskyttelsestøj / øjenbeskyttelse / ansigtsbeskyttelse. P305 + P351 + P338 + 310 : Ved øjnene: Skyl forsigtigt med vand i flere minutter. Fjern kontaktlinser, hvis offeret har dem på, og de let kan fjernes. Fortsæt med at skylle. Kontakt straks et GIFTINFORMATION eller en læge. |
||
| Økotoksikologi | ||
| DL 50 |
2100 mg · kg -1 (mus, oral ) 5110 mg · kg -1 (rotte, oral ) |
|
| Enheder af SI og STP, medmindre andet er angivet. | ||
Den palladiumacetat (II) er en organisk forbindelse af palladium med formlen [Pd (CH 3 COO) 2 ] n, forkortet [Pd (OAc) 2 ] n . Det er mere reaktivt end dets platinanalog . Afhængigt af dens støkiometri findes den i to forskellige former med væsentligt forskellige egenskaber.
Struktur
Med et forhold mellem et atom af palladium og to acetatligander eksisterer forbindelsen i molekylær og polymert form. Palladium får i begge tilfælde en kvadratisk plan molekylær geometri .
I sin form udarbejdet af Wilkinson og hans team i 1965 og karakteriseret ved Skapski og Smart i 1970 ved røntgenkrystallografi , er palladium (II) acetat et rødbrunt fast stof, der krystalliserer i form af monokliniske plaques. Den har en trimer struktur, hvor de tre palladiumatomer danner en ligesidet trekant, der hver er bundet til to par acetatligander, der broder atomerne i palladium, i en sommerfuglkonformation.
Palladium (II) acetat kan også fremstilles som et lyserødt pulver. Det pulver diffraktion røntgen lad os sige, at denne form er polymere.
-
Timerisk form
-
Polymer form
Syntese
Palladium (II) acetat kan fremstilles i sin trimere form ved behandling af et skum af palladium med en blanding af salpetersyre varm og eddikesyre . Palladium skal være i overskud, eller en strøm af nitrogen skal være til stede for at forhindre forurening med nitritoacetatblandingen (Pd 3 (OAc) 5 NO 2 ):
palladium +4 HNO 3 → Pd (NO 3 ) 2 + 2 NO 2 + 2 H 2 O Pd (NO 3 ) 2 + 2 CH 3 COOH → Pd (O 2 CCH 3 ) 2 + 2 HNO 3Trimeicacetat har en anden opløselighed og katalytisk aktivitet sammenlignet med dens variant indeholdende nitrat-acetatblanding. Forebyggelse af dets dannelse eller kontrol af mængden er et vigtigt aspekt i pålidelig anvendelse af palladium (II) acetat.
Den palladium propanoat (II) fremstilles analogt; andre carboxylater fremstilles ved behandling af palladium (II) acetat med den passende carboxylsyre . Omvendt kan acetatet fremstilles ved behandling af de andre palladium (II) carboxylater med eddikesyre. Denne metode til ligandudveksling med andre oprensede carboxylater er et levedygtigt alternativ til syntese af palladium (II) acetat uden nitroforurening.
Opvarmet i nærværelse af alkoholer eller kogt i lang tid i andre opløsningsmidler nedbrydes palladium (II) acetat til palladium.
Anvendelser
Katalyse
Palladiumacetat anvendes som en katalysator i mange organiske reaktioner , især dem med alkener , diener , alkyl- , aryl- og vinyl halogenider til dannelse reaktive addukter .
Der kan nævnes blandt reaktionerne katalyseret af palladium (II) acetat:
- vinylering, for eksempel Heck-reaktionen og relaterede processer;
- omlejring af acykliske diener, for eksempel Cope-omlejring ;
- carbonyleringsreaktioner reaktioner , for eksempel dannelsen af estere fra aryliodider, carbonmonoxid , en alkohol eller phenol (molekyle) ;
- den reduktive aminering af aldehyder eller ketoner med kaliumformiat ;
- den Wacker processen , dvs. oxidationen af ethylen ved vand til acetaldehyd , en precursor for poly (vinylacetat) .
- den Buchwald-Hartwig-reaktion mellem en aryl hlogenide eller pseudohalogenid med en amin ;
- omdannelse af arylbromider til trimethylsilaner, en funktionel gruppe, der findes i mange organiske forbindelser inklusive "Latitude" fungicid.
Pd (O 2 CCH 3 ) 2 er forenelig med de elektroniske egenskaber af arylbromider, og i modsætning til andre syntesemetoder, denne fremgangsmåde ikke kræver højtryksudstyr.
Forløber for andre palladiumforbindelser
Palladiumacetat anvendes til at fremstille andre palladium (II) forbindelser, for eksempel phenylpalladiumacetat, der anvendes til at isomerisere allylalkoholer til aldehyder. Den fremstilles som følger:
Hg (C 6 H 5 ) (OAc) + Pd (OAc) 2 → Pd (C 6 H 5 ) (OAc) + Hg (OAc) 2Palladium (II) acetat reagerer med acetylacetone ("acac" liganden) til dannelse af Pd (acac) 2 .
Det kan bruges til at fremstille éalement Hermann-katalysator (en) bruges især i Heck-reaktionen . For at gøre dette reagerer vi acetatet med tris (o-tolyl) phosphin (en) :
2 Pd (OAc) 2 + 2P (C 6 H 4 -2-CH 3 ) 3 → 2 HOAc + Pd 2 (OAc) 2 [P (C 6 H 4 -2-CH 2 ) (C 6 H 4 - 2-CH 3 ) 2 ] 2Lys eller varme reducerer aluminiumacetat til at danne tynde lag af palladium. Denne egenskab kan bruges til at producere nanotråde og kolloider .
Noter og referencer
- (en) Denne artikel er helt eller delvist taget fra Wikipedia-artiklen på engelsk med titlen " Palladium (II) acetat " ( se listen over forfattere ) .
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- Sigma-Aldrich ark af forbindelsen Palladium (II) acetat , konsulteret den 14. august 2020.
- Gigiena i Sanitariya. Flyvningen. 51 (12), s. 88, 1986.
- OECD testretningslinje 401
- T. A. Stephenson , SM Morehouse, AR Powell, JP Heffer og G. Wilkinson, “ 667. Carboxylater af palladium, platin og rhodium og deres addukter ”, Journal of the Chemical Society (Genoptaget) ,1965, s. 3632 ( DOI 10.1039 / jr9650003632 )
- Skapski, A C. og ML Smart, " Crystal Structure of Trimeric Palladium (II) Acetate ", J. Chem. Soc. D , n o 11,1970, s. 658b - 659 ( DOI 10.1039 / C2970000658b )
- Kirik, SD, Mulagaleev, SF og Blokhin, AI, " [Pd ( CH3COO ) 2] n fra røntgenpulverdiffraktionsdata ", Acta Crystallogr. C , bind. 60, n o 9,2004, m449 - m450 ( DOI 10.1107 / S0108270104016129 )
- Bakhmutov, VI, Berry, JF, Cotton, FA Ibragimov, S. og Murillo, CA, " Non-Trivial Behavior of Palladium (II) Acetate ," Dalton Transactions , n o 11,2005, s. 1989–1992 ( PMID 15909048 , DOI 10.1039 / b502122g )
- " Homogen katalysator med høj renhed " [ arkiv af17. marts, 2006] , Engelhard ,September 2005(adgang til 24. februar 2006 )
- Stephen K. Ritter , ” Kemikere introducerer en brugervejledning til palladiumacetat, ” Chemical & Engineering News , vol. 94, nr . 18,2. maj 2016, s. 20–21 ( DOI 10.1021 / cen-09418-scitech1 )
- Suggs, J W. "Palladium: Organometallisk kemi." Encyclopædi for uorganisk kemi. Ed. R B. King. 8 flyvninger. Chichester: Wiley, 1994.
- Kirill V. Nikitin , Andryukhova, NP, Bumagin, NA og Beletskaya, IP, “ Syntese af Arylestere ved Pd-katalyseret carbonylering af Aryljodider ”, Mendeleev Communications , bind. 1, nr . 4,1991, s. 129–131 ( DOI 10.1070 / MC1991v001n04ABEH000080 )
- Linli He, Shawn P. Allwein, Benjamin J. Dugan, Kyle W. Knouse, Gregory R. Ott, Craig A. Zificsak, " Synthesis of a-Carboline ", Org. Synth. , Vol. 93,2016, s. 272 ( DOI 10.15227 / orgsyn.093.0272 )
- " Buchwald-Hartwig Cross Coupling Reaction " , portal for organisk kemi
- Gooben, L J. "Forskningsområde" Nye Pd-katalyserede krydskoblingsreaktioner "" 28. feb. 2006 < http://www.mpi-muelheim.mpg.de/kofo/bericht2002/pdf/2.1.8_gossen.pdf > “ https://web.archive.org/web/20070712180504/http://www.mpi -muelheim.mpg.de/kofo/bericht2002/pdf/2.1.8_gossen.pdf ” ( Arkiv • Wikiwix • Archive.is • Google • Hvad skal jeg gøre? ) ,12. juli 2007.
- Herrmann, WA, Brossmer, C., Reisinger, C.-P., Riermeier, TH, Öfele, K. og Beller, M., ” Palladacycles: Effektive Nye Katalysatorer til Heck vinylering af arylhalogenider ”, Chemistry - A European Journal , bind. 3, nr . 8,1997, s. 1357–1364 ( DOI 10.1002 / chem.19970030823 )
- Richard F. Heck , Aldehyder fra allylalkoholer og Phenylpalladium Acetat: 2-methyl-3-phenylpropionaldehyd , Org. Synth. , koll. "flyvning. 6 ”, s. 815