Claisen kondens
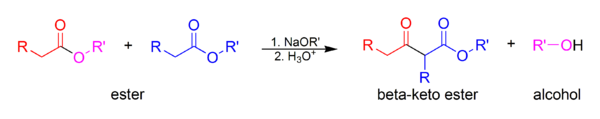
Den Claisen kondensering (ikke at forveksle med Claisen-omlejring ) er et ubikvitært biologisk reaktionsmedium. Det er en reaktion, der danner en carbon-carbonbinding fra to estere (eller to thioestere for eksempel) eller mellem en ester og en carbonylforbindelse i nærvær af en stærk base, der danner en β-ketoester eller en β-di- keton :
|
| En animation af mekanismen |
Det er opkaldt efter Ludwig Claisen, der offentliggjorde en undersøgelse af denne reaktion i 1881.
Forudsætninger
Mindst et af reagenserne skal være enoliserbart (dvs. have et hydrogenatom på alfa-carbon ). Afhængig af reagensernes enoliserbare natur eller ikke, er der forskellige typer Claisen-kondens.
Basen bør heller ikke interferere med en reaktion med nukleofil substitution eller nukleofil tilsætning på carbonylgruppens carbon. Af denne grund anvendes generelt alkoholatet konjugeret med den alkohol, der dannes ved reaktionen (for eksempel natriumethanolat, hvis ethanol dannes ), hvilket yderligere tillader, at alkoholatet regenereres. I "kryds" Claisen-kondensationer kan en ikke-nukleofil base såsom lithiumdiisopropylamid (LDA) anvendes, da kun en forbindelse er enoliserbar. På den anden side kan LDA ikke bruges til "klassiske" kondensationer eller Dieckmann-kondensationer , fordi alle estere kan omdannes til esterenolat, og kondensering derefter ikke kan finde sted.
Den alkoholholdige del af esteren skal også være en god forlader gruppe . Methyl- eller ethylestere anvendes til dette , som danner methonalat- eller ethonalatgrupper.
Typer
Afhængig af reagensernes enoliserbare natur eller ikke er der forskellige typer Claisen-kondens. I den "klassiske" Claisen-kondens anvendes kun en enoliserbar ester:
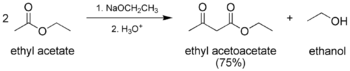
I den "krydsede" Claisen-kondens anvendes en enoliserbar ester eller keton og en ikke-enoliserbar ester:
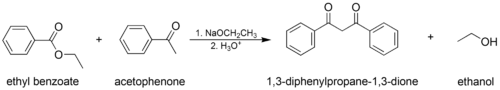
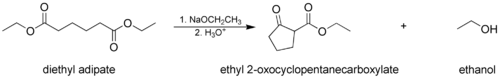
I Dieckmanns kondensering anvendes et molekyle, der bærer to estergrupper, der reagerer intramolekylært for at danne en cyklisk β-ketoester. I dette tilfælde skal den dannede ring indeholde mindst 5 eller 6 atomer for at respektere cyklusspændingen :
Biologi
Vi finder især Claisen-kondensationen under det første ketogenese- trin under kondensationen af to acetyl-CoA til acetoacetyl-CoA .
Det findes også under syntesen af fedtsyrer fra malonyl-CoA, som derefter omdistribueres af fedtsyresyntase for at føre til forlængelse af fedtsyrer under dannelsen.
Variant
Stobbes kondens er en variation af Claisens kondens, der anvender en ravsyre- diester i stedet for esteren og kondenserer på en carbonylforbindelse til dannelse af en α, β-umættet ester. På grund af den større stabilisering af ravsyre carbanion kan der generelt anvendes en svagere base end den, der anvendes i Claisen-kondensationen. Reaktionen har den fordel, at den fungerer med et stort antal alkyl- eller arylsubstituenter, herunder voluminøse substituenter .

Noter og referencer
- (i) FA Carey , organisk kemi , New York, NY, McGraw-Hill ,2011, 8 th ed. , 1333 s. ( ISBN 978-0-07-340261-1 , online præsentation ) , kap. 20 ("Enoler og Enolates") , s. 882-884.
- (De) L. Claisen og A. Claparède , " Condensationen von Ketonen mit Aldehyden " , Ber. Dtsch. Chem. Ges. , Vol. 14, nr . 21881, s. 2460-2468 ( ISSN 0365-9496 , DOI 10.1002 / cber.188101402192 ).
- (De) L. Claisen , " Ueber die Einführung von Säureradicalen in Ketone " , Ber. Dtsch. Chem. Ges. , Vol. 20, nr . 1,1887, s. 655-657 ( ISSN 0365-9496 , DOI 10.1002 / cber.188702001150 ).
- (en) CR Hauser og BE Hudson, Jr. , Organic Reations , bind. 1, John Wiley & Sons ,1942, 402 s. ( ISBN 978-0-471-00462-2 , DOI 10.1002 / 0471264180.or001.09 , online præsentation ) , kap. 9 ("Acetoeddikesyreester-kondens og visse relaterede reaktioner").
- Jerry March (i) , Advanced Organic Chemistry: Reaktioner, Mechanisms, og Structure , New York, Wiley,1985, 3 e ed. , 1345 s. ( ISBN 0-471-85472-7 )