Bergman-reaktion
Den Bergman ringslutning eller ringslutning af Bergman , opkaldt efter kemikeren US Robert Bergman (de) er en omlejringsreaktion i organisk kemi af enediyn et derivat radikal af benzen .
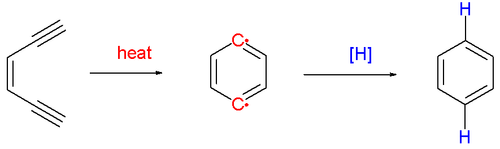
Reaktionen fortsætter ved pyrolyse (over 200 ° C ), hvorved der dannes en 1,4-benzendyl- diradisk forbindelse , en meget reaktiv art. Sidstnævnte reagerer med donorer af hydrogenradikaler, såsom cyclohexa-1,4-dien, hvilket giver den tilsvarende arene . Ved behandling med tetrachlormethan opnås 1,4-dichlorbenzen og med methanol , benzylalkohol .
Når enyn er del af en 10 carbonring (fx cyclodeca-3-en-1,5-diyn i figuren nedenfor), kan reaktionen finde sted ved meget lavere temperaturer ( 37 ° C her) takket være cyklus spænding .

Naturlige forbindelser, såsom calicheamicin, indeholder den samme 10-carbon ringenhed og er cytotoksiske . De genererer den mellemliggende diradical beskrevet ovenfor, som kan skære DNA -enkeltstrenget og dobbeltstrenget. Der er nye lægemidler baseret på denne egenskab, herunder monoklonale antistoffer som mylotarg .
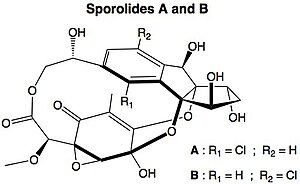
En diradisk mekanisme foreslås også til dannelse af visse biomolekyler af marine oprindelse, sporoliderne , som indeholder en cholorbenzen i deres struktur.
I denne mekanisme er halogenidsalt kilden til halogenet. En modelreaktion med cyclodeca-1,5-diyn-3-en , lithiumbromid som kilde til halogen, eddikesyre som kilde til hydrogen i DMSO ved 37 ° C gør denne teori levedygtig:

Reaktionen er af første orden i dannelse af p- benzzyne A som et begrænsende trin . Halogenidionen giver derefter to elektroner under dannelsen af den nye binding Br-C, og de radikale elektron transitter via en C1-C4-bindende flygtig til dannelse af mellemproduktet anion B . Denne anion er en stærk base, der er i stand til at strippe protoner selv fra DMSO for at give det endelige produkt. Der observeres ingen dannelse af dibrom- eller dihydrogenforbindelserne.
eksterne links
- (en) Bergman Cycloaromatization Powerpoint Whitney M. Erwin 2002
- (in) Bergman Cycloaromatization Organic Chemistry Portal
Noter og referencer
- Navn Reaktioner: En samling af detaljerede reaktionsmekanismer af Jie Jack Li Udgivet 2003 Springer ( ISBN 3-540-40203-9 )
- (i) Design og syntese af heterocykliske fusioneret enediyn aktiverede prolægemidler efter behag Luca Banfi Andrea Basso Giuseppe GUANTI, og Renata Riva arkivoc 2006 HL-1786GR 261-275 Abstract
- (i) Charles L. Perrin , Betsy L. Rodgers og Joseph M. O'Connor , " nukleofil addition til en p-benzyn Stammer fra år endiyn: en ny mekanisme for halogenid Inkorporering i biomolekyler " , Journal of American Chemical Society , vol. 129, nr . 15,2007, s. 4795-4799 ( DOI 10.1021 / ja070023e )
- Ny rute for Halide-tilsætning Stu Borman Chemical & Engineering News 2. april 2007 Link
- ( fr ) Denne artikel er helt eller delvist hentet fra den engelske Wikipedia- artikel med titlen " Bergman cyclization " ( se listen over forfattere ) .