Pinnick oxidation
Den Pinnick oxidation er en reaktion af organisk kemi , der består af en oxidation af en aldehyd til carboxylsyren svarende. Det blev udviklet i 1981 af Harold Pinnick fra Lindgrens og Kraus 'arbejde.
Det oxiderende reagens er natriumchlorit, og tilsætningen til reaktionsmediet af 2-methylbut-2-en gør det muligt at undgå overoxidation af substratet. Reaktionen udføres i nærværelse af en buffer af natriumdihydrogenphosphat .
Mekanisme
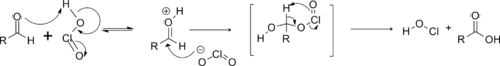
Den reaktionsmekanisme begynder med dannelsen af chlorsyrling ved reaktion mellem chlorit og dihydrogenphosphat.
Klorsyren protonerer derefter aldehydet, hvilket fremhæver elektrofiliciteten af dets funktionelle kulstof, som derefter gennemgår nukleofilt angreb af den frigjorte chlorition. En samordnet mekanisme tillader fjernelse af hypochlorsyre og dannelsen af den ønskede carboxylsyre .
Side reaktioner
Den hypochlorsyre, der dannes under reaktionen, er ansvarlig for to sidereaktioner.
I den første reagerer det med chloritioner for at danne chlordioxid og chloridioner .
Den hypochlorsyre er en oxidant, der er stærkere end chloritionen. Det vil derfor have en tendens til at oxidere andre funktioner i substratet end aldehydfunktionen. For at undgå denne overoxidering tilsættes et overskud af 2-methylbut-2-en til mediet .

Anvendelser
Anvendelsen af 2-methylbut-2-en gør det muligt at oxidere en bred vifte af umættede substrater uden at angribe carbon-carbon dobbeltbindinger , selv i tilfælde af α, β-umættede aldehyder. Grupper hydroxyl , epoxy , benzylether, halogenider og stannaner er stabile under reaktionsbetingelserne.
Det mulige stereogene centrum i α af carbonylet ændres ikke ved reaktionen. Denne egenskab er blevet udnyttet under samlede synteser af molekyler indeholdende stereogene centre i α af de funktioner, der skal oxideres. Dette er for eksempel tilfældet i syntesen af ditryptophrenalin af Overman i 2001, hvor en alkohol omdannes til carboxylsyre ved kæden af en Dess-Martin- oxidation og en Pinnick-oxidation eller ved syntesen af den zaragozikesyre, for hvilken en Swern-oxidation over Pinnick-oxidation. I sidstnævnte eksempel er andre oxidationsreaktioner, såsom Jones- oxidation eller Ley-oxidation, blevet forsøgt uden succes.
Noter og referencer
- (fr) Denne artikel er helt eller delvist taget fra Wikipedia-artiklen på engelsk med titlen " Pinnick oxidation " ( se listen over forfattere ) .
- Kürti og Czakó 2005 , s. 354
- Dalcanale, E; Montanari, F; " Selektiv oxidation af aldehyder til carboxylsyrer med natriumchlorit-hydrogenperoxid ", Journal of Organic Chemistry , bind. 51,1986, s. 567-569 ( DOI 10.1021 / jo00354a037 )
- Ishihara, J .; Hagihara, K.; Chiba, H.; Det ok .; Yanagisawa, Y.; Totani, K; Tadano, K., “ Syntetiske undersøgelser af viridenomycin. Konstruktion af cyclopentencarboxylsyre-delen ”, Tetrahedron. Lett. , Vol. 41,2000, s. 1771–1774 ( DOI 10.1016 / S0040-4039 (00) 00013-7 )
- Kuramochi, K.; Nagata, S.; Itaya, H. Takao, H.; Kobayashi, S., “ Convergent Total Synthesis of epolactaene: application of bridgehead oxiranyl anion strategy ”, Tetrahedron. Lett. , Vol. 40,1999, s. 7371–7374 ( DOI 10.1016 / S0040-4039 (99) 01512-9 )
- Raach, A.; Reiser, O., " Sodium Chlorite-Hydrogen Peroxide, a Mild and Selective Reagent for the Oxidation of Aldehydes to Carboxylic Acids ", Journal für praktische Chemie , bind. 342,2000, s. 605–608 ( DOI 10.1002 / 1521-3897 )
Bibliografi
- (en) László Kürti og Barbara Czakó , strategiske anvendelser af navngivne reaktioner i organisk syntese: Baggrund og detaljerede mekanismer , Elsevier Academic press,2005( ISBN 0-12-429785-4 )
- Nicolas Rabasso , Organisk kemi: 2. Heteroelementer, syntetiske strategier og organometallisk kemi , De Boeck , koll. "LMD-kemi",oktober 2009, 536 s. ( ISBN 978-2-8041-0168-8 , læs online )

