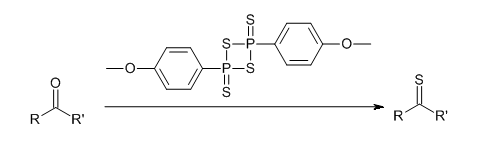
Lawessons reagens
| Lawessons reagens | |
| Identifikation | |
|---|---|
| IUPAC navn | 2,4-bis (4-methoxyphenyl) -1,3-dithia-2,4-diphosphetan 2,4-disulfid |
| N o CAS | |
| N o ECHA | 100.038.944 |
| N o EF | 242-855-4 |
| PubChem | 87949 |
| SMILE |
COC1 = CC = C (C = C1) P2 (= S) SP (= S) (S2) C3 = CC = C (C = C3) OC , |
| InChI |
InChI: InChI = 1S / C14H14O2P2S4 / c1-15-11-3-7-13 (8-4-11) 17 (19) 21-18 (20,22-17) 14-9-5-12 ( 16-2) 6-10-14 / h3-10H, 1-2H3 |
| Kemiske egenskaber | |
| Brute formel |
C 14 H 14 O 2 P 2 S 4 [isomerer] |
| Molar masse | 404,467 ± 0,033 g / mol C 41,57%, H 3,49%, O 7,91%, P 15,32%, S 31,71%, |
| Fysiske egenskaber | |
| T ° fusion | 229 ° C |
| Enheder af SI og STP, medmindre andet er angivet. | |
Det Lawessons reagens er en kemisk forbindelse organisk middel anvendt som en thionering . Det blev populært af Sven-Olov Lawesson, som imidlertid ikke er opfinderen.
Lawessons reagens er mere reaktiv end Belleaus reagens , men mindre end Davys reagenser .
Thionation
Thioneringsreaktionen omdanner en carbonyl til thiocarbonyl . Lawessons reagens er det mest anvendte reagens, da det gør det muligt at arbejde ved højere temperaturer end hydrogensulfid og er mere opløseligt i organiske opløsningsmidler end diphosphorpentasulfid .
Mekanisme
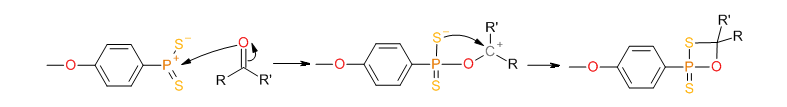
De aktive steder i molekylet aktiveres ved åbningen af den centrale ring dannet af fosfor og svovl. Denne åbning udføres hovedsageligt termisk:
Også opdaterede dithiophosphinylider kan reagere med carboxylgruppen til dannelse af et thiaoxaphosphetan-mellemprodukt:
Dannelsen af en stabil P = O dobbeltbinding skifter reaktionen til højre og fører til adskillelsen af mellemproduktet:
Denne reaktion ligner Wittig-reaktionen og er gyldig for ketoner , amider og lactamer . Da estere reagerer under mere aggressive reaktionsbetingelser, er det muligt at udføre selektive thionationer.
Produktion og syntese
Lawessons reagens syntetiseres fra anisol og diphosphorpentasulfid .

Se også
Noter og referencer
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- (i) " Lawessons reagens " om ChemIDplus , adgang til 18. januar 2010
- (i) T. Molina , Mr. Yanez , O. MB , R. Notario og J.-LM Abboud , The thiocarbonylgruppe , Chichester / New York / Brisbane etc., John Wiley & Sons Ltd, al. "Den funktionelle gruppekemi / Kemien i dobbeltbundet funktionel gruppe",1997, 1858 s. ( ISBN 0-471-95956-1 )
- " Lawessons reagens. Forberedelse, handlingsmekanisme, anvendelser, noter ” på boowiki.info (adgang til 17. februar 2021 )
- (i) Martin Jesberger , Thomas P. Davis og Leonie Barner , " Applications of Lawessons reagens i organisk og Organometalliske Synteser " , Synthesis , Vol. 13,Marts 2003
- Thomsen, I.; Clausen, K.; Scheibye, S.; Lawesson, S.-O. , Thiation med 2,4-bis (4-methoxyphenyl) -1,3,2,4-dithiadiphosphetan 2,4-disulfid: N-methylthiopyrrolidon , Org. Synth. , koll. "flyvning. 7 ",1990, s. 372