Carboxylsyre
Udtrykket carboxylsyre henviser til et molekyle, der omfatter en carboxylgruppe (–C (O) OH). De er syrer, og deres konjugerede baser kaldes carboxylationer .
I organisk kemi , en carboxylgruppe er en funktionel gruppe bestående af et atom af carbon , bundet af en dobbeltbinding til et atom af oxygen og bundet med en enkeltbinding til en gruppe hydroxyl -OH.
Generel
I kemi , carboxylsyrerne R-COOH udgør med sulfonsyrer R-SO 3 H de to typer af syrer af organisk kemi . De findes rigeligt i naturen som fedtsyre ( lipid ) og er meget vigtige inden for industriel kemi . For eksempel er eddikesyre ikke kun en vigtig byggesten for de komplekse molekyler, der findes i biologi , men er også et industrielt produceret molekyle, der findes i eddike . En af de mest kendte er acetylsalicylsyre eller aspirin. Byggestenen til proteiner , aminosyrer er carboxylsyrer.
Den karakteristiske funktionelle gruppe er carboxylgruppen, hvor R er hydrogen eller en organisk gruppe:

Carboxylsyrerne har det rå formel C n H 2 n O 2 når R er en alkyl -gruppe . Beregning af antallet af umættethed giver: . Denne umætning afspejler kulstof-ilt dobbeltbinding .
Carboxylgrupper skrives ofte i reduceret form: -COOH (ikke-ioniseret form af gruppen). Den ioniserede form af gruppen er: -COO - .
Dette er altid placeret i slutningen af kulstofkæden . Tilsætningen af en carboxylgruppe til en organisk forbindelse er en carboxylering , fjernelsen af den samme gruppe er en decarboxylering .
Carboxylationer
Dette er de konjugerede baser R-COO - carboxylsyrer. Disse baser er generelt ret svage . Den negative ladning på molekylet delokaliseres på de to oxygenatomer i carboxylgruppen ved mesomerisme, hvilket forklarer den relative stabilitet af denne type molekyler.

Den carboxylation er et amfifilt overfladeaktivt middel , er det detergent- arter af sæbe . Faktisk er _COO-carboxylatgruppen hydrofil, fordi den er meget polær . På den anden side er carbonkæden R apolar og derfor hydrofob og lipofil .
Nomenklatur
- Systematic: hvis carbonatomet af carboxylgruppen gruppe COOH indgår i hovedkæden på tilsvarende carbonhydrid (med samme antal carbonatomer, med CH 3 . I stedet for COOH), er navnet på denne fulgt carbonhydrid med suffikset " -oic "(dioic for en disyre) og forud for det med ordet" acid ". Ellers (i cykliske serie for eksempel), ordet ” syre ” er efterfulgt af navnet på det carbonhydrid, som suffix ”-carboxylsyre” tilsættes.
| Klasse | Formel * for den karakteristiske gruppe |
Suffiks |
|---|---|---|
| Carboxylsyrer | - (C) OOH- COOH |
syre- ... oinsyre ... -carboxylsyre |
- heptansyre CH 3 (CH 2 ) 5 -COOH kan alternativt navngives hexan-1-carboxylsyre, hvis carbonatom i -COOH ikke er inkluderet i kæden nummerering;
- HOOC- (CH 2 ) 5 -COOH heptandisyre er en dicarboxylsyre . Suffikset -oic er forud for det multiplikative præfiks di- ;
- cyclopentancarboxylsyre: -COOH .
- Usædvanligt: Som mange organiske forbindelser har carboxylsyrer almindelige navne, der ofte bruges i litteraturen og husker kilden, hvorfra de først blev isoleret. En liste defineret af IUPAC regulerer imidlertid brugen af trivielle navne, der accepteres sammen med systematiske navne.
| Type | Struktur | IUPAC navn | almindeligt navn | Kilde |
|---|---|---|---|---|
| Alifatiske monosyrer | H-COOH | methansyre | myresyre | udskilles af nogle myrer (latin: formica , myrer) |
| CH 3 COOH | ethansyre | eddikesyre | Latin: acetum , eddike | |
| CH 3 CH 2 COOH | propansyre | propionsyre | Græsk: bonde , fedt | |
| CH 3 (CH 2 ) 2 -COOH | butansyre | smørsyre | Græsk: bouturos , smør | |
| CH 3 (CH 2 ) 3 -COOH | pentansyre | valerinsyre | baldrian | |
| CH 3 (CH 2 ) 4 -COOH | hexansyre | capronsyre | ||
| CH 3 (CH 2 ) 5 -COOH | heptansyre | enantinsyre | ||
| CH 3 (CH 2 ) 6 -COOH | octansyre | caprylsyre | kokosnød , modermælk | |
| CH 3 (CH 2 ) 7 -COOH | nonansyre | pelargonsyre | ||
| CH 3 (CH 2 ) 8 -COOH | decansyre | caprinsyre | ||
| CH 3 (CH 2 ) 9 -COOH | undekansyre | undecylsyre | ||
| CH 3 (CH 2 ) 10 COOH | dodecansyre | laurinsyre | kokosolie | |
| CH 3 (CH 2 ) 11 COOH | tridecansyre | tridecylsyre | ||
| CH 3 (CH 2 ) 12 COOH | tetradecansyre | myristinsyre | muskatnød | |
| CH 3 (CH 2 ) 13 COOH | pentadecansyre | pentadecylsyre | ||
| CH 3 (CH 2 ) 14 COOH | hexadecansyre | palmitinsyre | palmeolie | |
| CH 3 (CH 2 ) 15 COOH | heptadecansyre | margarinsyre | ||
| CH 3 (CH 2 ) 16 COOH | octodecansyre | stearinsyre | animalsk fedt | |
| CH 3 (CH 2 ) 17 COOH | nonadecansyre | nonadecylsyre | ||
| CH 3 (CH 2 ) 18 COOH | eicosansyre | arachidinsyre | olie jordnødder , fiskeolier og vegetabilske olier | |
| CH 3 (CH 2 ) 20 COOH | docosansyre | behensyre | ||
| Aromatiske monosyrer | C 6 H 5 -COOH | benzoesyre | benzen | |
| HO-C 6 H 4 -COOH | 2-hydroxybenzoesyre | salicylsyre | frugt (som methylsalicylat ) | |
| Thiol syrer | CH 3 CH (SH) -COOH | 2-mercaptopropansyre | thiolaktinsyre |
NB: en mnemonisk enhed til at huske navnene på lineære syrer i stigende rækkefølge af antallet af carbonatomer er følgende sætning: " O n M angel S aucisse G rillée A P salvet" ( O xalique, M alonique, S uccinic , G lutaric, A dipic, P imelic). Diacider anvendes til syntese af polyamider og polyestere .
Andre typer carboxylsyrer kan nævnes: dicarboxylsyrer , tricarboxylsyrerne , syrene alfa- hydroxylés , ketosyrerne , aminosyrerne og fedtsyrerne .
Fysiske og strukturelle egenskaber
stat
Carboxylsyrer er flydende under normale forhold, så længe deres carbonkæde har mindre end otte carbonatomer. De er solide ud over det.
Syrer med lav molekylvægt har en stærk lugt; for eksempel er butansyre ansvarlig for lugten af harskt smør.
Polaritet, opløselighed
Carboxylsyrefunktionen er stærkt polær og er både donor og acceptor af hydrogenbindinger . Dette muliggør dannelse af hydrogenbindinger, for eksempel med et polært opløsningsmiddel, såsom vand, alkohol og andre carboxylsyrer.

På grund af denne egenskab er små carboxylsyrer (op til butansyre) fuldstændigt opløselige i vand. Syremolekyler er også i stand til at danne stabile dimerer ved hydrogenbinding, hvilket forklarer, hvorfor deres kogepunkt er højere end for de tilsvarende alkoholer.
Surhed
I opløsning i vand dissocieres syren delvist i carboxylationen i henhold til balanceligningen :
Disse er svage syrer i vand ( p K A mellem 4 og 5).
Ligesom alkoholer viser carboxylsyrer en sur og basisk karakter: deprotonering til carboxylationer er let, men protonering er vanskeligere. De har derfor en lavere p K A end alkoholerne. Faktisk forklares surhedsgraden af carboxylsyrer af den induktive virkning i carboxylgruppen: C = O-bindingen er meget polariseret ( elektronegativitet af ilt større end kulstof), hvilket gør kulstof elektrofil. , Og derfor tiltrækker det elektroner fra andet ilt. Nu er dette andet ilt i sig selv forbundet med et brint, og denne binding er også polariseret , så elektronen af brintet, som har nærmet sig ilt, tiltrækkes igen af det elektrofile kulstof. Dette hydrogen bliver derfor meget let mobilt, derfor er surhedsgraden i carboxylgruppen.
Opløseligheden af carboxylsyren stiger med pH .
Spektroskopi
I infrarød (IR) har carboxylsyren to valensbånd:
| Vibrationer | C = O | OH |
|---|---|---|
| Bølgetal (cm −1 ) | 1.680-1.710 | 2.500-3.200 |
| Intensitet | (stærk) | stor, medium til stærk |
Struktur

Ifølge VSEPR teori :
- geometrien omkring kulstofatomet (bindinger) er af trigonal type;
- geometrien omkring oxygenatom i carbonylfunktionen (dobbeltbinding + frie dubletter) er også af trigonal type;
- geometrien omkring oxygenatomet i hydroxyfunktionen (obligationer + frie dubletter) er af tetraedrisk typen (AX 2 E 2 ).
Carboxylsyre har flere mesomere former .
Reaktivitet
Som vist blandt andet de forskellige mesomere formler af carboxylsyre:
- oxygenatomer er nukleofile steder såvel som Lewis-baser;
- det centrale kulstof er elektrofilt;
- det elektrofile hydrogenatom er surt.
Derivater
Carboxylsyrer har mange derivater:
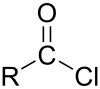
-
Syreanhydrid
- de esterne
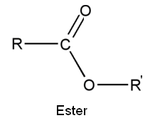
- de amider

- den nitril
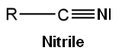
Med hensyn til at forlade gruppen (nukleofuge) er rækkefølgen af lethed:
Cl - (acylchlorid), RCOO - (anhydrid), RO - (ester), - NH 2 og - NR 1 R 2 (amider).
Reduktion
Oxidation
- Kuldioxid (CO 2)
Syntese
Syntese ved oxidation
alkoholer eller aldehyder Carboxylsyrer kan opnås ved oxidation af aldehyder , derfor faktisk ved dobbelt oxidation af primære alkoholer .af alkener eksempel: syntese af eddikesyre ved oxidation af propen
Syntese fra et syrerivat
Det er simpelthen hydrolyserne af de forskellige syrederivater.
ester- hydrolyse i surt medium: retroesterificering
- hydrolyse i et basisk medium: forsæbning af esteren
Syntese ved reaktion af et Grignard-reagens på carbondioxid
ReaktionSyntesen finder sted ved lav temperatur ( -40 ° C ). Kuldioxiden er derefter i fast form, kaldet tøris . Det overskydes. Efter reaktion udføres hydrolyse i et surt medium til opnåelse af carboxylsyren.
MekanismeFørste trin : tilsætning af Grignard-reagenset til CO 2

Andet trin : hydrolyse i et surt medium
Malonisk syntese
Malonsyntese er et sæt reaktioner, der gør det muligt at syntetisere mange primære eller sekundære carboxylsyrer fra diethylmalonat .
Hun er sammensat:
- en syre-base reaktion mellem diethylmalonat og ethanoat ( natrium , kalium osv. );
- en nukleofil substitution , hvor den ønskede gruppe (primær eller sekundær) indsættes for den endelige carboxylsyre;
- en dobbelt forsæbning af de to esterfunktioner af det substituerede diethylmalonat efterfulgt af forsuring af mediet;
- decarboxylering (frigivelse af kuldioxid ved opvarmning);
- omlejring af slutproduktet i carboxylsyre ved tautomerisme .
Denne syntese er så meget mere interessant som a priori , det gør det muligt at syntetisere en hvilken som helst carboxylsyre, for ud fra en tertiær gruppe, forekommer det, at vi kan sætte hvad vi ønsker i stedet for R .
Noter og referencer
- R. Panico og J.-C. Richer, IUPAC nomenklatur af organiske forbindelser , Masson, 1994, s. 70, 118- ( ISBN 978-2-225-84479-9 ) . Et suffiksarray (og præfikser), der bruges til at beskrive nogle vigtige karakteristiske grupper i substitutiv nomenklatur, er tilgængeligt i en reference IUPAC online (på engelsk): suffikser og præfikser for hovedkarakteristik Nogle grupper i substitutiv nomenklatur .
- Robert Panico, Jean-Claude Richer og Jean Rigaudy , Nomenklatur og terminologi i organisk kemi - Funktionelle klasser. Stereokemi , ingeniørteknikker , 1996, s. 20 ( ISBN 2 85 059-001-0 ) .
- http://www.acdlabs.com/iupac/nomenclature/93/r93_705.htm











