Hydrazin
| Hydrazin | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 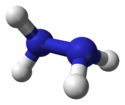 Dimensioner og 3D-model af hydrazin |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikation | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC navn | hydrazin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
diazan, diamin |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.005.560 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EF | 206-114-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 8058 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILE |
NN , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / H4N2 / c1-2 / h1-2H2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Udseende | hygroskopisk væske, farveløs, røgfyldt, med en skarp lugt. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formel | N 2 H 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar masse | 32,0452 ± 0,0007 g / mol H 12,58%, N 87,42%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolært øjeblik | 1,75 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekylær diameter | 0,390 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusion | 2 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kogning | 114 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighed | blandbar med vand og polære organiske opløsningsmidler |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighedsparameter δ |
37,3 MPa 1/2 ( 25 ° C ) 36,2 J 1/2 · cm -3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumenmasse |
1010 kg · m -3
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | 38 ° C ( cf ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosionsgrænser i luft | 1,8 - 100 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
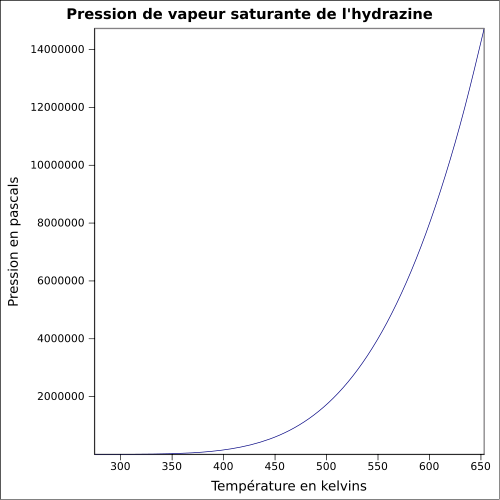
| Mættende damptryk | vandfri: 21 mbar ( 20 ° C ), opløsning ved 64 % m : ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynamisk viskositet | 0,9 mPa · s ved 25 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | 147,0 bar , 379,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gas, 1 bar | 238,68 J · K- 1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 væske, 1 bar | 121,52 J · K- 1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | 95,35 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 væske | 50,63 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° |
41,8 kJ · mol -1 ( 1 atm , 113,55 ° C ); 44,7 kJ · mol -1 ( 1 atm , 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| STK | 667,1 kJ · mol -1 ( 25 ° C , gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | -622,08 kJ · mol -1 (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ioniseringsenergi | 8,1 ± 0,15 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brydningsindeks | 1.469 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
     Fare H226, H301, H311, H314, H317, H331, H350, H410, P201, P261, P273, P280, P301 + P310, P305 + P351 + P338, H226 : Brandfarlig væske og damp H301 : Giftig ved indtagelse H311 : Giftig ved hudkontakt H314 : Forårsager svære forbrændinger af huden og øjenskader H317 : Kan forårsage en allergisk hudreaktion H331 : Giftig ved indånding H350 : Kan forårsage kræft (angive eksponeringsvej hvis det er endeligt bevist, at ingen andre eksponeringsveje forårsager faren) H410 : Meget giftig for vandlevende organismer, med langvarige virkninger P201 : Få specielle instruktioner inden brug. P261 : Undgå indånding af støv / røg / gas / tåge / dampe / spray. P273 : Undgå udledning til miljøet. P280 : Bær beskyttelseshandsker / beskyttelsestøj / øjenbeskyttelse / ansigtsbeskyttelse. P301 + P310 : Ved indtagelse: Søg straks et GIFTINFORMATION eller en læge. P305 + P351 + P338 : Ved øjnene: Skyl forsigtigt med vand i flere minutter. Fjern kontaktlinser, hvis offeret har dem på, og de let kan fjernes. Fortsæt med at skylle. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   B3, D1A, D2A, E, B3 : Brændbar væske D1A : Meget giftigt materiale, der forårsager øjeblikkelige alvorlige virkninger D2A : Meget giftigt materiale, der forårsager andre toksiske virkninger E : Ætsende materiale 0,1% offentliggørelse i henhold til listen over ingredienser |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 3 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Andet | Kan angribe nervesystemet. Dødelig i høje doser. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
0113 : GUANYL NITROSAMINOGUANYLIDENE HYDRAZINE FUGTET med mindst 30 procent (masse) vand Klasse: 1 Klassifikationskode: 1.1A : Stoffer og genstande, der medfører risiko for masseeksplosion (en masseeksplosion er en eksplosion, som næsten øjeblikkeligt påvirker næsten alle af lastningen). Primært eksplosivt materiale. Mærkat: 1 : Eksplosive stoffer og genstande 
663 : meget giftigt og brandfarligt materiale (flammepunkt lig med eller mindre end 60 ° C ) UN-nummer : 1163 : ASYMMETRISK DIMETHYLHYDRAZIN Klasse: 6.1 Klassificeringskode: TFC : Brandfarlige ætsende giftige stoffer. ; Mærkater: 6.1 : Giftige stoffer 3 : Brandfarlige væsker 8 : Ætsende materialer   
663 : meget giftigt og brandfarligt materiale (flammepunkt lig med eller mindre end 60 ° C ) UN-nummer : 1244 : METHYLHYDRAZINE Klasse: 6.1 Klassificeringskode: TFC : Brandfarlige ætsende giftige stoffer. ; Mærkater: 6.1 : Giftige stoffer 3 : Brandfarlige væsker 8 : Ætsende materialer   
886 : meget ætsende og giftigt materiale UN-nummer : 2029 : ANHYDROUS HYDRAZINE Klasse: 8 Klassificeringskode: CFT : Ætsende stoffer flydende, brandfarligt, giftigt; Labels: 8 : Ætsende materials 3 : brandfarlige væsker 6.1 : Giftige materials Emballage: Packing gruppe I : meget farlige materialer;   
86 : ætsende eller viser en mindre grad af ætsningsevne og toksicitet UN-nummer : 2030 : HYDRAZINEHYDRAT indeholdende mere end 37 procent, men ikke mere end 64 procent (masse) hydrazin; eller HYDRAZINE AQUEOUS SOLUTION indeholdende mere end 37%, men ikke mere end 64% (efter vægt) hydrazin Klasse: 8 Klassificeringskode: CT1 : Giftige ætsende stoffer: Væsker; Labels: 8 : Ætsende stoffer 6.1 : Giftige stoffer Emballage: Pakning gruppe I / II : meget / moderat farlige stoffer;  
86 : ætsende eller viser en mindre grad af ætsningsevne og toksicitet UN-nummer : 2030 : HYDRAZINEHYDRAT indeholdende mere end 37 procent, men ikke mere end 64 procent (masse) hydrazin; eller HYDRAZINE AQUEOUS SOLUTION indeholdende mere end 37%, men ikke mere end 64% (efter vægt) hydrazin Klasse: 8 Klassificeringskode: CT1 : Giftige ætsende stoffer: Væsker; Labels: 8 : Ætsende stoffer 6.1 : Giftige stoffer Emballage: Packing gruppe III : stoffer med lav fare.  
663 : meget giftigt og brandfarligt materiale (flammepunkt lig med eller mindre end 60 ° C ) UN-nummer : 2382 : SYMMETRISK DIMETHYLHYDRAZINE Klasse: 6.1 Klassifikationskode: TF1 : Brandfarlige giftige materialer: Væsker; Labels: 6.1 : Giftige materials 3 : brandfarlige væsker Emballage: Packing gruppe I : meget farlige materialer;  
60 : materiale giftig eller udviser en mindre grad af toksicitet UN-nummer : 2572 : PHENYLHYDRAZINE Klasse: 6.1 Klassificeringskode: T1 : Giftige stoffer uden subsidiær risiko: Organisk, væske; Label: 6.1 : Giftige stoffer Emballage: Pakning gruppe II : moderat farlige stoffer; 
3165 : AIRCRAFT HYDRAULIC MOTOR BRÆNDSTOFTANK indeholdende en blanding af vandfri hydrazin og monomethylhydrazin (M86 brændstof) Klasse: 3 Klassificeringskode: FTC : Brandfarlig, giftig, ætsende væsker Mærker: 3 : Væsker brandfarlige 6.1 : Giftige stoffer 8 : Ætsende stoffer Emballage: Emballage gruppe I : meget farlige stoffer;   
60 : materialetoksisk eller udviser en mindre grad af toksicitet UN-nummer : 3293 : HYDRAZINE AQUEOUS SOLUTION, der ikke indeholder mere end 37% (masseprocent) hydrazin Klasse: 6.1 Klassificeringskode: T4 : Giftige stoffer uden subsidiær risiko: Uorganisk, væske; Label: 6.1 : Giftige stoffer Emballage: Packing gruppe III : stoffer med lav fare.  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IARC- klassificering | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe 2B: Muligvis kræftfremkaldende for mennesker | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Økotoksikologi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -3,1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lugtgrænse | lav: 3 ppm høj: 4 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheder af SI og STP, medmindre andet er angivet. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den hydrazin , officielle navn diazane af kemiske formel N 2 H 4 og strukturformel H 2 N-NH 2 , er en kemisk forbindelse farveløs væske med en lugt, der minder om ammoniak . Det er blandbart med vand i alle forhold.
Hydraziner udgør også en familie af kemiske forbindelser afledt af hydrazin (H 2 N-NH 2 ved substitution af et eller flere H-atomer efter carbonhydridgrupper (f.eks 2,4-dinitrophenylhydrazin ).
Den årlige produktion af hydrazin er 260.000 tons. Det meste af denne produktion anvendes som et skummiddel til fremstilling af opskumede polymerer . Resten af denne produktion er opdelt i forskellige sektorer såsom organisk kemi til syntese af lægemidler eller uorganisk kemi til produktion af natriumazid , det eksplosive middel til oppustning af " airbags " (oppustelige sikkerhedspuder). Hydrazin kan også bruges som raketmotorbrændstof .
Molekylær struktur og egenskaber
Strukturen af hydrazin præsenteres som to ammoniakmolekyler koblet til hinanden ved at fjerne et hydrogen for hvert af de to molekyler. Hver -NH 2 underenhed er i en pyramideform. Afstanden mellem de to nitrogenatomer er 145 µm , og molekylet antager en antiklinisk konformation. Momentet er dobbelt så stort som etan . Dens strukturelle egenskaber ligner dem af hydrogenperoxidgas , som anvender en "asymmetrisk" konformation svarende til en lineær alkanstruktur med et højt drejningsmoment.
Det har egenskaberne af en base, der kan sammenlignes med ammoniak , men 15 gange svagere.
Substituenten på hver amin gør den elektroniske dublet mindre tilgængelig til at optage en proton og derfor mindre basisk. Hydrazin er en bedre nukleofil end ammoniak på grund af frastødning mellem de ikke-bindende dubletter af tilstødende nitrogenatomer.
Den anden protonation er sværere:
[N 2 H 5 ] ++ H + → [N 2 H 6 ] 2+ ; K = 8,4 × 10-16Hydrazin er et meget stærkere reduktionsmiddel i et basisk miljø end i et surt miljø. (E = -0,23 V ved pH = 0 og E = -1,16 V ved pH = 14). Når hydrazin reagerer med oxidanter, kan forskellige nitrogenholdige produkter dannes, men det er normalt dinitrogen. Reaktionen af hydrazin med dioxygen danner dinitrogen og vand, mens den frigiver en stor mængde varme.
Hydrazin N 2 H 4nedbrydes under påvirkning af varme og ultraviolette stråler til nitrogen N 2, Hydrogen H 2og ammoniak NH 3.
Nogle salte af hydrazin er eksplosive : nitrat hydrazin , chlorat hydrazin perchlorat hydrazin og azid hydrazonium.
Fysisk-kemiske egenskaber
Vandfri hydrazin er en farveløs, luftrygende væske med en amin-lugt. Lugtgrænsen er 3 ppm .
Syntese
Theodor Curtius syntetiserede først simpelt hydrazin i 1889 gennem bagdøren.
Hydrazin produceres ved Olin Raschigs proces fra natriumhypochlorit og ammoniak , en metode, der blev opfundet i 1907. Denne proces er afhængig af reaktion mellem chloraminer og ammoniak.
NH 2 Cl+ NH 3→ H 2 N - NH 2+ HCI .Den nødvendige monochloramin produceres på forhånd ved reaktionen: NH 3 + HOCI → NH 2 Cl + H 2 OEn variant af Olin Raschigs proces er oxidationen af urinstof med natriumhypochlorit :
(H 2 N) 2 C = O+ NaOCI + 2 NaOH → N 2 H 4+ H 2 O+ NaCl + Na 2 CO 3.I Atofina-PCUK-cyklussen fremstilles hydrazin i flere trin fra acetone , ammoniak og hydrogenperoxid. Acetonen og ammoniak reagerer først for at give en imin efterfulgt af reaktionsoxidation med hydrogenperoxid i oxaziridin , en heterocyklus til tre atomer omfattende et carbonatom, et nitrogenatom og et oxygenatom efterfulgt af ammoniolysis, hvilket resulterer i hydrazon , en proces der samler to nitrogenatomer. Hydrazonen reagerer med det overskydende acetone, og den producerede acetoneazin hydrolyseres til dannelse af hydrazin og regenererer acetonen. I modsætning til Raschig-processen genererer denne metode ikke salt. PCUK er tilknyttet Ugine Kuhlmann , en fransk producent af kemikalier.
Hydrazin kan også produceres ved en fremgangsmåde kendt som ketazin- og peroxidprocessen .
I 2001 opdagede Marc Strous, en mikrobiolog ved universitetet i Nijmegen i Holland, at hydrazin produceres af gær og en oceanisk bakterie , Brocadia anammoxidans , gennem en anammox- reaktion udført i specialiserede organeller kaldet anammoxosomes . De er de eneste levende organismer, der i øjeblikket er kendt for, at de naturligt kan producere hydrazin.
Derivater
Mange hydrazinsubstitutionsderivater er kendte, og flere af dem produceres naturligt. Nogle eksempler:
- den gyromitrine (i) og agaritine (i) er phenylhydraziner fundet i en art af svampe, der dyrkes og markedsføres af have-champignon . Gyromitrin metaboliseres til monomethylhydrazin ;
- den iproniazid , den hydralazin og phenelzin (en) er lægemidler fremstillet af hydrazin;
- den 1,1-dimethylhydrazin (UDMH) og 1,2-dimethylhydrazin (en) er hydraziner, hvor to hydrogenatomer er erstattet med methylgrupper ;
- den 2,4-dinitrophenylhydrazin (2,4-DNPH) er almindeligt anvendt til afprøvning af ketoner og aldehyder i organisk kemi ;
- den phenylhydrazin , C 6 H 5 NHNHz 2 , hydrazin er den første til at blive opdaget.
Anvendelse i kemi
Hydraziner anvendes til syntesen af mange organiske molekyler, og mange af dem er af praktisk betydning i den farmaceutiske industri som et lægemiddel mod tuberkulose såvel som i tekstiler som farvestof og i fotografering.
Det findes også i industrien generelt og mere specielt blandet med fodervand til dampkedler. Dens formål er at ødelægge de sidste iltmolekyler og dermed forhindre korrosion af ståldampledningerne.
Reaktion med carbonyler
For at illustrere kondensationen af hydrazin med en carbonylgruppe, lad os citere reaktionen med acetone, hvilket resulterer i dannelsen af diisopropylidenhydrazin. Dette reagerer igen med hydrazin til dannelse af en hydrazon:
2 (CH 3 ) 2 CO+ N 2 H 4→ 2 H 2 O+ [(CH 3 ) 2 C = N] 2. [(CH 3 ) 2 C = N] 2+ N 2 H 4→ 2 (CH 3 ) 2 C = N - NH 2.Aceton og diisopropylidenhydrazin er mellemprodukter i PCUK-Atofina-syntese. De alkylerings- direkte hydraziner med alkylhalogenider i nærvær af en base form af de alkylerede derivater af hydraziner, men reaktionen er i almindelighed ineffektive på grund af dårlig styring af graden af substitution (som for Aminer fælles). At reducere hydrazon til hydrazin er en elegant måde at producere dialkylerede 1,1 hydraziner på.
I en anden reaktion, 2-cyano pyridin til reagerer med hydrazin danner amiderede hydrazider, der kan omdannes til triaziner under anvendelse af 1,2-diketoner.
Wolff-Kishner-reaktion
Hydrazin anvendes i organisk kemi ved Wolff-Kishner-reduktion , en reaktion, der omdanner carbonylgruppen i en keton eller aldehyd til en methylenbro (eller methylgruppe ) via et hydrazonmolekyle . Produktionen af meget stabil dinitrogen fra hydrazin fremmer reaktionen.
Syntese af polycykliske molekyler
Med to aminfunktioner er hydrazin en nøgledel til fremstilling af mange heterocykliske forbindelser via kondensering med en del, der har to elektrofile funktioner . Med acetylacetone kondenserer den, hvilket giver 3,5-dimethylpyrazol . I Einhorn-Brunner-reaktionen reagerer hydraziner med imider for at give triazoler .
Sulfonering
Bliver en god nukleofil, N 2 H 4 er sårbare for angreb af sulfonylhalogenider og acylhalogenider. Den tosyl hydrazin også danne hydrazoner efter behandling med carbonyler.
Opdeling af ftalimider
Hydrazin bruges til at opdele N- phthalimid i alkylerede derivater. Denne spaltningsreaktion gør det muligt at bruge phthalimidanionen som en aminforløber i Gabriels syntese.
Reduktionsmiddel
Hydrazin er et populært reduktionsmiddel, fordi dets nedbrydningsprodukter normalt er nitrogengas og vand. Det bruges således som en antioxidant , iltfjernende og korrosionsinhibitor i vandet i kedler og varmekredse (i denne rolle foretrækkes nu N, N-diethylhydroxylamin med mindre toksicitet, men det bruges stadig i vid udstrækning mod korrosion i især termiske og atomkraftværker ). Det bruges også til at reducere salte af metaller og metaloxider til metallisk tilstand ved elektrolyse af nikkel såvel som ved ekstraktion af plutonium fra brugt nukleart brændsel .
Hydrazinsalte
Hydrazin omdannes til faste salte ved behandling med mineralsyrer. Den mest almindeligt salt er hydrazin hydrogensulfat, N 2 H 5 HSO 4 , som sandsynligvis bør kaldes hydrazin bisulfat. Hydrazin-bisulfat anvendes som en alternativ behandling for kræftinduceret kakeksi . Saltet af hydrazin og N 5 H 5 azothydric syre var af videnskabelig interesse på grund af dets høje nitrogenindhold og eksplosive egenskaber.
Industrielle anvendelser
Hydrazin anvendes i mange processer, for eksempel produktion af fibre af spandex , som katalysator for polymerisation , opblæsningsmiddel, til brændselsceller , såsom loddestrøm til svejsning , til udvikling af fotografier, såsom forlængerkæde til polymerisering af polyurethan , som en reducerende forbindelse til konditionering af vand i termiske kraftværker og sekundære kredsløb i kernekraftværker og som varmestabilisator. Derudover er en teknik, der anvender hydrazinaflejringer på halvledere, for nylig blevet testet med mulig anvendelse til fremstilling af tyndfilmtransistorer, der anvendes til flydende krystalskærme . Hydrazin i 70% opløsning med 30% vand bruges til at drive EPU (nødkraftenhed) på F-16 ( General Dynamics F-16 Fighting Falcon ) kampfly .
I militær anvendelse er et hydrazinderivat, den asymmetriske dimethylhydrazin (UDMH) kombineret med ammoniumnitrat den grundlæggende ingrediens i astrolit (in) , en eksplosiv ekstremt kraftig opfundet i 1960'erne.
Raketbrændstof
Hydrazin blev først brugt som raketbrændstof i 2. verdenskrig til Messerschmitt Me 163 fly (det første raketplan) under navnet B-Stoff (faktisk hydrazinhydrat ). Denne B-Stoff blev blandet med methanol ( M-Stoff ) til opnåelse af C-Stoff , som blev brugt som brændstof med T-Stoff , et koncentrat af hydrogenperoxid , anvendt som en oxidator i kontakt, med hvilken det antændtes spontant i en meget energisk reaktion.
I dag bruges hydrazin generelt alene som et monopropellant i motorer med lavt tryk (men høj præcision), der tillader positionering i kredsløb om satellitter og rumsonder ; i dette tilfælde tilvejebringes stød ved katalytisk nedbrydning af hydrazin og ikke ved forbrænding. Denne nedbrydning er faktisk en meget eksoterm reaktion . Det opnås ved at føre hydrazinen over en katalysator, hvis aktive komponent er metallisk iridium deponeret på en stor overflade af aluminiumoxid (aluminiumoxid) eller carbon-nanofibre eller for nylig molybdænitrid på aluminiumoxid eller endda molybdænnitrat . Dets nedbrydning i ammoniak , nitrogen og brint skyldes følgende reaktioner:
Denne nedbrydning udløses i nogle få millisekunder og gør det muligt at måle stødet meget præcist. Disse reaktioner er meget eksoterme (katalysatoren i kammeret kan nå 800 ° C på få millisekunder) og producerer et stort volumen varme gasser fra et lille volumen flydende hydrazin, hvilket gør det til et godt drivmiddel til rumfremdrivning .
Visse hydrazinderivater anvendes også som flydende drivmidler : monomethylhydrazin H 2 N - NHCH 3(eller MMH), og asymmetrisk dimethylhydrazin , H 2 N - N (CH 3 ) 2(eller UDMH). De anvendes generelt med nitrogen peroxid N 2 O 4som en oxidant, hvormed de danner et opbevarbart hypergolisk flydende drivmiddel .
Brændstofceller
Den italienske katalysatorproducent Acta har foreslået at bruge hydrazin som en alternativ løsning til brint i brændselsceller . Den største fordel ved dette produkt er dets evne til at producere mere end 200 mW / cm 2 , mere end en tilsvarende hydrogen brændselscelle uden behov for dyre katalysatorer, der indeholder platin . Da brændstof er flydende ved stuetemperatur, kan det håndteres og opbevares lettere end brint. Ved at opbevare hydrazin i en tank indeholdende en carbonyl med en carbon- oxygen- dobbeltbinding reagerer brændstoffet og danner et fast, sikkert materiale kaldet hydrazon . Derefter skal du bare fylde tanken med varmt vand for at frigive hydrazinhydratet i flydende form. Håndteringen af flydende brændstof er i praksis meget sikrere end brintgas, og væsken har et større redoxpotentiale (1,56 V ) sammenlignet med 1,23 V for brint. Hydrazinmolekylet brydes i batteriet for at danne dinitrogen- og hydrogenatomer , der binder til et oxygenatom for at danne vand.
sikkerhed
Toksicitet, økotoksicitet
Hydrazin er meget giftigt og farligt ustabilt, især i sin vandfri form . Det bruges generelt som et stabilt monohydrat .
Symptomer på akut eksponering for høje niveauer af hydrazin kan manifestere sig hos mennesker som irritation af øjne , næse og hals , svimmelhed, hovedpine , kvalme , lungeødem , krampeanfald , koma . Akut eksponering kan også skade leveren , nyrerne og centralnervesystemet hos mennesker. Væsken er ætsende og kan producere kontakteksem hos mennesker og dyr. Skadelige virkninger på lunger , lever, milt og skjoldbruskkirtlen er rapporteret hos dyr, der er kronisk udsat for hydrazin ved indånding. En stigning i antallet af lunge-, næsehule- og levertumorer er observeret hos gnavere udsat for hydrazin.
Dens toksicitet er underlagt periodiske revurderinger, efterhånden som viden udvikler sig.
Referencer
- HYDRAZINE (vandfri) , sikkerhedsark (er) fra det internationale program for kemisk sikkerhed , hørt den 9. maj 2009
- (en) Yitzhak Marcus, The Properties of Solvents , vol. 4, England, John Wiley & Sons Ltd,1999, 239 s. ( ISBN 0-471-98369-1 )
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- (i) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 978-0-387-69002-5 og 0-387-69002-6 , læs online ) , s. 294
- (da) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- Indtastning "Hydrazin" i kemikaliedatabasen GESTIS fra IFA (tysk organ med ansvar for arbejdsmiljø) ( tysk , engelsk ), adgang til 11. februar 2010 (JavaScript krævet)
- " Egenskaber ved forskellige gasser " på flexwareinc.com (adgang til 12. april 2010 )
- (en) "Hydrazine" , på NIST / WebBook , adgang 11. februar 2010
- (i) David R. Lide, Gummibibelen , CRC Press,2009, 90 th ed. , 2804 s. , Indbundet ( ISBN 978-1-4200-9084-0 )
- (i) David R. Lide , Gummibibelen , Boca Raton, CRC Press,18. juni 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online præsentation ) , s. 5-89
- (i) David R. Lide, Handbook of Chemistry and Physics , Boca Raton, CRC,2008, 89 th ed. , 2736 s. ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- IARC-arbejdsgruppen om evaluering af kræftfremkaldende risici for mennesker, “ Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 2B: Eventuelt kræftfremkaldende for mennesker ” , på http://monographs.iarc.fr , IARC,16. januar 2009(adgang til 22. august 2009 )
- Indeksnummer i tabel 3.1 i tillæg VI til EF-regulativ nr. 1272/2008 (16. december 2008)
- SIGMA-ALDRICH
- " Hydrazin " i kemikaliedatabasen Reptox fra CSST (Quebec-organisation med ansvar for sikkerhed og sundhed på arbejdspladsen), adgang til 24. april 2009
- " Hydrazine " på hazmap.nlm.nih.gov (adgang 14. november 2009 )
- “hydrazin” , om ESIS , adgang til 17. februar 2009
- Miessler, Gary L. og Tarr, Donald A. Inorganic Chemistry, tredje udgave . Pearson Prentice Hall (2004). ( ISBN 978-0-13-035471-6 ) .
- Uorganisk kemi, DF Shriver, Peter William Atkins
- Fundamenter for organisk kemi, Michael Hornby, Josephine Peach
- (in) Holleman, AF, Wiberg, E. "Uorganisk kemi" Academic Press: San Diego, 2001. ( ISBN 978-0-12-352651-9 ) .
- INRS sikkerhedsark
- Curtius, Journal für praktische Chemie , 39, 1889, s. 107-39
- Adams, R.; Brown, BK, Hydrazine Sulfate, 1, 309, 1941, cv1p0309
- " Hydrazine: Chemical product info, chemindustry.ru, 2007-01-08 " ( Arkiv • Wikiwix • Archive.is • Google • Hvad skal jeg gøre? ) (Adgang til 25. marts 2013 )
- Riegel, Emil Raymond. "Hydrazine" Riegels håndbog om industriel kemi s. 192 (1992).
- (i) Brian Handwerk , " Bakterier spiser Menneskelig Spildevand, Produce Rocket Fuel " , National Geographic Society ,9. november 2005( læs online , hørt den 12. november 2007 )
- National Geographic http://news.nationalgeographic.com/news/2005/11/1109_051109_rocketfuel.html
- [Day, AC; Hvilling, MC; Acetone Hydrazone; bind 6 | side 10; cv6p0010;]
- [Wiley, RH; Hexner, PE; 3,5-dimethylpyrazol, bind 4, side 351; cv4p0351]
- [Friedman, L; Litle, RL; Reichle, WR; p- toluensulfonylhydrazid; bind 5; side 1055, cv5p1055]
- [Weinshenker, NM; Shen, CM; Wong, JY, Polymer carbodiimid; bind 6, side 951; (1988); cv6p0951]
- 2013 Atomanlæg spilder kemikalier i Bay of Fundy New Brunswick atomkraftværk rapporterer kemisk lækage i Bay of Fundy (Canadian Press in Energy and Resources ) 3013-11-05, adgang 3013-11-06
- (en) R. Vieira , ” New carbon nanofiber / grafitfilt komposit til anvendelse som en katalysator støtte til hydrazin katalytisk nedbrydning ” , Chemical Communications , n o 9,2002, s. 954—955 ( DOI 10.1039 / b202032g )
- (da) Xiaowei Chen , " Katalytisk nedbrydning af hydrazin over understøttede molybdænitridkatalysatorer i en monopropellant thruster " , Catalysis Letters , bind. 79,April 2002, s. 21-25 ( DOI 10.1023 / A: 1015343922044 )
- " Flydende aktiver - Nyheder - Ingeniøren - Nyheder: ingeniørnyheder, ingeniørinformation, nyeste teknologi, produktionsnyheder, produktionsinfo, bilnyheder , luftfartsnyheder, materialenyheder, forskning og udvikling " ( Arkiv • Wikiwix • Archive.is • Google • Hvad skal jeg gøre? )
- ARC, monografi, bind 71 (1999) Revaluering af nogle organiske kemikalier, hydrazin og hydrogenperoxid .
- Sylvie Tissot, Annick Pichard, " Akutte toksicitetstærskler hydrazin (NH 2 NH 2 ) - Endelig rapport " [PDF] , på ineris.fr , National Institute for the industrial environment and risks ,august 2003(adgang til 29. oktober 2015 ) .
Relaterede artikler
eksterne links
- The Late Show med Rob! Aftens særlige gæst: Hydrazin (PDF) - Robert Matunas
- xMSDS-Hydrazine-9924279 (PDF) - MSDS for hydrazin
- (fr) INRS toksikologisk ark
- (en) International sikkerhedsdatablad








