Bicarbonat
| Bicarbonat | |
 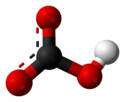 Struktur af bicarbonat -ion . |
|
| Identifikation | |
|---|---|
| IUPAC navn | hydrogencarbonat |
| N o CAS | |
| PubChem | 769 |
| ChEBI | 17544 |
| SMILE |
C (= O) (O) [O-] , |
| InChI |
Std. InChI: InChI = 1S / CH2O3 / c2-1 (3) 4 / h (H2,2,3,4) / p-1 Std. InChIKey: BVKZGUZCCUSVTD-UHFFFAOYSA-M |
| Kemiske egenskaber | |
| Brute formel | HCO 3 |
| Molar masse | 61,0168 ± 0,0018 g / mol C 19,68%, H 1,65%, O 78,66%, |
| Enheder af SI og STP, medmindre andet er angivet. | |
Den bicarbonat eller hydrogen , er en polyatomisk ion hvis kemiske formel er H C O 3 - . Bicarbonat skylder sit præfiks (“bi-”) til sin dobbelte syrebasekarakter (kaldet amfoterisk karakter ): det er både syre og base og tilhører to forskellige syre-basepar. Dette er den mellemliggende form i dobbelt deprotonering af kulsyre : fjernelse af den første proton ( H + ion ) af kulsyre giver bicarbonat; fjernelse af den anden proton giver formularenionisk carbonat .
Ordet er skrevet i flertal (bicarbonater), når det kommer til salte af bicarbonationen: for eksempel natriumbicarbonat (ofte kaldet "bagepulver" ved sprogbrug eller "bagepulver" og "lille ko" i Canada ) med formlen NaHCO 3 , som er den mest almindelige og udbredte salt af bicarbonation. Det bidrager til fordøjelsen af vores krop.
Ejendomme
I vand er kuldioxid , kulsyre , bicarbonation og carbonation i ligevægt , afhængigt af pH :
CO 2+ H 2 O H 2 CO 3 H + + HCO 3 - 2 H + + CO 3 2–.Tilsætningen af en syre skifter ligevægten til venstre (med mulig frigivelse af kuldioxid), mens tilsætningen af en base skifter dem til højre (med eventuelt udfældning af et carbonatsalt.).
Ansøgninger
Den delvise transformation af bicarbonater i kontakt med syrer (såsom eddikesyre fra eddike ) i carbondioxid gas anvendes i bagning at muliggøre brød til stige, og når fremdrift af raketter legetøj.
Humanbiologi
Standard
Bicarbonat koncentration i blodet er mellem 22 og 26 mmol / l .
Bufferopløsning
Den amfotere natur af bicarbonat (dets mellemliggende sted i ligevægten) får det til at spille en bufferrolle . Denne bicarbonatbufferfunktion findes især i blodet med en meget vigtig rolle i opretholdelsen af pH (jf. Homeostase ).
Mange organer er involveret i reguleringen af niveauet af bicarbonater og derfor af pH: hovedsageligt lungerne (gennem eliminering af kuldioxid ) og nyrerne . Fordøjelsessystemet er også involveret gennem udskillelse af sur mavesaft (under kontrol af secretin ) og galdesalte produceret af leveren og udskilt i galden .
Aktivering af fordøjelsesenzymer
Den eksokrine funktion af bugspytkirtlen producerer via kulsyreanhydraser bicarbonat HCO 3- ioner - som udledes i tolvfingertarmen for at neutralisere surhedsgraden i kymet og således aktivere tarmens enzymer og bugspytkirtlenzymer produceret af denne samme funktion.
Andre funktioner
Bicarbonat anvendes til syntesen af uracilmonophosphat (UMP), en forløber for pyrimidinbaser i DNA .
Det er også involveret i kapacitering af sædceller under befrugtning.
Noter og referencer
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- Webmaster Cuen, “ Komplet kapitel. Syre-base balanceforstyrrelser - [nefrologihåndbog nr. 7] ” , på cuen.fr (konsulteret 2. december 2018 ) .
