Carbondioxid
| Carbondioxid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Struktur af kuldioxid. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikation | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC navn | Carbondioxid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
Kuldioxid, kuldioxid |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.004.271 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EF | 204-696-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-kode | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 280 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 16526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E290 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMIL |
C (= O) = O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / CO2 / c2-1-3 InChIKey: CURLTUGMZLYLDI-UHFFFAOYSA-N |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Udseende | Flydende, farveløs og lugtfri komprimeret gas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formel |
C O 2 [isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar masse | 44,0095 ± 0,0014 g / mol C 27,29%, O 72,71%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusion | −78,48 ° C (sublimering ved 760 mmHg ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kogning | −56,6 ° C ( 5,12 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighed | i vand ved 20 ° C : 88 ml / 100 ml under 1 bar CO 21,69 g / kg vand (3,35 g ved 0 ° C , 0,973 g ved 40 ° C og 0,576 g ved 60 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumenmasse |
1,87 kg m −3 ( gas ved 15 ° C 1,013 bar ) tættere end luft ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mættende damptryk |
5,720 kPa ( 20 ° C ) 569,1 mmHg ( -82 ° C ); ligning:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynamisk viskositet | 0,07 mPa s ved -78 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | 31,3 ° C ; 72,9 atm og 0,464 g cm −3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Triple point | -56,6 ° C til 5,11 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varmeledningsevne | 3.840 × 10 −5 cal cm −1 s −1 K −1 ved 20 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lydens hastighed | 259 m s −1 ( 0 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | −393,52 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
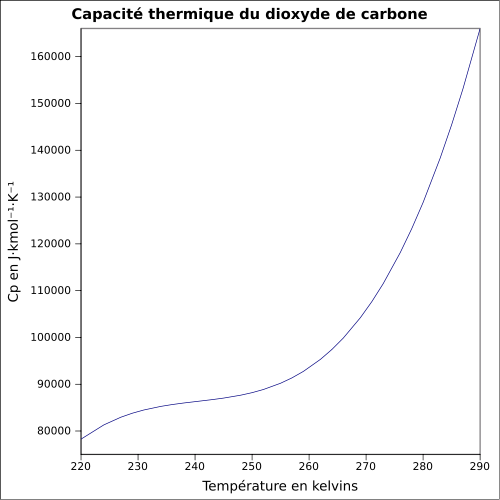
| C s |
ligning:
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionisering energi | 13,773 ± 0,002 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystallografi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalklasse eller rumgruppe | P42 / mnm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mesh-parametre |
a = 3,535 Å b = 3,535 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bind | 51,73 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brydningsindeks | 1.00045 (1 atm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Advarsel H280 , P403 og P410 H280 : Indeholder gas under tryk; kan eksplodere ved opvarmning P403 : Opbevares på et godt ventileret sted. P410 : Beskyt mod sollys. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 TIL, A : Kritisk komprimeret gaskritisk temperatur = 31,1 ° C Oplysning ved 1,0% i henhold til listen over ingredienser |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : kvælende gas eller gas, der ikke udgør en subsidiær risiko UN -nummer : 1013 : CARBON DIOXIDE Klasse: 2.2 Klassificeringskode: 2A : Flydende gas, kvælende; Mærkning: 2.2 : Ikke-brændbare, ikke-giftige gasser (svarer til de grupper, der er angivet med A eller stort O); 
22 : nedkølet flydende gas, kvælende UN -nummer : 2187 : KØLESKÆLENDE CARBON DIOXIDE Klasse: 2.2 Klassificeringskode: 3A : Kølet flydende gas, kvælende; Mærkning: 2.2 : Ikke-brændbare, ikke-giftige gasser (svarer til de grupper, der er angivet med A eller stort O); 
- UN-nummer : 1845 : KULDIOXID, FAST; eller CARBON SNOW Klasse: 9 Klassificeringskode: M11 : Andre stoffer, der udgør en risiko under transport, men som ikke opfylder definitionen af nogen anden klasse. Tag: 9 : Diverse farlige stoffer og genstande  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheder af SI og STP, medmindre andet er angivet. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den kuldioxid , også kendt som kuldioxid eller kuldioxid er en uorganisk forbindelse , hvis kemiske formel er CO 2The molekyle har en lineær struktur af formen O = C = O . Det præsenteres under standardbetingelserne for temperatur og tryk , såsom en gas farveløs, lugtfri, tang.
CO 2bruges af anabolismen af planter til at producere biomasse gennem fotosyntese , en proces, der består i at reducere kuldioxid med vand takket være den lysenergi, der modtages fra solen og fanget af klorofyl , ved at frigøre iltet til at producere monosaccharider , og først af glucose ved Calvin-cyklussen . CO 2frigives gennem Krebs -cyklussen ved katabolisme af planter , dyr , svampe (svampe eller svampe ) og mikroorganismer . Denne katabolisme er særligt oxidere den lipider og kulhydrater vand og kuldioxid med oxygen af luft til at generere strøm og reduktionsevne, henholdsvis i form af ATP og NADH + H + . CO 2er derfor en grundlæggende del af kulstofcyklussen på vores planet. Det produceres også ved forbrænding af fossile brændstoffer som kul , naturgas og olie samt ved al organisk materiale generelt. Det er et uønsket biprodukt i store industrielle processer.
Betydelige mængder CO 2afvises også af vulkaner og andre geotermiske fænomener som gejsere .
I januar 2021 indeholdt Jordens atmosfære 415,13 ppmv (dele pr. Million i volumen) CO 2eller 0,04153%. Dette niveau var 283,4 ppmv i 1839 ifølge iskerner taget fra Antarktis , en samlet stigning på ca. 46% i 182 år.
CO 2er en vigtig drivhusgas , gennemsigtig i synligt lys, men absorberer i det infrarøde område , så den har en tendens til at blokere genemissionen til rummet af termisk energi modtaget på jorden under påvirkning af solstråling . Det er ansvarligt for omkring 26% af drivhuseffekten ved arbejde i jordens atmosfære ( vanddamp giver 60%); øge sin koncentration er delvis ansvarlig for den opvarmning observeret på tværs af kloden i løbet af de sidste årtier af det XX th århundrede. Desuden forsuring kunne følge af opløsningen af atmosfærisk kuldioxid true overlevelsen af mange marine organismer inden udgangen af XXI th århundrede.
Fysisk -kemiske egenskaber
Ved atmosfærisk tryk sublimerer det ved -78,5 ° C (skifter fra fast til gasform), men smelter ikke (skifter fra fast til flydende tilstand).
Væskefasen kan kun eksistere ved et minimumstryk på 519 kPa ( dvs. 5,12 atm ) og i et temperaturinterval fra -56,6 ° C ( tredobbelt punkt ) til et maksimum på 31,1 ° C ved 7,38 MPa ( dvs. 72,8 atm ) ( kritisk punkt ).
Mættende damptryk
|
| Overgang | Temperatur | Latent varme |
|---|---|---|
| Fordampning | 0 ° C | 234,5 kJ kg −1 |
| Fordampning | −16,7 ° C | 276,8 kJ kg −1 |
| Fordampning | −28,9 ° C | 301,7 kJ kg −1 |
| Fusion | −56,6 ° C | 199 kJ kg −1 |
Der ville være mindst fem faste molekylære faser (eksisterende ved "lavt" tryk, mindre end 30 til 60 GPa) og tre faste polymerfaser (ved højere tryk) af C02 . :
- molekylære faser:
- I: “tøris”, op til 800 K og 11-12 GPa
- II: mellem 400 og 5-600 K og et tryk på 12 til ca. 50 GPa
- III: ud over 12 GPA og mindre end 500 K
- IV: ud over 11 GPa og mere end 500 K
- VII: fra 600 til 900 K (op til 1000 K inklusive den superkritiske del) og 11 til 20 GPa
- polymere faser:
- V: over 30 GPa og over cirka 1.300 K
- VI: temperatur mellem ca. 500 K og 1300 K og tryk større end 30 (ved 1300 K) ved 50 GPa (ved 500 K)
- amorf, mindre end 500 K og mere end 50 GPa
Vandig opløselighed
CO 2opløses i vand og danner kulsyre H 2 CO 3 : CO 2 (aq)+ H 2 O (l) H 2 CO 3 (aq), med K h = [H 2 CO 3] / [CO 2] ≈ 1,70 × 10 -3 til 25 ° C .
Det er også liposoluble (opløseligt i fede stoffer).
Kulsyre er kun moderat stabilt og det let nedbrydes til H 2 Oog CO 2. På den anden side, når kuldioxid opløses i en basisk vandig opløsning (sodavand, kalium, etc.), deprotonerer basen kolsyre til dannelse af en hydrogencarbonation HCO-
3, også kaldet bicarbonation , derefter en carbonation CO2-
3. På denne måde er opløseligheden af CO 2øges betydeligt. Den kaliumcarbonat K 2 CO 3for eksempel har en opløselighed på 1,12 kg / l vand ved 20 ° C .
Sådan opløses kalksten i vand i det pH- område , hvor syrehydrogencarbonatet er stabilt, hvorved der dannes en opløsning af hydrogencarbonat (er) (af calcium og magnesium ...). Det vil derfor sandsynligvis udfældes, når CO 2opløst afgasses, som ved dannelsen af stalagmitter og stalaktitter . Kalksten har således i nærvær af CO 2en opløselighed, der falder med stigende temperatur, ligesom gasser og i modsætning til de fleste faste stoffer (hvis opløselighed generelt stiger med temperaturen).
Under visse betingelser (højt tryk + lav temperatur) CO 2kan blive fanget i såkaldte clathrate -vandbure . Det er et af de mulige midler til industriel adskillelse af CO 2indeholdt i en for- eller efterforbrændingsgas . Det er også et af de planlagte midler til CO 2 -bindingindustriel eller geologisk lagring undersøgt, muligvis korreleret med afsaltning af havvand (teoretisk set kan det endda erstatte metanhydrat methan ).
Videnshistorie
Kuldioxid er en af de første gasser (sammen med vanddamp ), der beskrives som et stof, der adskiller sig fra luft. I XVII th århundrede , kemikeren og lægen Flemish Jan Baptist van Helmont observeret, at brændende kul i en lukket beholder, massen af den dannede aske er lavere end den for kul. Hans fortolkning var, at den manglende masse var transmitteret til et usynligt stof, som han kaldte " gas " eller spiritus sylvestre ("vild ånd").
Kuldioxidets egenskaber blev undersøgt mere detaljeret i 1750'erne af den skotske kemiker og fysiker Joseph Black . Han opdagede, at ved opvarmning eller ved at hælde en syre på kalksten (sten sammensat af calciumcarbonat ) var resultatet emissionen af en gas, som han kaldte "fast luft", hvilket underminerede teorien om phlogiston. Stadig undervist på det tidspunkt. Han observerede, at den er tættere end luft, og at den hverken kan understøtte en flamme eller et dyrs liv. Sort opdagede også, at når kuldioxid indføres i en kalkstenopløsning ( calciumhydroxid ), dannes et bundfald af calciumcarbonat. Han brugte dette fænomen til at illustrere, at kuldioxid produceres ved animalsk respiration og mikrobiel gæring.
I 1772 offentliggjorde den engelske kemiker Joseph Priestley et værk med titlen Impregnering Water with Fixed Air , hvor han beskrev en proces med at hælde svovlsyre (eller "olie af vitriol", som det blev kaldt på det tidspunkt) på kridt for at producere kulstof. dioxid og derefter tvinge gassen til at opløses i en skål med vand. Han havde netop "opfundet" mousserende vand . Processen blev derefter overtaget af Johann Jacob Schweppe, der i 1790 i London grundlagde et sodaproduktionsanlæg kendt som Schweppes .
I 1781 fremhævede den franske kemiker Antoine Lavoisier det faktum, at denne gas er et produkt af forbrænding af kulstof med ilt .
Kuldioxid blev først flydende i 1823 af Humphry Davy og Michael Faraday . Den første beskrivelse af kuldioxiden i den faste fase blev skrevet af Charles Thilorier (fr) , som i 1834 åbnede en beholder med flydende kuldioxidgas under tryk og fandt ud af, at den afkøling, der blev frembragt ved den hurtige fordampning af væsken, der blev genereret i "sneen "CO 2.
Anvendelser
Kuldioxid markedsføres i forskellige former til forskellige anvendelser på et marked domineret af store virksomheder som Messer , Air Liquide og Air Products . For fødevareindustrien er benchmarkstandarden i Europa offentliggjort af European Industrial Gases Association (de ). I Frankrig udgør det 70% af forbruget.
Det Internationale Energiagentur offentliggjorde en rapport om anvendelsen af CO 2 i september 2019, som han anslår til 230 Mt / år , inklusive 130 Mt / år til fremstilling af gødning og 80 Mt / år til forbedret genvinding af olie og naturgas. Formålet med denne rapport er at vurdere deres potentiale til at bidrage til udligning af CO 2 -emissioner.. Han konkluderer, at dette potentiale er lavt på kort sigt og vil forblive på lang sigt meget lavere end potentialet for opsamling og opsamling af kuldioxid ; de mest lovende veje er anvendelserne i byggematerialer, til fremstilling af polymerer og i drivhuse.
I gasform
CO 2 har mange anvendelser, herunder:
- slukning af brande : mange datacentre (computerserverrum) eller arkivrum er udstyret med et system, der i tilfælde af brand fylder rummet med CO 2 som har den virkning, at ilden slukkes;
- mousserende komponent i kulsyreholdige drikkevarer ;
- i akvarier og drivhusdyrkning for bedre plantevækst
- i kontrolleret atmosfære emballage som et neutraliserende element;
- ved distribution af drikkevand, associeret med karbonat, for at hæve vandhårdheden (TH) af alt for aggressivt vand;
- opløseliggørelse af kalksten i hårdt vand (TH større end 25 ° F );
- ølpumper: ved at være i kontakt med øloverfladen forhindrer den dets oxidation og forlænger dens konservering i modsætning til en kompressor, der bruger (omgivende) luft;
- CO 2 bruges også nogle gangei store svineslagterier for at bedøve dem, før de blødes; det blev brugt til konservering af kød ;
- komponent, der er nødvendig for fænomenet fotosyntese, som gør det muligt for planter at vokse ved at omdanne uorganisk stof til organisk materiale og dermed udgøre deres træ;
- varmeoverføringsvæske i visse typer atomreaktorer såsom dem fra UNGG- sektoren i Frankrig
- det bruges af dets diffusibilitet (evne til at diffundere) til dannelsen af pneumoperitoneum under laparoskopier .
I flydende form
I flydende form bruges det som:
- kølemiddel til frysning af visse fødevarer;
- kølemiddel i elektronikindustrien;
- slukningsmiddel i såkaldte "kuldioxid" slukkere , taler vi nogle gange om kuldioxid sne, fordi en del af CO 2 væske størkner straks efter udgang til ildslukkeren og frembringer et hvidt pulver blandet med kuldioxidgas
- drivmiddel (og nogle gange også kulsyreholdig) til drikkevarer, der serveres på fad.
Når det bruges som kølemiddel , CO 2bærer det industrielle nomenklaturnavn "R744". Dets anvendelse som kølemiddel har haft en tendens til at blive mere demokratisk i de senere år: det anses for at være "naturligt kølemiddel", og dets globale opvarmningspotentiale er meget lavt sammenlignet med "traditionelle" kølemidler.
Ved atmosfærisk tryk er kuldioxid aldrig i flydende form. Det går direkte fra fast form til gasform ( sublimering ).
I fast form
Kuldioxid i fast form har mange navne: "tøris", "tøris", "tøris", "tøris". Det kommer fra størkning af CO 2væske. Der opnås tøris, som derefter komprimeres for at opnå tøris.
I sin faste fase sublimerer denne tøris ingen rester med en sublimeringsenthalpi på 573 kJ kg −1 (eller 25,2 kJ mol −1 ) ved −78,5 ° C og 1 atm . Det blev derfor hurtigt fundet flere anvendelser som kølemiddel.
Det markedsføres i forskellige præsentationer afhængigt af dets anvendelse:
- i granuler (størrelsen af et riskorn 3 mm i diameter): hovedsageligt til rengøring og kryogen stripping ;
- i pinde (ca. 16 mm lange ):
- til bevarelse og transport af produkter under kontrolleret temperatur (farmaceutiske produkter, transport af frosne fødevarer, transport af prøver osv.),
- i tilfælde: tørisen i vandet danner en meget tæt tåge, der glider langs beholderens vægge;
- til grundlæggende eller anvendt forskning, for eksempel:
- i kemi, som et kølemiddel blandet med et organisk opløsningsmiddel (oftest acetone ) for at lede varme bedre, sjældnere som et reagens. I dette felt bruger vi udtrykket "Carboglace" i Frankrig eller bare "carbo" på det talte sprog, og aldrig udtrykket "tøris", der på den anden side foretrækkes i Quebec;
- til vinifikation : det bremser gæring og forhindrer oxidation ;
- i blærer eller blokke:
- til lufttilførsel ( catering ), cateringfirmaer, begravelsesdirektører osv. ;
- i brød:
- at lave tyk tåge (specialeffekter, biograf, video).
Fast kuldioxid er også til stede i form af kuldioxid sne på polerne på planeten Mars , hvor det dækker iskapperne (hovedsageligt sammensat af vand) og deres periferier i løbet af den lokale vinter såvel som i form af kuldioxid is. ved lavere breddegrad, sen aften i tidlige lokale kilder (fotografier taget af vikingelandere , Sojourner- roveren , Phoenix- landeren og adskillige HRSC- billeder ). Vigtige aflejringer sekventeres geologisk ved sydpolen.
I superkritisk fase
Ud over det kritiske punkt går kuldioxid ind i en fase kaldet superkritisk . Væske-gas-ligevægtskurven afbrydes på det kritiske punkt, hvilket sikrer den superkritiske fase et kontinuum af fysisk-kemiske egenskaber uden faseændring. Det er en fase så tæt som en væske, men sikrer transportegenskaber (viskositet, diffusion) tæt på en gas. Superkritisk kuldioxid anvendes som et grønt opløsningsmiddel, hvor ekstrakterne er fri for spor af opløsningsmiddel.
I denne form fungerer det som:
- agent ekstraktion :
- Fjernelse af koffein i kaffe ,
- eliminering af 2,4,6-trichloroanisol (TCA) fra korkpropper behandlet med klor (eller hypochlorit) for at undgå at give vinen en korket smag efter aftapning
- ekstraktion af kemiske eller biologiske forbindelser
- oprensning af kemiske forbindelser (mobil fase ved kromatografi , især i SFC );
- transport- og opbevaringsmiddel i den geologiske opsamling af kuldioxid (i sjældne industrielle anvendelser);
- kølemiddel for at tillade mikronisering af aktive ingredienser .
Biprodukt fra industrielle processer
Det er et biprodukt af store industrielle processer. Et eksempel er produktionen af acrylsyre, der produceres i en mængde på over fem millioner tons om året. Udfordringen ved at udvikle disse processer er at finde en passende katalysator og procesbetingelser, der maksimerer produktdannelse og minimerer CO 2 -produktion..
Reaktivitet
Kuldioxid er et meget stabilt molekyle med en standard-entalpi af dannelse på -393,52 kJ mol -1 . Kulstof har en positiv delladning, hvilket gør molekylet svagt elektrofilt . For eksempel vil en carbanion være i stand til at udføre en nukleofil tilsætning på CO 2og dannelse af en carboxylsyre efter hydrolyse. Derudover CO 2kan bruges til at danne organiske carbonater ved tilsætning til epoxy .
Endelig CO 2kan reduceres for eksempel til kulilte ved elektrokemi med et redoxpotentiale på -0,53 V sammenlignet med standardbrintelektroden eller ved hydrogenering .
Toksicitet
Udeluften indeholder omkring 0,04% CO 2 i 2019 (412 ppm i januar 2019).
Fra en bestemt koncentration i luften er denne gas farlig eller endda dødelig på grund af risikoen for kvælning eller acidose , skønt CO 2er ikke kemisk giftig. Eksponeringsgrænseværdien er 3% over en periode på femten minutter. Denne værdi bør aldrig overskrides. Udover det er sundhedseffekterne desto mere alvorlige som CO 2 -indholdetøget. Således ved 2% CO 2i luften øges respirationsamplituden. Ved 4% (eller 100 gange den nuværende koncentration i atmosfæren) accelereres respirationsfrekvensen. Ved 10%kan der forekomme synsforstyrrelser, rysten og svedtendens. Med 15%er det pludseligt tab af bevidsthed . Ved 25%resulterer åndedrætsstop i dødsfald.
Indånding af koncentreret kuldioxid forårsager blokering af ventilation, undertiden beskrevet som en voldsom følelse af kvælning, åndenød, åndedrætsbesvær eller tæthed i brystet , som hurtigt kan føre til døden, hvis eksponeringen forlænges.
Ifølge ANSES rapporterer undersøgelser "koncentrationer forbundet med iboende sundhedsmæssige virkninger af CO 2(tærskel på omkring 10.000 ppm svarende til udseendet af respiratorisk acidose (fald i blodets pH), den første kritiske effekt af CO 2) ” . Respiratorisk acidose kan forekomme så lavt som 1% (10.000 ppm ) CO 2i luften, hvis den åndes i tredive minutter eller mere af en sund voksen med moderat fysisk belastning og muligvis tidligere hos sårbare eller følsomme individer. Disse satser “er højere end de regulatoriske og / eller normative grænseværdier for luftfornyelseskvalitet i Frankrig og internationalt, som normalt varierer mellem 1.000 og 1.500 ppm CO 2. ". En lille eksperimentel undersøgelse (med 22 voksne) konkluderede, at CO 2 havde en effektom psykomotricitet og intellektuel funktion (beslutningstagning, problemløsning) fra 1000 ppm (undersøgelse af Satish et al. , 2012), men denne undersøgelse skal bekræftes af undersøgelser med en højere statistisk styrke. ANSES bemærker, at der i sidste ende er få epidemiologiske undersøgelser af denne almindelige gas, herunder mulige CMR-effekter (kræftfremkaldende, mutagene og reprotoksiske).
Kuldioxid er en farveløs og tung gas, der akkumuleres i plader, og det er vanskeligt at opdage af en uerfaren person.
I indeluft
Mennesker bruger mere og mere tid i en begrænset atmosfære (ca. 80-90% af tiden i en bygning eller et køretøj). Ifølge ANSES og forskellige aktører i Frankrig er CO 2 -satseni indendørs luft i bygninger (knyttet til menneskers eller dyrs belægning og tilstedeværelsen af forbrændingsanlæg ), vægtet ved luftfornyelse, er "normalt mellem 350 og 2500 ppm ca." .
I hjem, skoler, planteskoler og kontorer er der ingen systematisk sammenhæng mellem CO 2 -niveauerog andre forurenende stoffer og CO 2indendørs er statistisk set ikke en god forudsigelse for forurenende stoffer forbundet med udendørs vej (eller lufttrafik). CO 2er den parameter, der ændrer sig hurtigst (med hygrometri og iltmængde, når mennesker eller dyr samles i et lukket eller dårligt ventileret rum. I fattige lande er mange åbne ildsteder kilder til CO 2og CO udsendes direkte på livsstedet. Eller bliv hele dagen i luften med en CO 2 -satsnår eller overstiger 600 ppm nedbrydes vores kognitive evner (tænkning, ræsonnement, huskelse, beslutning). Små ændringer i CO 2 -niveauer ifølge en undersøgelse offentliggjort i Environmental Health Perspectivesi luften påvirker stærkt vores komplekse tænkning og beslutningsevne. Dette niveau på 600 ppm nås ofte i indeluft, hvor det ofte overstiger 1000 ppm flere gange om dagen med for eksempel et gennemsnitligt indhold på 3110 mg / m 3 CO 2i de studerede klasseværelser; til skade for børns indlæringsevner).
Et specielt tilfælde er sportshaller, hvor fysisk indsats indebærer et yderligere behov for ilt og en stigning i CO 2.udløbet af spillere (og tilskuere). For eksempel under ishockeyspil , CO 2stiger fra 92 til 262 ppm under et spil (mest spillet af voksne mænd). I midten af skøjtebanen er CO 2 -niveauetoverstiger 1000 ppm i hver kamp (maksimal tærskel anbefalet af det norske institut for folkesundhed). In situ målinger viser, at en spiller ånder luft mere beriget med CO 2at tilskuerne, og at CO 2falder ned i hviletider og stiger i løbet af spilletiden. Den nat efter et spil, i en lukket hockey hal, det tager næsten en halv snes timer at genvinde et niveau af CO 2lav (600-700 ppm ), hvilket stadig er over det normale. Derudover er der i kolde, tempererede eller varme lande mange sportshaller med aircondition. af energibesparelser har de ikke en konstant eller tilstrækkelig fornyelse af udeluften. Under et ishockeyspil udsender kvinder og børn mindre CO 2end mænd, men i samme rum, graden af stigning i niveauet af CO 2i luften i sportshallen er sammenlignelig, og i alle de undersøgte tilfælde reducerer bruddet mellem to kampe ikke koncentrationen af CO 2nok, så starten på den anden periode er lige så svag som starten på den første. Når antallet af tilskuere stiger, niveauet af CO 2i rummet stiger endnu mere. Antallet af åbninger / lukninger af døre, der fører udad, påvirker også fornyelsen af luft og dermed CO 2 -hastigheden.i gymnastiksalen. Undersøgelser har vist et fald i kognitiv præstation og i beslutningstagning eller læring, når CO 2øget. Få undersøgelser har fokuseret på effekten af den samme CO 2 på sportspræstationen for en person eller hans hold.
I boligerneDet er ikke reguleret i hjemmeluften; men det skal måles som en "indikator for indeslutning og for kvaliteten af luftfornyelse" på bestemte lukkede steder på grundlag af standarder, som ANSES mener ikke har noget sanitært grundlag.
I ikke-beboelsesbygningerI Frankrig anbefaler departementets sundhedsbestemmelser (RSD) ikke at overskride tærsklen på 1000 ppm (del pr. Million) "under normale belægningsforhold" med en tolerance på 1300 ppm på steder, hvor det er forbudt. Rygning ( "uden en eksplicit sundhedsgrundlag for disse to værdier " ifølge ANSES.
Et dekret af 5. januar 2012pålægger overvågning af indeluftkvaliteten i visse virksomheder, der modtager følsom offentlighed, f.eks. børn; den foreslår beregning af et "indeslutningsindeks" kaldet "Icone-indeks" (foreslået af det videnskabelige og tekniske center for bygning (CSTB) på basis af hyppigheden af at overskride CO 2 -niveauerne.sammenlignet med to tærskler på 1000 og 1700 ppm i klasseværelserne .
På arbejdspladsen er spørgsmålet om sikkerhed og forebyggelse forbundet med risikoen for kuldioxidforgiftning et stort problem for at begrænse risikoen for arbejdsulykker . På grund af mangel på epidemiologiske data blev det dog ikke anset for relevant i Frankrig som en indikator for den sanitære kvalitet af indeluften af ANSES, som ikke giver en vejledende værdi for indeluftkvaliteten (IGAI) til dette.
I høje koncentrationer, der nærmer sig 50 til 100%, f.eks. Dem, der findes i menneskeskabte kuldioxidplader på arbejdspladsen, kan der være en effekt af nervøs forbløffelse og øjeblikkeligt tab af bevidsthed , efterfulgt af hurtig død uden fravær fra hjælp. Disse ulykker udgør en høj risiko for en anden ulykke , da vidner kan skynde sig til ofrets hjælp uden at tænke over deres egen sikkerhed og også blive ofre for rus.
CO 2 i jordens atmosfære
Kuldioxid er normalt kun til stede i jordens atmosfære i spormængder. Det måles via et indeks , kaldet ” Årligt drivhusgasindeks ” (AGGI) siden 1979 af et netværk på omkring hundrede stationer på land og til søs, der ligger fra Arktis til Sydpolen.
Siden den industrielle revolution , på grund af den konstante forbrænding af meget store mængder fossilt kulstof , mens faldet i brande , skove og vegeterede områder er fortsat, har CO 2 -hastighedeni luften stiger regelmæssigt (i januar 2021: 415,13 ppm i volumen, eller også 632,96 ppm i masse. Dette svarer til en samlet masse af CO 2atmosfærisk på ca. 3,258 × 10 15 kg (ca. tre tusind gigaton ) . Dette indhold var 283,4 ppmv i 1839 fra iskernerne taget fra regionen Poinsett cap i Antarktis , en samlet stigning på ca. 42% i 177 år. CO 2 satsenatmosfærisk forventes i slutningen af XXI th århundrede anslås til mellem 540 og 970 ppmv af udvalgte simuleringer (ISAM model og Bern-CC model). Året 1990 (hvilket svarer til et overskud på ca. 2,1 W / m 2 sammenlignet med 1980 ) er referenceåret, der blev brugt til Kyoto-protokollen (det har derfor et ”AGGI-indeks” på 1). Der er nedsat en specifik forskningsgruppe om kulstofcyklus og drivhusgasser.
På tidspunktet t , CO 2 -indholdetadskiller sig på hver halvkugle med regelmæssige sæsonvariationer på hver halvkugle (jf. “savtand” mønster på grafen til højre, der viser et fald i CO 2i sæsonen af vegetation og en stigning om vinteren). Der er også regionale variationer, især på niveauet med det atmosfæriske grænselag , det vil sige i lagene tæt på jorden.
CO 2 niveauer er generelt højere i byområder og i boliger (op til ti gange baggrundsniveauet).
Kort tid efter jordens dannelse (længe før livets udseende), da solen var næsten halvt så “varm”, begyndte CO 2 -trykketvar ca. 100.000 gange højere end i dag (30 til 60 atmosfærer CO 2( dvs. 3.000.000 til 6.000.000 pascal), dvs. 100.000 gange den nuværende mængde CO 2 for omkring 4,5 milliarder år siden).
Derefter optrådte liv og fotosyntese under CO 2af atmosfæren og vandet for at omdanne det til carbonatsten og kul, olie og naturgas, meget af det begravet dybt i jordens dybder. CO 2 satsenhar alligevel stadig oplevet nogle toppe af meget mindre betydning (tyve gange højere end i dag for omkring en halv milliard år siden, men solen var da mindre varm end i dag (solstråling øges med tiden og er steget med ca. 40% i de sidste fire milliarder år) CO 2faldt yderligere fire-fem gange under juraen og faldt derefter langsomt, undtagen på en accelereret måde under en geologisk kort episode, kendt som " Azolla-begivenheden " (for omkring 49 millioner år siden).
Vulkanisme udsender også CO 2(op til 40% af de gasser, som visse vulkaner udsender under subaerielle udbrud, er kuldioxid) og visse varme kilder udsender det også (for eksempel på det italienske sted Bossoleto nær Rapolano Terme, hvor der i en fordybning i form af et bassin var omkring 100 m i diameter, på en rolig nat, CO 2kan klatre 75% på få timer, nok til at dræbe insekter og små dyr. Men gasmassen opvarmes hurtigt, når stedet er solrigt og spredes derefter af luftens konvektionsstrømme i løbet af dagen. Lokalt høje koncentrationer af CO 2, produceret af forstyrrelse af vandet i en dyb sø mættet med CO 2kan også dræbe (eksempel: 37 dødsfald under et CO 2 -udbrudfra Monoun-søen i Cameroun i 1984 og 1.700 ofre omkring Nyos-søen (også Cameroun) i 1986.
CO 2 -emissioneraf menneskelige aktiviteter er i øjeblikket mere end 130 gange større end den mængde, der udledes af vulkaner, og beløber sig til næsten 27 milliarder ton om året i 2007. I 2012 var Kina verdens førende udledning af kuldioxid med 27% af det samlede antal og De Forenede Stater Stater producerer på andenpladsen 14% af verdens samlede. I 2016 rapporterer FNs meteorologiske agentur, at koncentrationen af kuldioxid nåede en ny heltidshøjde på 403,3 ppm , og en temperaturrekord blev brudt for El Niño 2017 ifølge OMM, mens den med 405 ppm , CO 2 luft har aldrig været så høj i omkring 800.000 år.
Globale CO 2 -emissionersteg med 2,7% i 2018, den største stigning i syv år. I en rapport fra 2019, CO 2 -koncentrationernåede 407,8 ppm i 2018, et fund korrelerede også med stigningen i metankoncentrationer (CH 4) Og lattergas (N 2 O).
Plantenæringsstof
Et højere niveau af CO 2stimulerer fotosyntese og plantevækst med potentielle fordele for produktiviteten af kornafgrøder, verdens primære fødekilde til mennesker og husdyr. Kulstof, taget fra kuldioxid i luften af autotrofiske planter gennem fotosynteseprocessen eller taget fra jordkulstof, er faktisk et af de vigtigste næringsstoffer i fødevarebanen . Stigningen i biomasse er en effekt af simulerede eksperimenter, der forudsiger en 5-20% stigning i afgrødeudbyttet ved 550 ppm CO 2. Bladfotosyntesehastigheder har vist sig at stige 30-50% i C3-planter og 10-25% i C4 under CO 2 -niveauer fordoblet.
Fra 2010 fremkommer et mere komplet billede med en signifikant forskel i reaktionerne observeret for forskellige plantearter, vandtilgængelighed og ozonkoncentration . F.eks. Fandt Horsham Free-air koncentration berigelse ( FACE) 2007-2010-projektet (ved anvendelse af hvedeafgrøder) i Victoria, Australien, at "effekten af CO2 var at øge afgrødens biomasse. Ved modenhed 20% og rodbiomassen af antesis 49% ". Det har vist sig, at en stigning i atmosfærisk kuldioxid reducerer planternes vandforbrug og dermed kvælstofoptagelse , hvilket især gavner afgrødeudbyttet i tørre regioner.
Påtænkte virkninger på planternes næringsværdi
Men hvis stigningen i niveauet for CO 2Atmosfærisk øger effektivt væksten ( for eksempel korn ), af grunde, der stadig er dårligt forstået, reducerer den derefter næringsværdien af de vigtigste basisafgrøder (især ris , hvede og kartofler ) ved at reducere deres proteinindhold , af sporstoffer og B -vitaminer . Under eksperimentelle forhold er niveauet af CO 2øget (selv ikke kombineret med en øget temperatur) resulterer i et højere sukkerindhold i dyrkede planter (kilde til stadig stærkere alkoholer til druer), men også ved protein- og mineralmangler. Ris har også ofte høje koncentrationer af arsen , hvilket forsuring af medierne kan forværre. Endelig højere koncentrationer af CO 2forværre forsuring af ferskvand og forsuring af havene , hvilket kan påvirke algernes produktivitet (og dermed algedyrkning ).
Af denne grund er det unormalt høje CO 2 -niveau ifølge en nylig undersøgelse (2018) fra 2015-2050af vores atmosfære kunne i verden før 2050 føre til sygdomme forårsaget af mennesker og visse husdyr (svin, køer, fjerkræ) på grund af ernæringsmæssige mangler. I en undersøgelse offentliggjort i et specialnummer af PLOS Medicine om klimaforandringer og sundhed fokuserede Christopher Weyant og hans kolleger ved Stanford University på to vigtige mikronæringsstoffer , zink og jern. Under hensyntagen til klimaændringer og spisevaner viser de, at risikoen for sygdom vil ændre sig i de 137 lande. Hvis der ikke gøres noget, er stigningen i CO 2 -hastighedenvil reducere zink- og jernniveauet i fødevarer og koste anslået 125,8 millioner handicapjusterede leveår (95% konfidensinterval [CrI] 113,6–138,9) på verdensplan i perioden 2015–2050 på grund af en stigning i infektionssygdomme , diarré og tilfælde af anæmi , især i Sydøstasien og Afrika, hvor befolkningen allerede er hårdt ramt af zink- og jernmangel. Børn vil blive særlig påvirket med risiko for irreversible udviklingsforstyrrelser forbundet med disse mangler, som kan overføres over flere generationer i det mindste af epigenetiske årsager .
Weyants undersøgelse indikerer også, at ernæringsmæssig ulighed kan øges, og viser, at traditionelle folkesundhedsreaktioner (inklusive tilskud med mineraler og vitaminer og styrket kontrol af menneskers og dyresygdomme) måske ikke er nok til at dæmme op for sygdommen. Sådanne svar ville faktisk kun reducere 26,6% (95% af CI 23,8–29,6) af denne sundhedsmæssige, menneskelige og økonomiske byrde, mens en effektiv strategi til at reducere drivhusgasemissioner. Drivhuseffekt, som foreslået i Paris -klimaaftalen , ville forhindre op til 48,2% (95% af CIF -indekset 47,8–48,5) af denne belastning.
Selvom CO 2nærer plantens vækst, dets overskud forårsager en forringelse af deres fødeværdi, hvilket vil have globale konsekvenser for alle levende væsner, der forbruger planter, inklusive mennesker. Forfatterne tilskynder til bedre undersøgelse af virkningerne af øget CO 2atmosfærisk på andre forbindelser af vegetabilsk oprindelse, der har konsekvenser for menneskers sundhed (fx fedtsyrer, vitaminer, farmakologiske forbindelser, især da denne undersøgelse ikke tog højde for andre konsekvenser af stigningen i CO 2, om meteorologiske og biologiske farer (øget nedbrydning osv.) for fødevaresikkerhed, adgang til fødevarer, dets anvendelse og prisstabilitet eller kæderne af konsekvenser forsinket i rum og tid (især langsigtede virkninger af underernæring).
Landbrugsudbyttet stagnerer eller forringes i en del af verden, især på grund af opvarmning (hedebølger osv.) Og modificerede nedbørsregimer. Vitalafgrøder (især hvede og ris) er allerede påvirket i tropiske og tempererede zoner, og prospektive undersøgelser tyder på, at ris- og majsafgrøder kan falde med 20 til 40% bare på grund af de forventede temperaturstigninger i zonen. Tropisk og subtropisk i 2100, selv under hensyntagen til virkningerne af ekstreme klimatiske begivenheder. Denne sammenhæng kan medføre, at fødevarepriserne stiger, hvilket gør dem overkommelige for de fattigste, mens stigningen i niveauet af CO 2 i luftenkunne også reducere ernæringskvaliteten, især korn, der er vigtig for menneskers sundhed og potentielt for dyrenes (også kilder til mælk og kød (og derfor proteiner), mens biomassen i fisk også falder til søs .
"Det er endnu ikke klart, om faldet i næringsværdien af fødeafgrøder forårsaget af CO 2er lineær, og hvis ernæringskvaliteten allerede er faldet på grund af stigningen i CO2 siden starten af den industrielle revolution. "
Ud over tilpasningstiltag til klimaændringer, foranstaltninger til reduktion af CO 2 -emissionerog biologisk opsamling af CO 2er presserende nødvendige. Nogle sorter, der er mindre modtagelige for ernæringsmæssige underskud i et opvarmende klima, søger afslutter arbejdet fra Weyant og kolleger.
Virkningerne af stigende CO 2på planter er mere bekymrende end hvad der blev forudsagt af de første modeller i 1990'erne og begyndelsen af 2000'erne. Morgan et al. på basis af laboratorie- og in situ -forsøg bekræftet allerede i 2004, at CO 2 i fremkomne økosystemer, selv når det forbedrer produktiviteten med hensyn til biomasse, kan det alligevel have negative virkninger ved at ændre sammensætningen af arten og ved at reducere fordøjeligheden af korte græs f.eks. i steppevegetation ).
Drivhusgas og forsuring
CO 2er den næstvigtigste drivhusgas i atmosfæren efter vanddamp og bidrager med henholdsvis 26% og 60% til dette fænomen. Virkeligheden af global opvarmning observeret i planetarisk skala siden sidste århundrede bestrides ikke længere fra et videnskabeligt synspunkt, men den nøjagtige andel af ansvaret for kuldioxid i denne proces (sammenlignet med især metan ) skal stadig afklares, takket være fossile optagelser af især paleoklimater.
Desuden forsuring kunne følge af opløsningen af atmosfærisk kuldioxid true overlevelsen af mange marine organismer før XXI th århundrede, især i Exoskeleton forkalkede såsom koraller og skaldyr , men også nogle fisk.
En reduktion af menneskeskabte emissioner er målrettet af Kyoto-protokollen samt af direktiv 2003/87 / EF ; dens langsigtede geologiske binding er genstand for forskning, men er en kontroversiel løsning, når det kommer til simpelthen at indsprøjte CO 2 i geologiske lag.
Økosystemeffekter af øgede CO 2 -niveauer i vand og i luften
I vandCO 2har en vis eutrofisk virkning (det er et basisk næringsstof , essentielt for planter), men det er også en faktor i forsuring af havene og visse organer af ferskvand , som kan påvirke mange arter negativt (herunder visse mikroalger og andre akvatiske vand mikroorganismer beskyttet af kalkholdige strukturer, som kulsyre kan opløses). Forsuring fremmer også frigivelse og cirkulation og derfor biotilgængeligheden af de fleste tungmetaller , metalloider eller radionuklider (naturligt til stede i sedimenter eller af menneskeskabt oprindelse især siden den industrielle revolution).
I luftenForøgelsen af CO 2 -indholdet i atmosfærenkan også have differentierede eller endog antagonistiske virkninger afhængigt af dens hastighed, den miljømæssige og biogeografiske kontekst og ifølge nyere data afhængigt af årstid og sæsonvariationer i nedbør (især over skove)
Der er enighed blandt økologer forbundet med undersøgelsen af virkningerne af klimaændringer , at terrestriske og marine økosystemer vil blive alvorligt negativt påvirket ud over en stigning på 2 ° C i et århundrede.
I 2013 var økosystemernes virkelige reaktion på CO 2og dets biogeografiske moduleringer betragtes stadig som komplekse og skal forstås bedre på grund af talrige " biogeokemiske tilbagemeldinger " . Det skal ikke desto mindre belyses, hvis vi korrekt vil vurdere eller endog forudsige økosystemers planetariske eller lokale kapacitet med hensyn til naturlig kulstoflagring og dæmpning af virkningerne af klimaændringer , som mennesker fremkalder.
Den feedback, medieret af hydrologiske kredsløb er særligt vigtige og regnfald spiller en stor rolle. Den fysiologi af planter har mindst en velkendt rolle; op til et bestemt trin (ud over hvilket planten dør), stigningen i niveauet af CO 2luft reducerer stomatal konduktans og øger effektiviteten af vandbrug fra planter (mængden af vand, der er nødvendig for at producere en enhed med tørstof ), resulterer faldet i vandforbrug i større tilgængelighed af jordfugtighed. Det blev anslået i 2008, at virkningerne af stigende CO 2i luften på økosystemet bør forværres, når vand er en begrænsende faktor (men nitrogenindtag skal også tages i betragtning); dette er blevet vist ved nogle eksperimenter, men er en faktor, der er blevet "overset" af mange undersøgelser.
Dette forhold synes så stærk, at den gør det muligt - i tempererede zoner - præcist at forudsige de årlige variationer i stimuleringen af antenne biomasse efter stigningen i CO 2 niveau.i et blandet græsareal, der indeholder planter af type C3 og C4 , baseret på den samlede sæsonmæssige nedbør ; den regnfulde sommer har en positiv effekt, mens efteråret og foråret har en negativ indvirkning på reaktionen på CO 2. Effekten af stigende CO 2 niveauer vil derfor hovedsagelig afhænge af de nye balancer eller ubalancer, der vil blive etableret mellem sommer og efterår / forår nedbør.
Forbindelsen til nitrogen (et andet element, der forstyrres af menneskelige aktiviteter, herunder industrielt landbrug, industri og biltrafikemissioner ) findes her: kraftig nedbør i kolde og våde årstider fører til begrænsning af adgangen til køretøjer. Terrestriske planter med nitrogen og derfor reducere eller forbyde stimulering af biomasse med et niveau af CO 2hævet. Det blev også bemærket, at denne forudsigelse også var gældende for parceller "opvarmet" med 2 ° C eller uopvarmede og var ens for planter i C3 og total biomasse, hvilket ser ud til at gøre det muligt for prognosemoderne at lave robuste forudsigelser. Om reaktioner på høje CO 2 -koncentrationeraf økosystemet . Dette er et værdifuldt aktiv, fordi klimaprognoser for modeller med høj opløsning bekræfter den meget høje sandsynlighed for store ændringer i den årlige nedbørsfordeling, selv hvor den samlede årlige nedbørsmængde, der er faldet til jorden, ikke vil ændre sig. Disse videnskabeligt bekræftede data (i 2013) skulle hjælpe med at forklare nogle af de forskelle, der viste sig i resultaterne af forsøg baseret på udsættelse af planter for øgede CO 2 -niveauer., og forbedre den potentielle effektivitet af modeller, der ikke i tilstrækkelig grad tog hensyn til de sæsonmæssige virkninger af nedbør på biodiversitetsreaktioner på CO 2 14, især i skovmiljøer.
CO 2 reduktion i luften
Flere måder udforskes eller implementeres for at begrænse akkumuleringen af CO 2i luften. De kan involvere naturlige processer såsom fotosyntese eller industrielle processer. Man skal også skelne mellem fangst ved kilden og fangst i atmosfæren.
Den opstart indiske Carbon Clean Solutions (CCSL) har lanceret sin første anlæg, som opfanger og genanvendelser 100% CO 2(60.000 tons om året) fra et lille kulfyret kraftværk i Indien i Chennai (Madras); denne CO 2renses og derefter sælges til en lokal industri, der bruger den til at fremstille sodavand. CCSL -teknologi reducerer omkostningerne ved CO 2solgt til 30 dollars pr. ton i Indien og 40 dollars i Europa eller USA, langt under markedsprisen: 70 til 150 dollars pr. ton. Veolia har underskrevet en kontrakt med CCSL om at markedsføre denne proces internationalt. Samtidig søger Climeworks -virksomheden at fange CO 2 ved at filtrere den omgivende luft.
Det canadiske firma Carbon Engineering, grundlagt af ingeniøren David Keith og finansieret af Bill Gates og flere olie- og mineselskaber, har udviklet en reaktor, der udvinder CO 2atmosfære til en lavere pris end eksisterende fangstteknologier. Midlerne fra investorerne vil blive brugt til at kombinere denne direkte opsamlingsproces med en "Luft til brændstof" -proces, der gør det muligt at omdanne kulstoffet i atmosfæren til et brændstof, der ligner benzin. Det planlægger at bygge et større anlæg i Houston i partnerskab med Occidental Petroleum . Imidlertid CO 2 sensor reaktorerer meget energiintensive og skal derfor drives af vedvarende energikilder Det Videnskabelige Råd for Academies of European Sciences (EASAC) har forbehold: ifølge det er eliminering af CO 2 i luften forhindrer ikke klimaændringer og er til dato ikke op til IPCC-anbefalingerne.
Mod produktion af "solmetan" fra CO 2 ? .
I teorien transformerer CO 2i brændstof eller kemiske råvarer ville reducere brugen af fossile brændstoffer og reducere CO 2 -emissioner.
Elektrokemisk konvertering fra vedvarende elkilder har været genstand for megen forskning siden 2010'erne.
Et håb baseret på fotokemi er, at vi kun kan bruge sollys og ikke-forurenende katalysatorer, der er billige og rigelige på Jorden. Blandt de fotokatalysatorer og molekylære elektrokatalysatorer, der er nævnt i den videnskabelige litteratur i 2010'erne, er kun få få stabile og selektive til reduktion af CO 2 ; desuden producerer de hovedsageligt CO eller HCOO, og katalysatorer, der er i stand til at danne selv lave til moderate udbytter af stærkt reducerede carbonhydrider, forbliver sjældne.
Fire forskere, heraf to franskmænd (Julien Bonin & Marc Robert) producerede en katalysator, som er et jerntetraphenylporphyrinkompleks funktionaliseret med trimethylammoniumgrupper , som de præsenterer som værende (på offentliggørelsestidspunktet) den mest effektive og mest selektive til omdannelse af CO 2i CO, fordi det kan katalysere reduktionen af otte elektroner af CO 2i metan under simpelt lys, ved omgivelsestemperatur og tryk. Katalysatoren skal dog anvendes i en acetonitrilopløsning indeholdende en fotosensibilisator og en offerdonor til donor; den fungerer derefter stabilt i et par dage. CO 2transformeres først hovedsageligt til CO ved fotoreduktion, og hvis der er to reaktorer, genererer CO derefter metan med en selektivitet op til 82% og med et kvanteudbytte , dvs. en lyseffektivitet, på 0, 18%). Forfatterne mener, at andre molekylære katalysatorer kunne inspireres af det.
Systemer med "co-katalyse" påtænkes også, af molekylære katalysatorer, såvel som systemer baseret på perovskit eller baseret på komplekser af overgangsmetaller .
Noter og referencer
- KULDIOXID , sikkerhedsark (er) fra det internationale program for kemisk sikkerhed , konsulteret den 9. maj 2009
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- " Kuldioxid " , om databasen over farlige stoffer (adgang til 8. marts 2010 )
- Bernard M. og Busnot F. (1996), Usuel of general and mineral chemistry , Dunod, Paris, s. 229 .
- (da) Robert H. Perry og Donald W. Green , Perrys kemiske ingeniørhåndbog , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- (i) WM Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 s. ( ISBN 978-1-4398-2077-3 ) , s. 14-40
- (i) Irvin Glassman og Richard A. Yetter, Forbrænding , Amsterdam / Boston, Elsevier,2008, 4 th ed. , 773 s. ( ISBN 978-0-12-088573-2 ) , s. 6
- (in) Carl L. Yaws, Handbook of Thermodynamic Diagrams , bind. 1-3, Huston, Texas, Gulf Pub.,1996( ISBN 0-88415-857-8 , 978-0-88415-858-5 og 978-0-88415-859-2 )
- (i) David R. Lide, Handbook of Chemistry and Physics , CRC,2008, 89 th ed. , 2736 s. ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- “ Kuldioxid ” , på www.reciprocalnet.org (adgang 12. december 2009 )
- Indtastning af CAS-nummer "124-38-9" i den kemiske database GESTIS fra IFA (tysk organ med ansvar for arbejdsmiljø) ( tysk , engelsk ), adgang til den 6. december 2008 (JavaScript krævet)
- SIGMA-ALDRICH
- " Kuldioxid " i databasen over kemiske produkter Reptox fra CSST (Quebec-organisation med ansvar for sikkerhed og sundhed på arbejdspladsen), adgang til den 25. april 2009
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 s. , indbundet ( ISBN 978-1-4200-9084-0 ) , s. 6-107
- Frédéric Datchi, " CO 2 -molekylettåler pres bedre end forventet. » , Om Institut for Mineralogi og Fysik af kondenserede medier (IMPMC, Paris) ,april 2010(adgang til 28. januar 2016 ) .
- T. Uchida, S. Mae, J. Kawabata og T. Hondoh, "Fysiske data for CO 2Hydrat ” , i N. Handa og T. Ohsumi (dir), Direkte bortskaffelse af kuldioxid fra havet , Terra Scientific Publishing Company (TERRAPUB),1995, 45-61 s. ( læs online ).
- HS Chen, Termodynamik og sammensætning af kuldioxidhydrater , MS Thesis, Syracuse University, New York, 1972.
- H. Lee, C.-S. Lee, W.-M. Sung og S.-P. Kang, hydratfase -ligevægten for gæsteblandinger indeholdende CO 2, N2 og tetrahydrofuran , Fluid Phase Equilib. , 2001, 185, 101
- P. Englezos, R. Kumar og J. Ripmeester, Gassen hydrat fremgangsmåde til separation af CO 2fra brændselsgasblanding: makro- og molekylært niveauundersøgelser , Proceedings of the 6. International Conference on Gas Hydrates (ICGH) , 2008
- P. Linga, R. Kumar og P. Englezos, clathrathydratprocessen til indfangning af kuldioxid efter og før forbrænding , J. Hazard. Mater. , 2007a, 149 (3), 625–629.
- NH Duc, F. Chauvy og J.-M. Herri, CO 2opsamling ved hydratkrystallisation - En potentiel løsning til gasemission fra stålindustrien , Energi. Konv. Administrer. , 2007, 48, 1313–1322.
- Wassila Bouchafaa, Måling og modellering af dissociation betingelser af stabiliserede gashydrater til påføring på CO 2 opsamling (ph.d.-afhandling fra École Polytechnique), 22. november 2011
- YD Kim, HJ Lee, YS Kim og JD Lee, En undersøgelse af afsaltning af unsing CO 2hydrat teknologi , Proceedings of 6th International Conference on gashydrater (ICGH) , 2008
- MD Max, K. Sheps, SR Tatro og LB Osegovic, afsaltning af havvand som en gavnlig faktor for CO 2sekwestrering , Proceedings of the 6th International Conference on Gas Hydrates (ICGH) , 2008
- kap. I-4.3. Samtidig methanekstraktion og CO 2 -lagringsproces, s. 61 (eller s. 67 i [PDF] -versionen ) af Nadia Mayoufis afhandling, Karakterisering af hydrat coulis indeholdende CO 2anvendt på køleanlæg , doktorafhandling, École Polytechnique, 8. december 2010
- (in) " Kuldioxid: Sylvester Spiritus " Ebbe Almqvist, Historie af industrielle gasser , Springer,2003, 472 s. ( ISBN 978-0-306-47277-0 , læs online ), s.
- Sigaud de La Fond, Essay on forskellige arter af fast luft eller gas ... , Paris, Chez P. Fr. Gueffier,1785( læs online )
- (i) Joseph Priestley , " Observationer af forskellige slags Air " , Phil. Trans. , Vol. 62,1772, s. 147–264 ( ISSN 0260-7085 , DOI 10.1098 / rstl.1772.0021 , læs online )
- (in) Humphry Davy , " Om påføring af væsker dannet ved kondensering af gasser som mekaniske midler " , Phil. Trans. , Vol. 113,1823, s. 199–205 ( ISSN 0261-0523 , DOI 10.1098 / rstl.1823.0020 , læs online [PDF] )
- (en) Charles Thilorier, " størkning af kulsyre " , CR Hebd. Acad-sessioner. Sci. , Vol. 1,1835, s. 194-196 ( læs online )
- (i) HD-Roller Duane , " Thilorier Først og størkning af en permanent Gas (1835) " , Isis , vol. 43, nr . 21952, s. 109–113 ( ISSN 0021-1753 , DOI 10.1086 / 349402 )
- Dominique Pialot, “ CO2, et nyt marked? » , På latribune.fr ,17. juni 2019(adgang til 6. august 2019 ) .
- (in) " Carbondioxid Mad og drikkevarer, kvalitetsstandarder, kvalitetsstandarder og verifikation: EIGA Doc 70/17 " på eiga.eu ,2016(adgang 12. juli 2019 ) .
- (da) Sætte CO2 i brug - skabe værdi ud fra emissioner , International Energy Agency , i september 2019.
- Neil A. Campbell og Jane B. Reece , biologi , Erpi,2007, 1.400 s.
- Carboglace er et varemærke, der er registreret i Frankrig af Air Liquide
- von Baczko, K., red. Gmelins Handbuch der Anorganischen Chemie: Kohlenstoff , 8 th ed. , Chemie GMBH, Weinheim / Bergstr., 1970, del C. Afsnit 1, s. 413–416 .
- Phillips, RJ, Davis, BJ, Tanaka, KL, Byrne, S., Mellon, MT, Putzig, NE, ... & Smith, IB (2011) Massive CO2- isaflejringer sekvestreret i de sydpolære lagaflejringer på Mars . Science, 332 (6031), 838-841.
- (in) " Reaktionsnetværket i propanoxidationstrin over rene MoVTeNb M1-oxidkatalysatorer " , Journal of Catalysis , Vol. 311,2014, s. 369-385 ( læs online )
- (in) " Overfladekemi af ren oxidfase M1 MoVTeNb Under drift ved selektiv oxidation af propan til acrylsyre " , Journal of Catalysis , Vol. 285,2012, s. 48-60 ( læs online )
- (in) Kinetiske undersøgelser af propanoxidation er Mo og V blandede oxidbaserede katalysatorer ,2011( læs online )
- (in) " multifunktionalitet af krystallinsk MoV (NBPT) M1 -oxidkatalysatorer ved selektiv oxidation af propan og benzylalkohol 3 (6) " , ACS Catalysis , bind. 3, n o 6,2013, s. 1103-1113 ( læs online )
- (in) Colin Finn , Sorcha Schnittger Lesley J. Yellowlees og Jason B. Love , " Molekylære tilgange til den elektrokemiske reduktion af kuldioxid " , Chemical Communications , bind. 48, nr . 10,2012, s. 1392-1399 ( PMID 22116300 , DOI 10.1039 / c1cc15393e ).
- (en) CO2. Jordkoncentration af CO 2 i jordens atmosfære.
- Intoxikation ved indånding af kuldioxid , Medicinsk-teknisk fil 79, INRS, 1999.
- CO 2 koncentrationer i indeluft og sundhedseffekter, ANSES-udtalelse, kollektiv ekspertrapport, ANSES, 2013/07, 294 s.
- Indoor Air Quality Observatory (Oqai), Ministeriet for Økologi, Ademe, CSTB, AirParif, Atmo ...
- (in) Chatzidiakou, L. Mumovic, D., & Summerfield, A. (2015). Er CO 2en god proxy for indeklima i klasselokaler? Del 1: Sammenhængen mellem termiske forhold, CO2-niveauer, ventilationshastigheder og udvalgte indendørs forurenende stoffer. Building Services Engineering Research and Technology, 36 (2), 129-161 ( abstrakt ).
- (in) Cetin Sevik M & H (2016) Indendørs kvalitetsanalyse af CO2 til Kastamonu University . I konference for International Journal of Arts & Sciences (bind 9, nr. 3, s. 71).
- (i) Jaber AR Dejan Marcella M & U (2017) Effekten af indendørs temperatur og CO2-niveauet er kognitiv præstation af voksne hundyr i en universitetsbygning i Saudi-Arabien , Energi Procedia , 122, 451-456.
- (in) Myhrvold AN, Olsen S & Lauridsen O Indendørs miljø i skoler, elever og sundhedsmæssige præstationer med hensyn til CO2-koncentrationer , Indendørs luft , 96 (4), 369-371, 1996
- (en) Prestmo LS (2018) Målinger af indeklima parametre i træningszonen i en ishockeyhal (kandidatafhandling, NTNU).
- (in) Prestmo LS (2018) Målinger af indeklimaparametre i træningsområdet i en ishockeyhal (kandidatafhandling, NTNU) (se afsnit 7.2 Forøget CO 2 koncentration under en kamp)
- (in) Eks: Kenneth W. Rundell (2004) "Lungefunktions henfald hos kvindelige ishockeyspillere: Er der et forhold til skøjteluftens kvalitet? " Toksikologi ved indånding , 16 (3): 117-123
- Forgiftning ved indånding af kuldioxid , Medico-teknisk fil 79 TC 74, INRS
- D Dr. Pieter Tans (3 maj 2008) Annual CO 2molfraktionsstigning (ppm) for 1959–2007 , National Oceanic and Atmospheric Administration , Earth System Research Laboratory , Global Monitoring Division ( yderligere detaljer .)
- NOAA / Law Dome
- NOAA / Mauna Loa
- Climate Research Unit (Univ. East Anglia)
- Solar Influences Data Analysis Center (SIDC)
- http://advances.sciencemag.org/content/3/1/e1601207
- Tendenser i atmosfærisk kuldioxid - Global månedlig gennemsnitlig CO2 , National Oceanic & Atmospheric Administration (NOAA) - Earth System Research Laboratories (ESRL), adgang 25. april 2021.
- (in) Kuldioxidinformationsanalysecenter i juni 1998 , " Historisk CO 2rekord afledt af en spline fit (20 års cutoff) af Law Dome DE08 og DE08-2 iskerner ”, DM Etheridge, LP Steele, RL Langenfelds, RJ Francey (Division of Atmospheric Research, CSIRO, Aspendale, Victoria, Australien), J.-M. Barnola ( Laboratorium for glaciologi og miljøgeofysik , Saint-Martin-d'Hères , Frankrig) og VI Morgan (Antarktis CRC og Australian Antarctic Division, Hobart, Tasmanien, Australien)
- (in) FN's miljøprogram (UNEP) - Tredje vurderingsrapport Klimaforandringer 2001 , " Klimaændringer 2001: Arbejdsgruppe I: Det videnskabelige grundlag - Kapitel 3. Kulcyklus og atmosfærisk kuldioxid " Resumé
- Vores planetinfo, CO 2 -indholdsteg kraftigt fra 1990 til 2004 (adgang 31. marts 2012)
- ESRL Global Monitoring Division
- Forskningsgruppe Carbon Cycle Greenhouse Gases
- Atmosphere Dossier , Pour la science , juni 1996
- Earth Guide / UCSD, Klima og CO 2i atmosfæren (adgang 10. oktober 2007)
- Robert A. Berner og Zavareth Kothavala, GEOCARB III: En revideret model af atmosfærisk CO 2over Phanerozoic [PDF] , American Journal of Science , bind. 301, 2001, c. 2, s. 182-204, DOI : 10.2475 / ajs.301.2.182 (adgang 15. februar 2008)
- Sigurdsson, Haraldur og Houghton, BF, Encyclopedia of vulkaner , 2000, Academic Press, San Diego ( ISBN 0-12-643140-X )
- Van Gardingen, PR; Grace, J .; Jeffree, CE; Byari, SH; Miglietta, F. Raschi, A.; Bettarini, I., kap. Langsigtede virkninger af forbedret CO 2koncentrationer om bladgasudveksling: forskningsmuligheder ved hjælp af CO 2fjedre , redaktør: Raschi, A .; Miglietta, F. Tognetti, R. van Gardingen, PR (red.), 1997, Cambridge University Press, Cambridge ( ISBN 0-521-58203-2 ) , s. 69-86
- Martini M., kap. CO 2emissioner i vulkanske områder: saghistorier og hasarder , i Planteanlæg på forhøjet CO 2: Beviser fra naturlige kilder , redaktør: Raschi, A.; Miglietta, F. Tognetti, R. van Gardingen, PR (red.), 1997, Cambridge University Press, Cambridge ( ISBN 0-521-58203-2 ) , s. 69-86
- De vulkanske gasser og deres virkninger (in) , adgang til 2007-09-07
- Martin Wolf, " Skeptikere over klimaændringer mister terræn ", om The New Economist ,17. juli 2014(adgang 26. juli 2014 ) .
- " Altid mere CO 2i atmosfæren ”, La Croix ,30. oktober 2017( ISSN 0242-6056 , læst online , adgang 31. oktober 2017 )
- Gamilloaug E., Atmosfærisk kulstof nåede sidste år niveauer, der ikke er set i 800.000 år , Science News , 2. august 2018
- " Globale CO 2 -emissioner"Gled" i 2018 på + 2,7% " på Liberation.fr (hørt den 6. december 2018 )
- " CO2 " .
- Lobell DB & Field CB (2008) Estimering af kuldioxid (CO 2) befrugtningseffekt ved anvendelse af væksthastighedsanomalier af CO 2og afgrødeudbytter siden 1961 . Glob Chang Biol. ; 14 (1): 39–45.
- FN Tubiello , JF Soussana og SM Howden , ” Crop og græs reaktion på klimaændringer ”,2007( PMID 18077401 , PMCID 2148358 , DOI 10.1073 / pnas.0701728104 , Bibcode 2007PNAS..10419686T ) ,s. 19686–19690
- (in) Rob Norton et al. Virkningen af forhøjet kuldioxid på hvedens vækst og udbytte i Australian Grains Free Air Carbon Dioxide Enrichment (AGFACE) eksperimentet , regional.org.au 2008
- (i) Daniel R. Taub, Virkninger af Rising luftens kuldioxid Koncentrationerne af et Planter , Natur , Education Viden 3 (10): 21 2010
- (in) Taub DR, Miller B, Allen H. Effekter af forhøjet CO2 på proteinkoncentrationen af madafgrøder: en meta-analyse , Global Change Biology 1. marts; 14 (3): 565-75, 27. november 2007
- (en) Myers SS Zanobetti A, Kloog I, P Huybers, Leakey AD, Bloom AJ, et al. (2014), Stigende CO2 truer menneskelig ernæring. Natur . Juni; 510 (7503): 139.
- (in) Zhu C, Kobayashi K, Loladze I, Zhu J, Jiang Q, Xu, et al. (2018), CO2-niveauer (CO2) i dette århundrede vil ændre protein, mikronæringsstoffer og vitaminindholdet i riskorn med potentielle sundhedsmæssige konsekvenser for de fattigste risafhængige lande , Sci Adv. 2018: 4: eaaq1012.
- (in) Loladze I (2014) Skjult skift af ionomet af planter udsat for forhøjede CO2-udtømte mineraler på basis af menneskelig ernæring , Elifa . ; 3: e02245.
- (i) Andrew A. Meharg, Jeanette Hartley-Whitaker (2002) Arsen optagelse og metabolisme i arsen resistente og ikke-resistente plantearter, udstationerede april 4, 2002 DOI: 10,1046 / j.1469-8137.2002.00363.x Issue New Phytologist , Bind 154, udgave 1, side 29–43, april 2002
- (da) Ebi KL, Ziska LH (2018) Stigninger i atmosfærisk kuldioxid: Forventede negative virkninger på fødevarekvaliteten. PLoS Med 15 (7): e1002600. https://doi.org/10.1371/journal.pmed.1002600 ; Undersøgelse offentliggjort under Creative Commons CC0 public domain licens
- (i) Helena Bottemiller evich, " Den store næringsstof sammenbrud " , Politico ,13. september 2017( læs online , hørt den 13. september 2017 ).
- (i) Weyant C Brandeau ML, Burke M, DB Lobell, Bendavid S & S Basu (2018), Forventet byrde og afbødning af carbondioxid-inducerede ernæringsmæssige mangler og relaterede sygdomme: en simulering modelundersøgelse, PLoS Med. ; 15 (7): e1002586
- Vickers MH (2014) Ernæring i tidligt liv, epigenetik og programmering af senere livssygdomme . Næringsstoffer. 2. juni; 6 (6): 2165–78.
- Zhu C, Zeng Q, McMichael A, Ebi KL, Ni K, Khan AS, et al. (2015) Historisk og eksperimentelt bevis for øget koncentration af artemesinin, en global anti-malariabehandling med nylige og forventede stigninger i atmosfærisk kuldioxid . Klima forandring. 1. september; 132 (2): 295-306
- Porter JR, Xie L, Challinor AJ, Cochrane K, Howden SM, Iqbal MM, et al. (2014) Fødevaresikkerhed og fødevareproduktionssystemer . I: Klimaændringer 2014: Virkninger, tilpasning og sårbarhed. Del A: Globale og sektorielle aspekter. Bidrag fra arbejdsgruppe II til den femte vurderingsrapport fra det mellemstatslige panel om klimaændringer [Field CB, Barros VR, Dokken DJ, Mach KJ, Mastrandrea MD, et al. (red.)]. Cambridge University Press, Cambridge, Storbritannien og New York, NY, USA, s. 485–533
- Battisti DS & Naylor RL (2009) Historiske advarsler om fremtidig fødevareusikkerhed med hidtil uset sæsonvarme . Science 323, 240–244.
- (in) Nowak RS, SD Ellsworth DS og Smith (2004), Planters funktionelle reaktioner på forhøjet atmosfærisk CO 2- understøtter fotosyntetiske og produktivitetsdata fra FACE-eksperimenter tidlige forudsigelser? , Nyt Phytol. , 162, 253–280 ( abstrakt )
- (i) Morgan JA et al. (2004), CO 2forbedrer produktiviteten, ændrer artssammensætningen og reducerer fordøjeligheden af kortgræsstegvegetation , Ecol. Appl. , 14, 208–219
- (in) JT Kiehl og Kevin E. Trenberth, " Earth's Annual Global Mean Energy Budget " , Bulletin of the American Meteorological Society , bind. 78, nr . 2Februar 1997, s. 197-208 ( DOI 10.1175 / 2008BAMS2634.1 , læs online )
- (in) Klimaændringer: Hvordan ved vi det? , NASA, udateret
- (da) Emmanuel Quiroz, temperatur og CO 2Korrelationer fundet i Ice Core Records , udateret
- (in) Bärbel Hönisch Andy Ridgwe Daniela N. Schmidt, Ellen Thomas, Samantha J. Gibbs, Appy Sluijs, Richard Zeebe, Lee Kump, Rowan C. Martindale, Sarah E. Greene, Wolfgang Kiessling, Justin Ries, James C.Zachos , Dana L. Royer, Stephen Barker, Thomas M. Marchitto Jr. , Ryan Moyer, Carles Pelejero Patrizia Ziveri, Gavin L. Foster og Branwen Williams, " The Geological Record of Ocean Acidification " , Science , vol. 335, nr . 6072, 2. marts 2012, s. 1058-1063 ( DOI 10.1126 / science.1208277 , læs online )
- (in) Joe Romm, Geological Society: Forsurende oceaner staver marin biologisk nedsmeltning "ved slutningen af århundredet" , Climate Progress , 31. august 2010
- (en) C. Langdon og J. Atkinson, " Effekt af forhøjet p CO 2om fotosyntese og forkalkning af koraller og interaktioner med sæsonændring i temperatur / bestråling og næringsstofberigelse ” , Journal of Geophysical Research , bind. 110,7. september 2005, C09S07 ( DOI 10.1029 / 2004JC002576 , læs online )
- (in) Katharina E. Fabricius, Chris Langdon, Sven Uthicke Craig Humphrey, Sam Noonan, Glenn De'ath, Remy Okazaki, Nancy Muehllehner, Martin S. Glas og Janice M. Lough, " Tabere og vindere i koralrev akklimatiserede sig til forhøjede kuldioxidkoncentrationer ” , Nature Climate Change , vol. 1,29. maj 2011, s. 165-169 ( DOI 10.1038 / nclimate1122 , læs online )
- (i) Joe Romm, kuldioxid "Driving Fish Crazy" og truer deres overlevelse, Undersøgelse finder , Klima Fremskridt 23. januar, 2012.
- Sebastian Leuzinger og Christian Korner, “Regnfordeling er den vigtigste drivkraft for afstrømning under fremtidig CO 2-koncentration i en tempereret løvskov ”, Glob. Skift Biol. , Vol. 16,2010, s. 246–254 ( resumé )
- Peters, GP et al. , Udfordringen med at holde den globale opvarmning under 2 ° C , Nature Clim. Ændring , 3, 4-6, 2013
- Reich PB og Hobbie SE (2013), årti-lang kvælstofbegrænsning på jorden på CO 2befrugtning af plantebiomasse , Nature Clim. Change , 3, 278-282 ( resumé )
- Mark J. Hovenden, Paul CD Newton og Karen E. Wills, " Sæsonbestemt ikke årlig nedbør bestemmer græsarealers biomasse-reaktion på kuldioxid ", Nature , bind. 511,2014( DOI 10.1038 / nature13281 , resumé )
- Sokolov AP et al. (2008), Konsekvenser af at overveje kulstof-nitrogen-interaktioner på feedbacks mellem klima og den terrestriske kulstofcyklus , J. Clim. , 21, 3776–3796 ( resumé og bibliografi )
- Morgan J. et al. (2011), C4 græsser trives, da kuldioxid eliminerer udtørring i opvarmet halvtørret græsareal , Nature , 476, 202–205 ( abstrakt )
- (en) Leakey A. et al. (2009), forhøjet CO 2virkninger på plantens kulstof-, nitrogen- og vandforhold: seks vigtige erfaringer fra FACE , J. Exp. Bot. , 60, 2859–2876 ( abstrakt )
- (i) McMurtrie, RE et al. (2008), Hvorfor er plantevækstrespons på forhøjet CO 2forstærket når vand er begrænsende, men reduceret når kvælstof er begrænsende? En hypotese om vækstoptimering , Funct. Plant Biol. , 35, 521–534
- PB Reich, SE Hobbie, T. Lee et al. , " Nitrogenbegrænsning begrænser holdbarheden af økosystemets reaktion på CO 2 », Nature , vol. 440,2006, s. 922–925 ( resumé )
- PB Reich, BA Hungate og Y. Luo, ” Kulstof-kvælstof-interaktioner i terrestriske økosystemer som reaktion på stigende atmosfærisk kuldioxid ”, Annu. Rev. Skole. Evol. Syst. , Vol. 37,2006, s. 611-636 ( resumé )
- J. A. Morgan, DE Pataki, C. Körner et al. , " Vandforhold i græsarealer og ørkenøkosystemer udsat for forhøjet atmosfærisk CO 2 », Oecologia , bind. 140,2004, s. 11–25 ( læs online [PDF] )
- (en) Derner JD et al. , Over og under jorden svarene fra C3 - C4 artsblandinger til forhøjet CO 2og tilgængelighed af jordvand , Glob. Skift Biol. , 9, 452–460, 2003
- (en) Dukes JS et al. (2005), Responses of grassland production to single and multiple globale miljøændringer , PLoS Biol. , 3, 1829-1837 ( abstrakt
- Grunzweig JM og Korner C. (2001), Vækst-, vand- og kvælstofrelationer i græsarealmodelle økosystemer i Israels halvtørre Negev udsat for forhøjet CO 2, Oecologia , 128, 251-262 ( abstrakt )
- (en) Marissink M., Pettersson A. og Sindhoj E. (2002) Overjordisk planteproduktion under forhøjet kuldioxid i en svensk semi-naturlig græsareal , Agric. Økosystem. Om. , 93, 107-120 ( abstrakt )
- (in) Singh D., Tsiang M., B. og Rajaratnam Diffenbaugh NS (2013) Ekstreme nedbørsmængder over det kontinentale USA i et forbigående, højopløst, helt klimamodeleksperiment , J. Geophys. Res. , D 118, 7063–7086 ( abstrakt )
- (i) Piao S. et al. (2013), Evaluering af terrestriske kulstofcyklusmodeller for deres reaktion på klimavariabilitet og CO 2tendenser , Glob. Skift Biol. , 19, 2117–2132 ( abstrakt )
- (in) De Kauwe MG et al. (2013), brug af skovvand og vandeffektivitet ved forhøjet CO 2: en model-data-sammenligning på to kontrasterende tempererede skov-FACE-steder , Glob. Skift Biol. , 19, 1759–1779 ( abstrakt )
- " Opstarten CCSL og Veolia vil opfange og videresælge CO 2i stor skala " ,30. marts 2017.
- Canadisk firma bakket op af Bill Gates ønsker at fange CO 2i luften , Le Figaro , 29. juni 2019.
- (in) Richard Littlemore, "Kan dette firma være en BC -andel af klimaforandringsløsningen?" , The Globe and Mail , Report on business magazine , oktober 2019
- Bonin J, Maurin A & Robert M (2017) Molekylær katalyse af den elektrokemiske og fotokemiske reduktion af CO 2med Fe og Co metalbaserede komplekser. Nylige fremskridt . Coord. Chem. Rev. 334, 184-198 | URL: https://www.researchgate.net/profile/Julien_Bonin/publication/308271980_Molecular_Catalysis_of_the_Electrochemical_and_Photochemical_Reduction_of_CO2_with_Fe_and_Co_Metal_Based_Complexes_Recent_Advances/links/5c0639fb299bf169ae3078e9/Molecular-Catalysis-of-the-Electrochemical-and-Photochemical-Reduction-of-CO2- med-Fe-og-Co-metalbaserede-komplekser-Recent-Advances.pdf
- Jhong HR.M, Ma S & Kenis PJA (2013) Elektrokemisk omdannelse af CO 2til nyttige kemikalier: nuværende status, resterende udfordringer og fremtidige muligheder . Curr. Opin. Chem. Eng. 2, 191–199 ( resumé )
- Aresta M, Dibenedetto A & Angelini A (2014) Katalyse til valorisering af udstødningskulstof: fra CO 2til kemikalier, materialer og brændstoffer . Teknologisk brug af CO2. Chem. Rev. 114, 1709–1742 ( resumé )
- Qiao J, Liu Y, Hong F & Zhang J (2014) En gennemgang af katalysatorer til elektroreduktion af kuldioxid for at producere brændstoffer med lavt kulstofindhold . Chem. Soc. Rev. 43, 631–675
- Parajuli R et al. (2015) Integration af anodiske og katodiske katalysatorer af jordrige materialer til effektiv, skalerbar CO 2reduktion . Top. Catal. 58, 57–66
- Tatin A et al. (2016) Effektiv elektrolyser til CO 2opdele i neutralt vand ved hjælp af masser af jordbund . Proc. Natl Acad. Sci. USA 113, 5526–5529 | URL: https://www.pnas.org/content/pnas/113/20/5526.full.pdf
- Sahara G & Ishitani O (2015) Effektive fotokatalysatorer til CO 2reduktion . Inorg. Chem. 54, 5096–5104 | URL: https://pubs.acs.org/doi/full/10.1021/ic502675a
- Takeda H, Cometto C, Ishitani O & Robert M (2017) Elektroner, fotoner, protoner og Earth-rigelige metalkomplekser til molekylær katalyse af CO 2reduktion . ACS Catal. 7, 70–88 ( resumé )
- Shen, J. et al. (2015) Elektrokatalytisk reduktion af kuldioxid til kulilte og metan ved en immobiliseret cobaltprotoporphyrin . Nat. Almindelige. 6, 8177 | URL: https://www.nature.com/articles/ncomms9177
- Weng Z et al. (2016) Elektrokemisk CO 2reduktion til carbonhydrider på en heterogen molekylær Cu -katalysator i vandig opløsning . J. Am. Chem. Soc. 138, 8076–8079 | URL: https://pdfs.semanticscholar.org/a69e/11c9a8e97716bdbd4a24aa5e687f447616fa.pdf .
- Manthiram K, Beberwyck BJ & Alivisatos AP (2014) Enhanced elektrokemisk methanisering af kuldioxid med et dispergerbart nanoskala kobberkatalysator . J. Am. Chem. Soc. 136, 13319–13325
- Xie MS et al. (URL: https://cloudfront.escholarship.org/dist/prd/content/qt4882v99t/qt4882v99t.pdf ) Aminosyremodificerede kobberelektroder til forbedret selektiv elektroreduktion af kuldioxid mod kulbrinter . Energi Ca. Sci. 9, 1687–1695 (2016)
- Wu T et al. (2014) En kulstofbaseret fotokatalysator omdanner effektivt CO 2til CH4 og C2H2 under synligt lys . Grøn Chem. 16, 2142–2146
- AlOtaibi B, Fan S, Wang D, Ye J & Mi Z (2016) Wafer-niveau kunstig fotosyntese forCO 2reduktion til CH4 og CO ved hjælp af GaN nanotråde . ACS Catal. 5, 5342-5348 ( resumé )
- Liu X, Inagaki S & Gong J (2016) Heterogene molekylære systemer til fotokatalytisk CO 2reduktion med vandoxidation . Angew. Chem. Int. Red. 55, 14924–14950 ( abstrakt )
- Wang Y et al. (2016) Let et-trins syntese af hybrid grafitisk carbonnitrid og carbonkompositter som højtydende katalysatorer for CO 2fotokatalytisk omdannelse . ACS-appl. Mater. Interf. 8, 17212–17219 ( resumé )
- Zhu, S. et al. (2016) Fotokatalytisk reduktion af CO 2med H2O til CH4 over ultratynde SnNb2O6 2D nanosheets under synlig lysbestråling . Grøn Chem. 18, 1355–1363 | URL: https://www.researchgate.net/profile/Ling_Wu10/publication/283244219_Photocatalytic_reduction_of_CO_2_with_H_2_O_to_CH_4_over_ultrathin_SnNb_2_O_6_2D_nanosheets_under_visible_light_irradiation/links/569dcad408ae950bd7a6b275.pdf )
- Yu L et al. (2016) Forbedret aktivitet og stabilitet af kulstofdekorerede kobberoxid mesoporøse nanoroder til CO 2reduktion i kunstig fotosyntese . ACS Catal. 6, 6444-6454 ( resumé )
- Azcarate I, Costentin C, Robert M & Savéant J.-M (2016) En undersøgelse af gennemgående rum charge interaktion erstatningsprodukter virkninger i molekylær katalyse fører til udformningen af den mest effektive katalysator af CO2-til-CO elektrokemiske omsætning . J. Am. Chem. Soc. 138, 16639–16644
- Costentin C, Robert M, Savéant JM. & Tatin A (2015) Effektiv og selektiv molekylær katalysator til CO2-til-CO elektrokemisk omdannelse i vand . Proc. Natl Acad. Sci. USA 112, 6882–6886
- Heng Rao, Luciana C. Schmidt, Julien Bonin & Marc Robert (2018) “ Synlig lysdrevet metandannelse fra CO 2med en molekylær jernkatalysator ”; Brev | 17. juli 2017 Natur bind 548, side 74–77 (3. august 2017) | URL: https://www.nature.com/articles/nature23016#ref2
- Li, X., Yu, J., Jaroniec, M., & Chen, X. (2019). Kokatalysatorer til selektiv fotoreduktion af CO 2til solbrændstoffer. Kemiske anmeldelser, 119 (6), 3962-4179. ( opsummering )
- Zhang, B., & Sun, L. (2019). Kunstig fotosyntese: muligheder og udfordringer ved molekylære katalysatorer . Chemical Society Anmeldelser, 48 (7), 2216-2264.
- Andrei V, Reuillard B & Reisner E (2019) Bias-fri solar syntesegasproduktion ved at integrere en molekylær cobaltkatalysator med perovskit - BiVO 4 tandem . Naturmaterialer, 1-6 ( resumé )
- Dalle KE, Warnan J, Leung JJ, Reuillard B, Karmel IS & Reisner E (2019) Electro-og sol-drevet brændstof syntese med første række overgangsmetalkomplekser . Kemiske anmeldelser, 119 (4), 2752-2875 | URL: https://pubs.acs.org/doi/full/10.1021/acs.chemrev.8b00392 ( PDF-version )
Se også
Bibliografi
- Gérard Borvon, Historie af kulstof og CO 2. Fra livets oprindelse til klimaændringer , Vuibert, 2013, 256 s.