Atomisk orbital
I kvantemekanikken , en atomorbital er en matematisk funktion , der beskriver bølge opførsel af en elektron eller et par elektroner i et atom . Denne funktion giver sandsynligheden for tilstedeværelsen af et elektron af et atom i en given region af dette atom. Det er således ofte repræsenteret ved hjælp af isosurfaces , som afgrænser det område, inden for hvilket sandsynligheden for tilstedeværelsen af elektronen er større end en given tærskel, for eksempel 90%. Sådanne regioner er ikke nødvendigvis forbundet og kan præsentere komplekse former som følge af sfæriske harmoniske .
Hver atombane defineres af en unik triplet ( n , ℓ , m ℓ ) af kvantetal, der henholdsvis repræsenterer elektronens energi , dens vinkelmoment og projektionen af dette vinkelmoment på en given akse. Hver af disse orbitaler kan optages af højst to elektroner, der adskiller sig fra hinanden ved hjælp af deres magnetiske kvantetal spin m s . Vi taler om s , p , d og f orbitaler for at betegne orbitaler defineret med et vinkelmoment ℓ lig med henholdsvis 0, 1, 2 og 3. Disse navne kommer fra de gamle navne på spektrallinierne af alkalimetalerne beskrevet som skarpe , hoved , diffus og fin eller grundlæggende ; orbitalerne svarende til ℓ > 3 derpå navngivet alfabetisk g , h , i , k , osv , undladelse af bogstavet j, fordi nogle sprog ikke skelner det fra bogstavet i.
Atomiske orbitaler er de elektroniske skyers grundlæggende bestanddele, hvilket gør det muligt at modellere elektroners opførsel i stof. I denne model kan elektronskyen i et multi-elektronatom tilnærmes som en elektronkonfiguration dannet ud fra produktet af flere hydrogenoide orbitaler . Strukturen af grundstoffernes periodiske system i blokke omfattende, på hver periode , i alt 2, 6, 10 eller 14 elementer , er en direkte konsekvens af det maksimale antal elektroner, der kan besætte atomorbitaler s , p , d og f .
Elektronens egenskaber
Kvante natur
Udviklingen af kvantemekanik og eksperimentelle observationer, såsom diffraktion af en elektronstråle gennem Youngs spalter, etablerede bølge-partikel-dualiteten til at beskrive elementære partikler . Elektroner kredser således ikke om atomkerner i definerede kredsløb som planeter omkring solen . Faktisk kan de ikke beskrives som små faste kugler defineret af en position og en hastighed omkring kernen. Snarere skal de ses som stående bølger, der optager et volumen, inden for hvilket de har defineret kvanteegenskaber, og de er i stand til at interagere med andre partikler.
- Korpuskulær natur :
- der kan kun være et helt antal elektroner i et atom;
- en udveksling af energi mellem en indfaldende partikel, for eksempel en foton , og elektronerne i et atom vedrører altid kun en elektron med undtagelse af alle de andre, selvom flere elektroner har en ikke-nul sandsynlighed for at være på samme tid kl. stedet hvor en af dem interagerer med denne foton;
- en elektron er udstyret med en bestemt og konstant elektrisk ladning og præsenterer et spin, hvis projektion på en kvantiseringsakse kan være lig med +12(spin op ) eller -12(drej ned ).
- Bølge natur :
- elektronens minimumsenergi svarer til en tilstand, der kan sammenlignes med den grundlæggende frekvens for en strenges vibrationer, kendt som jordtilstanden ; de højere energiniveauer niveauer af elektronen kan ses som de harmoniske af denne grundfrekvens;
- elektroner er aldrig placeret på et nøjagtigt punkt i rummet, men manifesterer sig i et volumen, hvori sandsynligheden for at interagere med dem på et givet punkt bestemmes af deres bølgefunktion .
Matematisk udtryk
Atomorbitaler kan defineres mere præcist gennem kvantemekanikens matematiske formalisme . I den forbindelse kvantetilstand af en elektron er bølgefunktionen Ψ som tilfredsstiller eigenvalue ligning af hamiltonsk H , også kaldet "tid uafhængig Schrödingerligning" , eller endda "ligning af stater stationær.”: H Ψ = E Ψ , hvor E er energien forbundet med denne bølgefunktion. Den elektroniske konfiguration af et multielektronisk atom tilnærmes ved lineær kombination ( konfigurationsinteraktion , baser ) af produkter med mono-elektroniske funktioner ( Slater-determinanter ). Den rumlige komponent i disse mono-elektroniske funktioner er atomorbitalerne, og hensynet til spin- komponenten definerer spinorbitalerne .
Atombanen er sandsynlighedsamplituden for tilstedeværelsen af en elektron omkring kernen i et isoleret atom. Denne sandsynlighed tæthed afhænger af kvadratet af modulus af bølgefunktionen Ψ . Dette bestemmes af Schrödinger-ligningen ved hjælp af orbital-tilnærmelse , hvilket indebærer at ignorere korrelationer mellem elektroner og beregne den elektroniske konfiguration af et atom som produkter af monoelektroniske bølgefunktioner. Dette er imidlertid en tilnærmelse, da fordelingen af forskellige elektroner i deres orbitaler faktisk er korreleret, hvor London-kræfter er en manifestation af denne korrelation.
Orbitalberegning
Atomorbitaler kan være monoelectron orbitaler, som er eksakte løsninger af Schrödingerligningen for en hydrogenoid (dvs. enkelt elektron) atom . De kan også være basis for beregningen af bølgefunktionerne, der beskriver de forskellige elektroner i et atom eller et molekyle. Det valgte koordinatsystem er generelt det for sfæriske koordinater (r, θ, φ) i atomer og kartesiske koordinater (x, y, z) i polyatomiske molekyler. Fordelen ved sfæriske koordinater er, at bølgefunktionen i en orbital er produktet af tre funktioner, der hver afhænger kun af en af de tre koordinater: ψ (r, θ, φ) = R (r) Θ (θ) Φ (φ) .
Den radiale funktion R (r) kan generelt modelleres gennem tre almindeligt anvendte matematiske former:
- Atomenergiorbinaler af hydrogen er afledt af nøjagtige løsninger af Schrödinger-ligningen for en elektron og en atomkerne. Den del af funktionen, der afhænger af den radiale afstand, har radiale knudepunkter og falder langs e - a r , a er en konstant.
- Den Slater-typen orbital ( STO ) er en form af en kredsende uden radiale knudepunkter men aftager langs r som en hydrogenoid orbital.
- Den Gaussiske orbitale ( GTO ) er blottet for radiale knudepunkter og falder langs e - a r 2 .
Hydrogenoide orbitaler anvendes i uddannelsesværktøjer, men det er orbitaler af Slater-typen, der fortrinsvis bruges til at modellere atomer og diatomiske molekyler i digital kemi . Polyatomiske molekyler med tre eller flere atomer modelleres generelt ved hjælp af Gaussiske orbitaler, som er mindre præcise end Slater-orbitaler, men hvis kombination i stort antal gør det muligt at nærme sig præcisionen med hydrogenoidorbitaler.
Den skarpkantethedsfaktor Θ (θ) Φ (φ) genererer funktioner, der er reelle lineære kombinationer af sfæriske harmoniske Ym
ℓ(θ, φ) , hvor ℓ og m er henholdsvis det azimutale kvantetal og det magnetiske kvantetal .
Orbitaler af et hydrogenatom
Orbitaler beregnes som komplekse tal , så vi taler om komplekse orbitaler , men oftest bruger vi lineære kombinationer af sfæriske harmoniske valgt, så de imaginære dele annullerer hinanden: orbitalerne bliver således reelle tal , og vi taler om rigtige orbitaler .
Komplekse orbitaler
Hver atombane defineres af en triplet af kvantetal ( n , ℓ , m ℓ ) og kan højst indeholde to elektroner, der hver især adskiller sig i deres magnetiske spin-kvantetal , som kun kan være op eller ned ; den udelukkelse princip Pauli faktisk forbyder to elektroner fra det samme atom i at dele samme kvantetilstand :
- det vigtigste kvantetal n er et naturligt tal, der ikke er nul: n ≥ 1 ;
- det sekundære kvantetal (eller det azimutale kvantetal) ℓ er et positivt eller nul heltal, der verificerer 0 ≤ ℓ ≤ n - 1 og er knyttet til kvantiseringen af orbitalens vinkelmoment ;
- det magnetiske kvantetal m ℓ er et heltal, der tilfredsstiller - ℓ ≤ m ℓ ≤ ℓ og knyttet til kvantiseringen af projektionen af vinkelmomentet på en given akse;
- det magnetiske kvantetal spin m s er lig med -12eller +12hvor de tilsvarende elektroner almindeligvis er repræsenteret af symbolerne ↓ og ↑; det er en iboende egenskab af elektronen uafhængigt af de andre tre kvantetal.
Det vigtigste kvantetal n definerer den elektroniske skal, mens det azimutale kvantetal ℓ definerer typen af elektronisk subshell af elektronen. Afhængigt af om ℓ er 0, 1, 2, 3, 4, 5, 6 eller flere, er typen af disse underlag betegnet med bogstaverne s , p , d , f , g , h , i , etc.
Underlagene selv betegnes ved at forbinde kvantetallet n med det bogstav, der repræsenterer kvantetallet ℓ ; således er underlaget svarende til ( n , ℓ ) = (2, 1) betegnet 2p.
Den elektroniske konfiguration af atomer bemærkes ved at angive de elektroniske underlag med, som en eksponent , antallet af elektroner på dette underlag. Ved konstruktion er antallet af underlag pr. Elektronisk lag lig med n , mens antallet af orbitaler pr. Elektronisk underlag s , p , d , f er 1, 3, 5, 7 osv. Hver af disse orbitaler kan højst indeholde to elektroner, det maksimale antal elektroner pr. Type subshell s , p , d , f er 2, 6, 10, 14.
Tabel over de første komplekse orbitaler af et hydrogen atom| Kvantumtal | Undercoat | Magnetisk kvantetal m ℓ | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Vigtigste | Azimuthal | -3 | -2 | -1 | 0 | 1 | 2 | 3 | |
| n = 1 | ℓ = 0 | 1 s |

|
||||||
| n = 2 | ℓ = 0 | 2 sek |

|
||||||
| ℓ = 1 | 2 s |

|

|

|
|||||
| n = 3 | ℓ = 0 | 3 sek |

|
||||||
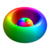
| ℓ = 1 | 3 s |

|

|
|
|||||
| ℓ = 2 | 3 d |

|

|

|

|

|
|||
| n = 4 | ℓ = 0 | 4 sek |

|
||||||
| ℓ = 1 | 4 s |

|

|

|
|||||
| ℓ = 2 | 4 d |

|

|

|

|

|
|||
| ℓ = 3 | 4 f |

|

|

|

|

|

|

|
|
| n = 5 | ℓ = 0 | 5 s |

|
||||||
| ℓ = 1 | 5 s |

|

|

|
|||||
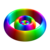
| ℓ = 2 | 5 d |

|

|

|

|
|
|||
| n = 6 | ℓ = 0 | 6 s |

|
||||||
| ℓ = 1 | 6 s |

|

|

|
|||||
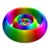
| ℓ = 2 | 6 d |
|

|

|

|

|
|||
Farverne på overfladerne vist ovenfor angiver tegnet på de virkelige og imaginære dele af bølgefunktionen (disse farver er vilkårlige og afspejler ikke en konvention):
| Bølgefunktion | Virkelig del | Imaginær del |
|---|---|---|
| Positiv værdi | Blå | Rød |
| Negativ værdi | Gul | Grøn |
Disse beregninger indebærer valget af en privilegeret akse - for eksempel z- aksen i kartesiske koordinater - og en privilegeret retning på denne akse: det er det, der gør det muligt at definere tegnet på det magnetiske kvantetal m ℓ . Denne model er derfor nyttigt med systemer, der deler denne symmetri, som i tilfældet med den Stern og Gerlach eksperiment , hvor atomer af sølv udsættes for en lodret uensartet magnetfelt .
Ægte orbitaler
Et atom, der er placeret i et krystallinsk fast stof, udsættes for flere præferenceakse, men ingen præferentiel orientering på disse akser. I stedet for at opbygge et sådant atoms atomorbitaler fra radiale funktioner og en enkelt sfærisk harmonisk bruger vi generelt lineære kombinationer af sfæriske harmoniske valgt, så deres imaginære del ophæves., Hvilket giver ægte harmoniske . Det er disse egentlige orbitaler, der generelt bruges til at visualisere atomorbitaler.
I reelle hydrogenoid orbitaler , for eksempel, n og ℓ har samme betydning på deres komplekse modstykke , men m ℓ er ikke længere et gyldigt kvantetal , selv om dets modul er. De faktiske hydrogen p- orbitaler er for eksempel givet ved:
hvor , og .
Ligningerne for p x og p y orbitaler afhænger af den fasekonvention, der er valgt for sfæriske harmoniske. De tidligere ligninger antager, at de sfæriske harmoniske er defineret af Ym
ℓ(θ, φ) = N e i m φ Pm
ℓ(cosθ) . Imidlertid er nogle gange en fasefaktor (–1) m inkluderet, som har den virkning, at p x orbital svarertil en forskel i harmoniske, og p y orbitaltil en sum af harmoniske.
| Kvantumtal | Undercoat | Modul | m ℓ | af det magnetiske kvantetal | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Vigtigste | Azimuthal | 0 | 1 | 2 | 3 | ||||
| n = 1 | ℓ = 0 | 1 s |
 1s |
||||||
| n = 2 | ℓ = 0 | 2 sek |
 2s |
||||||
| ℓ = 1 | 2 s |
 2p z |
 2p x |
 2p y |
|||||
| n = 3 | ℓ = 0 | 3 sek |
 3s |
||||||
| ℓ = 1 | 3 s |
 3p z |
 3p x |
 3p y |
|||||
| ℓ = 2 | 3 d |
 3d z 2 |
 3d xz |
 3d yz |
 3d xy |
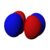 3d x 2 –y 2 |
|||
| n = 4 | ℓ = 0 | 4 sek |
 4s |
||||||
| ℓ = 1 | 4 s |
 4p z |
 4p x |
 4p y |
|||||
| ℓ = 2 | 4 d |
 4d z 2 |
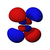 4d xz |
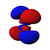 4d yz |
 4d xy |
 4d x 2 –y 2 |
|||
| ℓ = 3 | 4 f |
 4f z 3 |
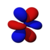 4f xz 2 |
 4f yz 2 |
 4f xyz |
 4f z (x 2 –y 2 ) |
 4f x (x 2 –3y 2 ) |
 4f y (3x 2 –y 2 ) |
|
| n = 5 | ℓ = 0 | 5 s |
 5s |
||||||
| ℓ = 1 | 5 s |
 5p z |
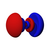 5p x |
 5p y |
|||||
| ℓ = 2 | 5 d |
 5d z 2 |
 5d xz |
 5d yz |
 5d xy |
 5d x 2 –y 2 |
|||
| n = 6 | ℓ = 0 | 6 s |
 6s |
||||||
| ℓ = 1 | 6 s |
 6p z |
 6p x |
 6p y |
|||||
| ℓ = 2 | 6 d |
 6d z 2 |
 6d xz |
 6d yz |
 6d xy |
 6d x 2 –y 2 |
|||
| n = 7 | ℓ = 0 | 7 s |
 7s |
||||||
I gengivelsen ovenfor angiver farven tegn på bølgefunktionen, som er positiv i rødt og negativt i blåt.
Atomorbitalers geometri
Formålet med grafiske repræsentationer af orbitaler er at vise de områder af rummet, at elektronerne i en atombane har en vis sandsynlighed for at besætte. Disse modeller kan ikke repræsentere hele regionen, hvor elektronen sandsynligvis vil være placeret, fordi der i kraft af elektronens kvanteegenskaber er en ikke-nul sandsynlighed for at finde den næsten hvor som helst i elektronrummet omkring atomet. Derfor repræsenterer disse repræsentationer isosurfaces, på hvilke sandsynlighedstætheden | ψ (r, θ, φ) | 2 er konstant, og inden for hvilken sandsynligheden for tilstedeværelsen af elektronen er lig med en given værdi, for eksempel 90%. Skønt | ψ | 2 er aldrig negativ , vi angiver generelt tegnet på bølgefunktionen ψ (r, θ, φ) .
Det er også muligt at repræsentere funktionen ψ og dens fase snarere end ψ 2, der indikerer sandsynlighedstætheden, men ikke har nogen fase. Repræsentationerne af | ψ (r, θ, φ) | 2 har tendens til at have mindre sfæriske og smallere lapper end dem af ψ (r, θ, φ) , men de to repræsentationer har det samme antal lapper med det samme rumlige arrangement og kan genkendes fra hinanden.
Fortolkning af kvantetal
Generelt bestemmer det vigtigste kvantetal n størrelsen og energien af orbitalen for en given atomkerne : jo mere n stiger, jo mere stiger orbitalen. Men når man sammenligner de orbitaler flere grundstoffer , jo højere de atomare tal Z stiger, jo mere atomare orbitaler kontrakt fordi elektriske ladning samlede kerne også stiger med Z . Som et resultat forbliver størrelsen af atomer relativt konstant på trods af akkumulering af elektroniske lag .
Stadig generelt azimutale kvantetal ℓ bestemmer formen af den orbitale, mens det magnetiske kvantetal m ℓ bestemmer sin orientering i rummet. Imidlertid bestemmer antallet m ℓ også formen på nogle komplekse orbitaler . Sættet med orbitaler svarende til et givet par ( n , ℓ ) fylder rummet så symmetrisk som muligt med et stigende antal lapper og knuder.
S orbitaler
S orbitaler , identificeret ved ℓ = 0 , er repræsenteret af kugler. For n = 1 er sandsynlighedstætheden højere i midten og falder udad, men for n = 2 eller mere danner sandsynlighedsdensiteten inde i hver s orbital en radial bølgestruktur, hvor alternative koncentriske lag med høj sandsynlighed og lavere sandsynlighed.
De s orbitaler er de eneste, at forelægge en anti-knude, dvs. en region, hvor den bølge funktion har en højt modul, i midten af kernen. P , d , f og efterfølgende orbitaler har vinkelmoment og undgår kernen, hvor de præsenterer en knude.
P-, d- og f-orbitaler
De tre p- orbitaler for n = 2 har form af to ellipsoider, der deler et tangenspunkt på atomkernens niveau . Denne form kaldes undertiden som håndvægte . De er orienteret vinkelret i forhold til hinanden som en funktion af deres magnetiske kvantetal m ℓ .
Fire af de fem d orbitaler for n = 3 har lignende former, hver med fire pæreformede lapper, idet disse lapper er ortogonalt tangente to og to, idet disse fire lober er i samme plan . Tre af disse orbitaler, navngivet d xy , d yz og d xz , er justeret på xy- , yz- og xz- planerne - lapperne er placeret mellem hvert af de tre par koordinatakser - mens den fjerde, der hedder d x 2 - y 2 , er på linje med selve x- og y- akserne .
Den femte orbital d , opkaldt d z 2 , svarende til m ℓ = 0 , består af tre regioner, hvor sandsynligheden er høj: to pæreformet regioner på hver side af kernen langs aksen z og en torus omkring kerne i xy- planet .
-
Orbital d xy
-
Orbital d yz
-
Orbital d xz
-
Orbital d x 2 - y 2
-
D z orbital 2
Der er syv f orbitaler og har mere komplekse former end d orbitaler .
Formen på atomorbitaler af hydrogenatomer er afledt af sfæriske harmoniske . Disse former er ikke unikke, og mange lineære kombinationer er gyldige, såsom en transformation til kubiske harmoniske (in) . Det er også muligt at generere sæt af funktioner, der producerer d- orbitaler, der alle har samme form, såsom p- orbitaler .
Det skal huskes, at alle disse orbitaler, præsenteret individuelt som en del af modeller fra brintatomer, eksisterer samtidigt i virkelige atomer.
Analogi med vibrationer fra en membran
Det er muligt at repræsentere i to dimensioner betydningen af de forskellige tredimensionelle former for atomare orbitaler ved hjælp af vibrationstilstande for en cirkulær membran, for eksempel af en trommes hud . I denne repræsentation er afstanden fra centrum af membranen ækvivalent med elektronens afstand fra atomkernen , og størrelsen af afvigelsen fra membranens ligevægtsplan repræsenterer densiteten af tilstedeværelsen af elektronen. . Denne analogi er ikke perfekt, især fordi spændingen i en fysisk membran som en trommes hud har den virkning, at den afrunder de bølger, der krydser den, men den tegner sig for flere kvalitative egenskaber ved atomorbitaler, for eksempel for eksempel det faktum, at kun s orbitaler har en antiknude (maksimal amplitude) i midten, mens alle de andre har en knude (nul amplitude) på dette sted, eller for at visualisere den geometriske fordeling af loberne af orbitalerne af rang Student:
- De første 9 vibrationsmetoder i en trommes hud
-
Mode u 01 , analog med 1s
-
Mode u 02 , analog med 2s
-
Mode u 03 , analog med 3s
-
Mode u 11 , analog med 2p
-
Mode u 12 , analog med 3p
-
Mode u 13 , analog med 4p
-
U 21- tilstand , analog med 3d
-
Mode u 22 , analog med 4d
-
Mode u 23 , analog 5d
Den reelle del af bølgefunktionen af s- og p -atomorbitaler repræsenteret på samme måde for forskellige værdier af n og ainsi er således analog med de forskellige vibrationsmetoder for et tromlehoved:
- Virkelig del af bølgefunktionen i s- og p-orbitaler
-
1s orbital
-
2s orbital
-
orbital 3s
-
2p orbital
-
orbital 3p
-
orbital 4p
Ansøgninger
I atomfysikken , spektrallinier svarer til elektroniske overgange som følge af overgangen fra den ene kvantetilstand af atomet til en anden. Disse tilstande er defineret af et sæt kvantetal, der generelt er forbundet med en elektronisk konfiguration , det vil sige med fordelingen af elektroner mellem de forskellige atomorbitaler. Den elektroniske konfiguration af neon i jordtilstand er således 1s 2 2s 2 2p 6 , opsummeret i udtrykket1S
0.
Atomiske orbitaler er et nøglekoncept til visualisering af excitationsprocesserne ved oprindelsen af elektroniske overgange . For eksempel er det muligt at relatere en given overgang til excitation af en elektron, der passerer fra et besat orbital af primære kvantetal n = n 1 til en ledig orbital af kvantetallet n = n 2 . Således er en elektrons energi i et hydrogenoidatom lig med:
,vi kan udlede Rydberg formel giver bølgetallet forbundet med en elektronisk overgang fra en n = n 1 orbital til en n = n 2 orbital i en hydrogenoid atom, hvor λ er bølgelængden , R ∞ den Rydberg konstant , og Z eff den effektiv nuklear ladning (in) :
Anvendt på hydrogen , den formel, der anvendes til beregning af emissionslinierne i spektret af hydrogen :
Det skal dog huskes, at de således definerede orbitaler er monoelektroniske bølgefunktioner, der vedrører hydrogenatomer . Da atomer generelt ikke er hydrogenoid, er de tværtimod polyelektroniske, så denne tilnærmelse er en måde at forenkle modelleringen af den elektroniske konfiguration af atomer på, men kan have grænser, især til beskrivelse af store atomer.
Noter og referencer
- (i) David Griffiths, Introduktion til kvantemekanik , 1995 Prentice Hall, pp. 190–191 . ( ISBN 0-13-124405-1 )
- (en) Ira Levine, (2000). Quantum Chemistry , 5 th edition, 2000, Prentice Hall, pp. 144–145 . ( ISBN 0-13-685512-1 )
- (i) Keith J. Laidler, John H. Meiser, Physical Chemistry , 1982, Benjamin / Cummings, s. 488 . ( ISBN 0-8053-5682-7 )
- (i) Peter Atkins, Julio de Paula, Ronald Friedman, Quanta, Matter og Forandring: En Molekylær tilgang til fysisk kemi , 2009, Oxford University Press, s. 106 . ( ISBN 978-0-19-920606-3 )
- Roger Penrose , Discovering the Laws of the Universe: The Wonderful History of Mathematics and Physics , 2004.
- (i) Ira Levin, Kvantekemi , 7 th udgave, Pearson Education, 2014, pp. 141–142 . ( ISBN 0-321-80345-0 )
- (i) Miguel A. Blanco, Mr. Flórez og Mr. Bermejo , " Evaluering af rotation matricer i grundlag af de faktiske sfæriske harmoniske " , Journal of Molecular Structure: THEOCHEM , vol. 419, n knogler 1-3, 8. december 1997, s. 19-27 ( DOI 10.1016 / S0166-1280 (97) 00185-1 , læs online )
- (i) Albert Messias, Kvantemekanik: to bind bundet som en 1999 Mineola, Dover, New York. ( ISBN 978-0-486-40924-5 )
- Claude Cohen-Tannoudji, Bernard Dui, Franck Laloë, Quantum Mechanics , Science Education Collection, Herman, Paris, 1973. Bibcode : 1973mequ.book ..... C
- (i) Richard E. Powell , " The five d orbitals equivalent " , Journal of Chemical Education , bind. 45, nr . 1, Januar 1968, s. 45 ( DOI 10.1021 / ed045p45 , Bibcode 1968JChEd..45 ... 45P , læs online )
- (i) George E. Kimball , " Directed Valencia " , The Journal of Chemical Physics , vol. 8, nr . 2 Februar 1940, s. 188-198 ( DOI 10.1063 / 1.1750628 , Bibcode 1940JChPh ... 8..188K , læs online )
Se også
Relaterede artikler
- Schrödingers model
- Brintatom
- Sfærisk harmonisk
- Molekylær orbital
Eksternt link
- Aktiviteter, applikationer og forskning relateret til atomorbitaler og kvantificering (Paris Sud University)







