Hyponitrous syre
| Hyponitrous syre | |
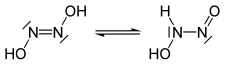 Hyponitrous syre tautomerer |
|
| Identifikation | |
|---|---|
| IUPAC navn | diazenediol |
| Synonymer |
Hyponitritis |
| N o CAS | |
| PubChem | 61744 |
| ChEBI | 14428 |
| Kemiske egenskaber | |
| Brute formel |
H 2 N 2 O 2 [isomerer] |
| Molar masse | 62,0281 ± 0,0011 g / mol H 3,25%, N 45,16%, O 51,59%, |
| Enheder af SI og STP, medmindre andet er angivet. | |
Den hyponitrous syre er en kemisk forbindelse med formlen H 2 N 2 O 2. Dens strukturelle formel kan skrives som HON = NOH , dimer af nitroxyl HNO og isomer af nitramide H 2 N - NO 2. Det ser ud som et hvidt krystallinsk fast stof, eksplosivt, når det er tilstrækkeligt dehydreret. I vandig opløsning er hyponitrøs syre en svag syre ( pK 1 = 7,21 , pK 2 = 11,54 ). Det nedbrydes til lattergas N 2 Oog i vand H 2 Omed en halveringstid på 16 dage ved pH = 1 til 3 :
H 2 N 2 O 2→ H 2 O+ N 2 O.Da denne reaktion ikke er reversibel, kan lattergas ikke betragtes som anhydrid af hyponitronsyre.
Hyponitrous syre danner to serier af salte: syrehyponitritter, der indeholder [HON = N] - anionen , og hyponitritter, der indeholder [ON = NO] 2− anionen . Sidstnævnte kan fremstilles i vandig opløsning ved to metoder. De første anvendelser organiske nitritter til dannelse af natrium -saltet af hyponitrous syre:
R ONO + NH 2 OH+ 2 EtONa → Na 2 N 2 O 2+ R OH + 2 EtOH .En anden fremgangsmåde er reduktionen af natriumnitrit NaNO 2 at give sølvsaltet:
2 NaNO 2+ 4 NaHg + 2 H20+ 2 AgNO 3→ Ag 2 N 2 O 2+ 2 NaNO 3+ 4 NaOH + 4 Hg .Tilsætning af Ag + -ioner forårsager udfældning af sølvhyponitrit Ag 2 N 2 O 2. Den hyponitrøse syre frigives derefter ved virkningen af hydrogenchlorid HCI vandfri :
Ag 2 N 2 O 2+ 2 HCI → H 2 N 2 O 2+ 2 AgCl .Den hyponitrøse syre kan antage en cis- eller trans- konfiguration ; natrium hyponitrite hydrat Na 2 N 2 O 2 5H 2 O, som er fast, har en trans- konfiguration , ligesom den frie syre. Den cis- formen kan opnås som natrium hyponitrite Na 2 N 2 O 2ved opvarmning natriumoxid Na 2 Oi nærvær af lattergas N 2 O gasformig.
Noter og referencer
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .