Mælkesyre
| Mælkesyre | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
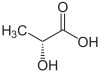
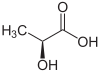
| R enantiomer af mælkesyre (øverst, venstre), S-mælkesyre (øverst, højre) og tredimensionel struktur af S-mælkesyre (bunden). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikation | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC navn | 2-hydroxypropansyre | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS |
(RS) (S+ eller L) (R- eller D) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.017 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EF | 200-018-0 209-954-4 ( RS ) 201-196-2 ( S ) 233-713-2 ( R ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-kode | G01 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E270 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2611 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILE |
CC (O) C (= O) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = InChI = 1 / C3H6O3 / c1-2 (4) 3 (5) 6 / h2,4H, 1H3, (H, 5,6) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Udseende | farveløs til gul tyktflydende væske eller farveløs til gul krystaller (DL) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formel |
C 3 H 6 O 3 [isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar masse | 90,0779 ± 0,0037 g / mol C 40%, H 6,71%, O 53,29%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | 3,86 ( 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusion |
D / L : 16,8 ° C L : 53 ° C D : 53 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kogning | 122 ° C ( 12 mmHg ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighed | let jordet. i ether ; insol. i chloroform , petroleumsether , carbondisulfid |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blandbarhed | blandbar med vand , alkohol , glycerol og furfuraldehyd , en sol. alkohol-ether | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumenmasse | 1,248 5 g cm −3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | 110 ° C (lukket kop) (DL) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brydningsindeks | 1,4414 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Roterende kraft |
−2,6 ° ( 80 g l −1 , R) + 2,6 ° ( 25 g l −1 , S) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mælkesyre: Produkt ikke klassificeretKlassificeringen af dette produkt er endnu ikke valideret af Toxicological Directory Service Disclosure med 1,0% i henhold til listen over ingredienser Mælkesyre, (dl-): E,  E : Stærkt surt ætsende materiale (beregnet pH = 1,9 for en 9% opløsning) Offentliggørelse ved 1,0% i henhold til listen over ingredienser |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Direktiv 67/548 / EØF | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Xi Symboler : Xi : Lokalirriterende R-sætninger : R38 : Irriterer huden. R41 : Risiko for alvorlig øjenskade. S-sætninger : S26 : I tilfælde af kontakt med øjnene, skylles straks med rigeligt vand og læge kontaktes. S39 : Bær øjen- / ansigtsbeskyttelse. R-sætninger : 38, 41, S-sætninger : 26, 39, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Relaterede forbindelser | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isomer (er) | 3-hydroxypropansyre | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheder af SI og STP, medmindre andet er angivet. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den mælkesyre er en organisk syre , der spiller en rolle ved forskellige processer biokemisk . Den lactat er den konjugerede base af denne syre (dvs. den ioniserede form af mælkesyre). I modsætning til hvad navnet antyder, er mælkesyre ikke kun til stede i den mælk, hvorfra den først blev ekstraheret af den svenske kemiker Carl Wilhelm Scheele . Det findes også i vin , visse frugter og grøntsager , i dyreceller, hvor det adskilles og er til stede i form af lactat såvel som i visse præparater ( surkål osv.).
Mælkesyre er en α-hydroxysyre , dens rå formel er C 3 H 6 O 3 og dets struktur afspejles i dets systematiske navn, 2-hydroxypropansyre.
Kemi
Den atom af carbon 2 bærer gruppen hydroxy er asymmetrisk gør molekylet af mælkesyre chirale . Det er derfor i form af to enantiomerer :
- ( R ) -mælkesyre eller D (-) - mælkesyre;
- ( S ) -mælkesyre eller L (+) - mælkesyre.
I opløsning kan carboxylgruppen -COOH miste en H + ion . Således mælkesyre (C 3 H 6 O 3 ) omdannes til lactat ion : CH 3 CHOHCOO -.
På den anden side, i musklen, to H + ioner tilsættes til pyruvat (C 3 H 3 O 3 ) til dannelse af lactat (C 3 H 5 O 3 2+ ) .
Mælkesyre er opløselig i vand og anses for at være en svag syre ( pKa = 3,90), dvs. dissociationsreaktionen i vand er ikke komplet:
CH 3 CHOHCOOH+ H 2 O⇄ CH 3 CHOHCOO -+ H 3 O +Mælkesyre findes derfor både i opløsning og dens basiske form, lactationen, i varierende proportioner afhængigt af pH .
Muskuløs indsats og mælkesyregæring
Mælkesyre er især et af nøgleprodukterne i produktion af energi i muskler. Cellular respiration (forbrug af sukker for at producere energi) kan opdeles i to hovedfaser, den første er glykolyse , den cytoplasmatiske del af processen, der finder sted i fravær af ilt. Det leverer pyruvat, som leverer den anden, mitokondrie del af cellulær respiration ( Krebs cyklus og oxidativ fosforylering), hvilket resulterer i reduktion af ilt i vand. I den ene ende af kæden oxideres glukose , og i den anden reduceres ilt. Den frigjorte energi genvindes af cellen.
Hvis iltforsyningen er større end sukkerforbruget, forbruges al den producerede pyruvinsyre straks i den mitokondrie del.
Hvis sukkerforbruget bliver større end iltforsyningen (intens indsats), reduceres en del af den pyruvinsyre, der produceres i den første del af processen, til mælkesyre, hvilket gør det muligt at fortsætte den oxidative cyklus af glykolyse. Det er en gæring . Den mitokondrie del er mættet, og energiudbyttet reduceres kraftigt. Imidlertid stilles denne teori om sukkerforbrug / iltforbrug tvivl. Hvad angår det anaerobe energiudbytte, ser det ud til at være forholdsmæssigt højere end det aerobe energiudbytte, i modsætning til hvad der er almindeligt accepteret.
Laktat passerer cellemembranen for at komme ind i blodbanen. Den lever , skeletmuskulatur, hjerte og hjerne kan bruge denne substrat for energi. Leveren genbruger den i det, der kaldes glukoneogenese, der vil syntetisere glukose, mens en anden del oxideres af myokardiet såvel som af musklerne, der er mindre krævet af sportslig indsats. Laktat metaboliseres ca. en time efter træning uden nogen sportsaktivitet efter træning, dvs. godt inden muskelstivhed , som det derfor ikke er ansvarlig for.
Bakteriel gæring
Der er to hovedtyper af bakteriel gæring, der producerer mælkesyre: i vin og mejeriprodukter.
- I vin er dette malolaktisk gæring : æblesyre, der naturligt er indeholdt i vin, opdeles i mælkesyre under påvirkning af bakterier.
- I mælk og mejeriprodukter kommer mælkesyre fra nedbrydning af lactose af bakterier. Jo friskere mælken er, jo mindre mælkesyre indeholder den. Mælkesyrekoncentrationen i mælk udtrykkes i Dornic-grad (° D): 1 ° D svarer til 0,1 g mælkesyre pr. Liter mælk. En frisk mælk indeholder fra 15 til 18 ° D , det vige tilbage til 60 - 70 ° D .
De organismer, der er ansvarlige for udseende af mælkesyre, er lactobaciller . Når de opererer i munden, kan den producerede mælkesyre føre til hulrum .
Denne mælkesyregæringsmetode forekommer også på bestemte grøntsager ( kål = surkål og andre såkaldte “lacto-fermenterede” grøntsager). Mælkesyre anvendes som AHA i kosmetik er ikke udvundet fra mælk, men for eksempel sukker fra roer , blåbær , etc.
Anvendelser
Kilde.
Direkte i menneskelig mad
Mælkesyre anvendes i fødevareindustrien som et tilsætningsstof (E270) som en antioxidant , syrningsmiddel eller smagsforstærker . Mælkesyre er også til stede i form af salte: natrium ( E325 ), kalium ( E326 ) og calcium ( E327 ) salt . Disse salte er i pulverform og er også opløselige i vand. Det virker som et bakteriostatisk middel, især på patogene bakterier såsom salmonella (eller listeria ) og også en depressiv virkning på vandaktivitet .
Ifølge forskning, der fandt sted i Quebec, ser det ud til, at mælkesyre er et af de mest naturlige midler til at forhindre blærekræft , men også hudens .
I kosmetik
Denne syre bruges undertiden som en del af et æstetisk skræl, især til farvet hud (intervaller af æstetiske misfarvningsprodukter er sammensat af mælkesyre); denne syre skal dog påføres under opsyn af en hudlæge og under doseringsbetingelser og specifik fortynding i henhold til patientens hudtone.
Som et dekontamineringsmiddel og rengøringsmiddel
Mælkesyre blev fremtrædende i vaskemiddelindustrien efter 2000'erne. Det er et godt afkalkningsmiddel , sæbefjerner og antibakterielt middel. Det er også økonomisk fordelagtigt og er en del af en tendens til ingredienser, der er mere sikre og mere naturlige for miljøet. Mælkesyre anvendes derfor i USA til bakteriedekontaminering af slagtekroppe på slagterier . Den oksekød omfattet af denne praksis først forbudt af EU , fordi brugen af mælkesyre er her for at korrigere en mangel på hygiejne forbindelse med en lemfældig skovdrift. Som en del af kompromiset om import af nordamerikansk oksekød til Europa efter embargoen med hormon oksekød blev denne anvendelse endelig godkendt efter offentliggørelsen af den europæiske forordning 101/2013 fra startenFebruar 2013. I Europa kan denne praksis principielt spores.
Forløber af plast
Mælkesyre polymeriseres for at give polymælkesyre (PLA), et biologisk nedbrydeligt plastmateriale, der især anvendes til 3D-printere , til mademballage og til kirurgi .
Historisk
Mælkesyre blev opdaget af Carl Wilhelm Scheele (1742-1786).
Handle
Frankrig er i 2014 en nettoimportør af mælkesyre ifølge fransk told. Den gennemsnitlige importpris pr. Ton var € 1.400.
Noter og referencer
- Mælkesyre, sikkerhedsark (er) fra det internationale program for kemisk sikkerhed , hørt den 9. maj 2009
- " CAS-registreringsnummer: 50-21-5 " , på ntp.niehs.nih.gov (adgang 14. februar 2010 )
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- (da) JG Speight og Norbert Adolph Lange, Lange's Handbook of Chemistry , New York, McGraw-Hill ,2005, 16 th ed. , 1623 s. ( ISBN 978-0-07-143220-7 , LCCN 84643191 ) , s. 2.289
- (i) Carl L. kæberne, Handbook of Termodynamiske diagrammer , Vol. 1, Huston, Texas, Gulf Pub. Co.,1996( ISBN 978-0-88415-857-8 , LCCN 96036328 )
- (en) Maryadele J. O'Neil, Ann Smith, Patricia E. Heckelman og Susan Budavari, The Merck Index: An Encyclopedia of Chemicals, Drugs and Biologicals , United States, Merck,2001, 13 th ed. , 2564 s. ( ISBN 978-0-911910-13-1 )
- " Mælkesyre " i databasen over kemikalier Reptox fra CSST (Quebec-organisation med ansvar for sikkerhed og sundhed på arbejdspladsen), adgang til 24. april 2009
- " Mælkesyre, (dl-) " i databasen over kemiske produkter Reptox fra CSST (Quebec-organisation med ansvar for sikkerhed og sundhed på arbejdspladsen), åbnet den 25. april 2009
- " Mælkesyre " , på societechimiquedefrance.fr (adgang til 18. september 2019 )
- (i) George A. Brooks , " The Science og Oversættelse af laktat Shuttle Theory " , Cell Metabolism , Vol. 27, nr . 4,april 2018, s. 757–785 ( ISSN 1550-4131 , DOI 10.1016 / j.cmet.2018.03.008 , læst online , adgang til 30. maj 2018 )
- Luc Léger , Georges Cazorla , Cyril Petibois og Laurent Bosquet , ” Laktat og øvelse: myter og realiteter ”, Staps , vol. Nr. 54, nr . 1,2001, s. 63–76 ( ISSN 0247-106X , DOI 10.3917 / sta.054.0063 , læst online , adgang 30. maj 2018 )
- Pascal Prevost, " Courbatures " , på Sciensport ,2006(adgang til 8. januar 2008 )
- UN Wiesmann , S. DiDonato og NN Herschkowitz , " Effekt af klorquin på dyrkede fibroblaster: frigivelse af lysosomale hydrolaser og inhibering af deres optagelse ", Biokemisk og biofysisk forskningskommunikation , bind. 66, nr . 4,27. oktober 1975, s. 1338-1343 ( ISSN 1090-2104 , PMID 4 , læse online , adgang 1 st april 2018 )
- C. Chêne (2002), Organiske syrer [PDF] , Technological Resource Center for Agro-Food Enterprises, http://www.adrianor.com .
- http://sante.canoe.com/channel_health_news_details.asp?channel_id=2001&relation_id=3483&news_channel_id=2001&news_id=3695
- Spørgsmål og svar i senatet
- " Indikator for import / eksporthandel " om tolddirektoratet. Angiv NC8 = 29181100 (adgang til 7. august 2015 )
Se også
Relaterede artikler
- Fødevaretilsætningsstof
- Aroma
- Mælk og vin
- Polymælkesyre , biologisk nedbrydelig polymer
eksterne links
- [video] "Molecular Mojito - Molecular Cocktail - Molecular Cuisine - Molecular Gastronomy" på YouTube ,15. november 2016.
Bibliografi
- Ackerman SH og Sachar EJ (1974), The lactate theory of anxiety: a review and reevaluation , Psychosom. Med. , Januar-februar 1974, 36 (1), 69-81.





