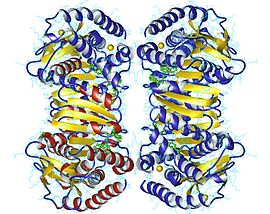
Malatdehydrogenase
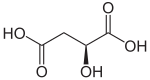
Den malatdehydrogenase ( MDH ) er en oxidoreduktase af Krebs 'cyklus , der katalyserer den reaktion :
|
+ NAD + NADH + H + + |

|
| L- Mate | Oxaloacetat |
Dette enzym er involveret i flere vigtige metaboliske veje , herunder Krebs-cyklussen .
Malatdehydrogenase| EF-nr. | EC |
|---|---|
| CAS-nummer |
| IUBMB | IUBMB-post |
|---|---|
| IntEnz | IntEnz-visning |
| BRENDA | BRENDA indgang |
| KEGG | KEGG-indgang |
| MetaCyc | Metabolisk vej |
| PRIAM | Profil |
| FBF | Strukturer |
| GÅ | AmiGO / EGO |
Isoformer
De prokaryoter har en enkelt form, men alle eukaryoter har mindst to isoformer , en i cytosolen og en anden i mitochondriematricen . De svampe og planter har også en bestemt form for glyoxisome , som er involveret i glyoxylat cyklus . Planterne har en fjerde særlig form til chloroplaster og operativ til NADP + , den malatdehydrogenase NADP + ( EF ) , som er involveret i Calvin cyklussen , den fiksering af carbon i C 4og krassulaceansyremetabolisme .
Endelig har archaea en malatdehydrogenase tæt beslægtet med lactatdehydrogenase .
Biokemi
Malatdehydrogenase forekommer først i Krebs cyklus , hvor hun oxid den L -malat i oxaloacetat . Sidstnævnte kan igen kondenseres med acetyl-CoA ved citratsyntase for at indlede en ny runde af Krebs-cyklussen.
Det er også involveret i gluconeogenese i dets mitokondrie og cytosoliske former . Den pyruvat kan faktisk omdannes til oxaloacetat ved pyruvatcarboxylase , som er reduceret med L -malat ved malatdehydrogenase mitokondrie mens den kører i den modsatte retning af Krebs cyklus: den -malat kan efterlade mitokondrier at nå cytosolen og der bliver igen oxideres til oxaloacetat af cytosolisk malatdehydrogenase. Oxaloacetatet omdannes derefter til phosphoenolpyruvat med phosphoenolpyruvat-carboxykinase (PEPCK).
Den mitokondrielle form er også involveret i malat-aspartat-shuttle , der er afgørende for cellulær respiration .
Struktur og katalytisk mekanisme
Malatdehydrogenase forekommer i de fleste levende ting som et homodimert protein, der i struktur er nært beslægtet med lactatdehydrogenase . Det er et stort molekyle, hvis underenheder har en masse på 30 til 35 kDa . Den peptidsekvensen af disse enzymer har tendens til at vise, at de har afveget i to fylogenetiske grupper : de mitokondriske isoenzymer på den ene side og de cytosoliske og chloroplast- isoenzymer på den anden. Disse observationer understøtter den endosymbiotiske teori om, at mitokondrier og kloroplaster udvikles inde i eukaryote celler fra forfædres prokaryoter . Derudover svarer peptidsekvensen for malatdehydrogenase fra archaea til den for lactatdehydrogenase som den for malatdehydrogenase fra andre organismer, som illustrerer et forhold mellem lactatdehydrogenase og malatdehydrogenase.
Hver underenhed af malatdehydrogenasedimerer har to forskellige domæner, der varierer i struktur og funktionalitet. Hvert domæne vedtager en parallel β-arkstruktur med fire β-ark og en α-helix omfattende det centrale NAD + -bindingssted . Underenhederne er bundet sammen af adskillige hydrogenbindinger og hydrofobe interaktioner.
Det aktive sted for malatdehydrogenase er et hydrofobt hulrum, der er inkluderet i proteinet, hvori der er specifikke bindingssteder til substratet og dets coenzym , NAD + . I den aktive tilstand gennemgår enzymet en konformationsændring, som omslutter substratet for at minimere dets eksponering for opløsningsmidlet og placerer tæt på substratet resterne af aminosyrer katalytiske nøgler. De tre rester, der omfatter en katalytisk triade, er på den ene side His195 og Asp168 , som begge fungerer som et protonoverføringssystem, og resterne Arg102 , Arg109 og Arg171 , som binder substratet. Kinetiske undersøgelser har vist, at den enzymatiske aktivitet af malatdehydrogenase er sekventeret: NAD + / NADH er bundet før substratet.
Noter og referencer
- Værdierne af massen og antallet af rester, der er angivet her, er værdierne for proteinforløberen, der er resultatet af translationen af genet , før posttranslationsmodifikationer og kan afvige markant fra de tilsvarende værdier til det funktionelle protein .
- (in) P. Minárik N. Tomášková, M. og M. Kollárová Antalík , " malatdehydrogenase - struktur og funktion " , General Physiology and Biophysics , Vol. 21, nr . 3, September 2002, s. 257-265 ( PMID 12537350 , læs online )
- (in) RA Musrati M. Kollárová, N. og D. Mernik Mikulášová , " malatdehydrogenase: distribution, funktion og egenskaber " , General Physiology and Biophysics , Vol. 17, nr . 3, September 1998, s. 193-210 ( PMID 9834842 , læs online )
- (i) Lee McAlister-Henn , " Evolutionary Relationships blandt de malatdehydrogenase " , Trends in Biochemical Sciences , vol. 13, nr . 5, Maj 1988, s. 178-181 ( PMID 3076279 , DOI 10.1016 / 0968-0004 (88) 90146-6 , læs online )
- (i) Fabrice Ash Lad, Jadwiga Chroboczek Giuseppe Zaccai, Henryk Eisenberg og Moshe Mevarech , " Kloning, sekventering og ekspression i Escherichia coli af genet, der koder for malatdehydrogenase af den ekstremt halofile archaebacterium Haloarcula marismortui " , Biochemistry , vol. 32, nr . 16, 27. april 1993, s. 4308-4313 ( PMID 8476859 , DOI 10.1021 / bi00067a020 , læs online )
- (in) Michael D. Hall, David G. Levitt og Leonard J. Banaszak , " Crystal structure of Escherichia coli malate dehydrogenase: A complex of the apoenzyme and citrate at 1 - 87 Å resolution " , Journal of Molecular Biology , bind. 226, nr . 3, 5. aug. 1992, s. 867-882 ( PMID 1507230 , DOI 10.1016 / 0022-2836 (92) 90637-Y , læs online )
- (i) Victor S. Lamzin Zbigniew Dauter og Keith S. Wilson , " Dehydrogenering Bag spejlet " , Nature Structural Biology , bd. 1, nr . 5, Maj 1994, s. 281-282 ( PMID 7664032 , DOI 10.1038 / nsb0594-281 , læs online )
- (in) Thomas B. Shows, Verne Chapman og Frank H. Ruddle , " Mitochondrial malate dehydrogenase and malic enzym: Mendelian inherited electrophoretic variants in the mouse " , Biochemical Genetics , bind. 4, n o 6, December 1970, s. 707-718 ( PMID 5496232 , DOI 10.1007 / BF00486384 , læs online )