Kvælstofperoxid
| Kvælstofperoxid | |||
 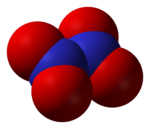 Struktur af nitrogenperoxid. |
|||
| Identifikation | |||
|---|---|---|---|
| IUPAC navn | Kvælstoftetraoxid | ||
| N o CAS | |||
| N o ECHA | 100.031.012 | ||
| N o EF | 234-126-4 | ||
| N o RTECS | QW9800000 | ||
| PubChem | 25352 | ||
| ChEBI | 29803 | ||
| SMILE |
[N +] (= O) ([N +] (= O) [O -]) [O-] , |
||
| InChI |
InChI: InChI = 1S / N2O4 / c3-1 (4) 2 (5) 6 InChIKey: WFPZPJSADLPSON-UHFFFAOYSA-N |
||
| Udseende | farveløs væske | ||
| Kemiske egenskaber | |||
| Brute formel |
N 2 O 4 [Isomerer] |
||
| Molar masse | 92,011 ± 0,0016 g / mol N 30,45%, O 69,55%, |
||
| Fysiske egenskaber | |||
| T ° fusion | −9,3 ° C | ||
| T ° kogning | 21,15 ° C | ||
| Opløselighed | reagerer med vand | ||
| Volumenmasse | 1,45 g · cm -3 til 20 ° C | ||
| Kritisk punkt | 431 K ; 10,1 MPa ; 167 cm 3 · mol -1 | ||
| Termokemi | |||
| Δ vap H ° | 38,12 kJ · mol -1 ( 1 atm , 21,15 ° C ) | ||
| Forholdsregler | |||
| SGH | |||
    Fare H270, H280, H314, H330, P220, P260, P280, P284, P310, P305 + P351 + P338, H270 : Kan forårsage eller intensivere brand; oxidator H280 : Indeholder gas under tryk; kan eksplodere ved opvarmning H314 : Forårsager svære forbrændinger af huden og øjenskader H330 : Dødelig ved indånding P220 : Opbevares / opbevares væk fra beklædning / ... / brændbare materialer P260 : Indånd ikke støv / dampe / gasser / tåger / dampe / aerosoler. P280 : Bær beskyttelseshandsker / beskyttelsestøj / øjenbeskyttelse / ansigtsbeskyttelse. P284 : Bær åndedrætsværn. P310 : Ring omgående til et GIFTINFORMATIONSCENTER eller en læge / læge. P305 + P351 + P338 : Ved øjnene: Skyl forsigtigt med vand i flere minutter. Fjern kontaktlinser, hvis offeret har dem på, og de let kan fjernes. Fortsæt med at skylle. |
|||
| WHMIS | |||
|
Uklassificeret produktKlassificeringen af dette produkt er endnu ikke valideret af Toxicological Directory Service Disclosure med 1,0 % i henhold til listen over ingredienser |
|||
| Transportere | |||
265 : giftig og oxiderende gas (fremmer brand) UN-nummer : 1067 : NITROGEN DIOXIDE; eller DIAZOTE TETROXIDE Klasse: 2.3 Mærkater: 2.3 : Giftige gasser (svarer til grupper, der er betegnet med et stort T, dvs. T, TF, TC, TO, TFC og TOC). 5.1 : Oxiderende stoffer 8 : Ætsende stoffer    |
|||
| Enheder af SI og STP, medmindre andet er angivet. | |||
Den nitrogendioxid eller dinitrogentetroxid , er en kemisk forbindelse med formlen N 2 O 4. Det er en farveløs til gulbrun væske afhængigt af koncentrationen af nitrogendioxid NO 2den indeholder: N 2 O 4er i ligevægt med NO 2, hvoraf det faktisk er en dimer . Det er en meget kraftig, ætsende og giftig oxidant . Også kaldet NTO (fra det engelske kvælstof TetrOxide) i astronautik , kvælstofperoxid er en oxidator, der er meget udbredt, især med hydrazin og dets derivater til dannelse af lagringsbare hypergoliske flydende drivmidler .
Egenskaber og struktur
Strukturen af dette molekyle blev meget diskuteret indtil slutningen af 1940'erne, da vi begyndte at forstå det, ligesom kvælstoftrioxid . N 2 O 4 molekyleer plan med en NN-binding på 178 µm og en NO-binding på 119 µm . I modsætning til NO 2- molekylet, N 2 O 4 dimerer diamagnetisk .
Også i 1940'erne blev det vist, at det i flydende form, i modsætning til ammoniak NH 3eller svovldioxid SO 2, dette medium var ikke befordrende for de uorganiske reaktioner, som oprindeligt skulle antages at være mulige ved ionisering af mediet. Opløselige mineralsalte i denne væske blev ikke fundet på det tidspunkt, og i betragtning af den høje opløselighed af mange organiske forbindelser, kemikere derefter konkluderet, at denne væske havde et ikke-ioniserende karakter og en opførsel, der minder om den for opløsningsmidler. Organisk såsom benzen C 6 H 6.
Under normale temperatur- og trykforhold og under ligevægten mellem nitrogen peroxid N 2 O 4og nitrogendioxid NO 2, er de to arter altid til stede samtidigt, stigningen i temperatur skifter ligevægten af denne endotermiske reaktion mod dioxid ved dissociation af dimeren:
N 2 O 4 2 NO 2 : .DELTA.h = 57,23 kJ · mol -1 .Forberedelse
Nitrogen peroxid fremstilles ved katalyseret oxidation af ammoniak NH 3i vanddamp H 2 Ofor at begrænse temperaturen, hvilket gør det muligt at oxidere nitrogenmonoxid N20 til nitrogendioxid NO 2mens vandet udledes i form af salpetersyre HNO 3 ; den resterende gas er i det væsentlige sammensat af nitrogenperoxid, som derefter er tilstrækkelig til at afkøle.
Astronautisk brug
Kvælstofperoxid er et af de vigtigste drivmidler, der anvendes i dag i rumfremdrift . Det erstattede den første salpetersyre, der blev brugt som forbrænding af drivmidler fra raketmotorer , med brændstof såsom RP-1 , UDMH eller MMH . Motorerne blev beskyttet mod oxidatorens surhed ved tilsætning af 0,6% hydrogenfluorid HF, temmelig dyrt, meget giftigt og farligt at håndtere. Salpetersyre blev erstattet af andre oxidationsmidler, især kvælstofperoxid, så tidligt som i begyndelsen af 1990'erne. Rumskyttere og ballistiske missiler begyndte at bruge det i slutningen af 1950'erne , da staterne STATER og USSR valgte det som oxidationsmiddeldannende med hydrazin og dets derivater. - hydrazinhydrat , MMH , UDMH , aerozin 50 og UH 25 hovedsageligt - af flydende drivmidler, der kan lagres hypergolisk .
Kaldt NTO (for nitrogentetroxid ) i forbindelse med rumfremdrivning , kvælstofperoxid er den hyppigst anvendte oxidator i hypergoliske motorer . Som sådan bruges det på et stort antal lavere etaper designet i 1960'erne, såsom den russiske Proton- bærerakett , Fregat-scenen for de russiske Sojuz- og Zenit- løfteraketter og de kinesiske raketter med lang marts . Det blev erstattet på disse stadier med flydende ilt på løfteraketter designet efterfølgende. Det bruges meget ofte på de øverste etager, der bibeholdes på trods af deres toksicitet, hypergoliske drivmidler, fordi de er nemme at opbevare i tankskydere og tillader flere antændelser som orbitale manøvreringsmotorer (OMS) i rumfærgen til NASA , Ariane 5, der kan lagres drivmiddel ( EPS) eller den indiske GSLV- løfteraket , motorerne, der tillader rumsonder at blive indsat i kredsløb osv.
Når det anvendes som drivmiddeloxidant (oxidant) blandes nitrogenperoxid generelt med en lille procentdel af nitrogenmonoxid N20 for at begrænse virkningerne på ætsende på legeringer af titanium involveret i fremdrivningssystemet for rumfartøjer : dette kaldes MON (for blandede oxider af Kvælstof ); WHO af rumfærgen bruger f.eks. MON-3 ved 3 % N (O (vægtfraktion).
Syntese
Ved fyring kobber nitrat + bly (II) nitrat , nitrogendioxid og nitrogen peroxid vises.
Toksicitet, økotoksicitet
Den toksicitet af inhaleret nitrogen peroxid er kendt og er blevet undersøgt i laboratoriedyr.
Det skyldes dets oxiderende natur , som har direkte virkninger på celler, men også effekter på hormonforstyrrelser . Kinesiske militærforskere har vist, at nitrogenperoxid især påvirker visse faktorer, der produceres af hjertets højre atrium (hormonelle faktorer, der regulerer blodtrykket ). Disse samme forskere har vist, at andre regulatoriske faktorer (kaldet natriuretika ), polypeptider ( atrielt natriuretisk polypeptid eller ANP) produceret af lungerne og til stede i lungeslim også blev forstyrret.
Noter og referencer
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- "Nitrogen Tetroxide" i databanken for farlige stoffer , adgang til 11. juni 2010
- (i) David R. Lide, Gummibibelen , CRC Press,2009, 90 th ed. , 2804 s. , Indbundet ( ISBN 978-1-4200-9084-0 )
- Indeksnummer i tabel 3.1 i tillæg VI til EF-regulativ nr. 1272/2008 (16. december 2008)
- SIGMA-ALDRICH
- " Nitrogen tetroxide " i databasen over kemikalier Reptox fra CSST (Quebec-organisation med ansvar for sikkerhed og sundhed på arbejdspladsen), adgang til den 25. april 2009
- "Dinitrogen tetraoxide" , om ESIS , adgang til 11. juni 2010
- JS BROADLEY & J. MONTEATH ROBERTSON Struktur af dinitrogen tetroxid natur 164, 915-915 1949/11/26; doi: 10.1038 / 164915a0
- CK INGOLD & E. HILDA INGOLD [Konstitutioner af dinitrogentetroxid og trioxid] Nature 159, 743-744; Dato 1947/05/31; doi: 10.1038 / 159743b0
- Holleman, AF; Wiberg, E. "Uorganisk kemi" Academic Press, 2001, San Diego. ( ISBN 978-0-12-352651-9 ) .
- W. Rogie ANGUS, RICHARD W. JONES & GLYN O. PHILLIPS Forekomst af nitrosylchlorid Ioner (NO +) i dinitrogentetroxid og af nitronium ioner (NO2 +) i gylle dinitrogenpentoxid natur 164, 433-434 (1949/11/10 ); doi: 10.1038 / 164433aZ
- CC ADDISON & R. THOMPSON Ioniske reaktioner i flydende dinitrogentetroxid ; natur 162, 369-370 (1948/11/04); doi: 10.1038 / 162369a0
- YE Ming Liang, XIA Ya Dong, WEN Si Zhen, GUO Xu Yi; [Ændring i atrielt natriuretisk faktorindhold hos rotter, der led af akut lungeødem induceret af dinitrogentetroxid]; (Institute of Pharmacology and Toxicology, Academy f Military Medical Sciences, Beijing 100850) ( Adgang til artiklen på kinesisk)
- [Effekt af dinitrogentetroxid på atrielt natriuretisk polypeptid og lungesurfaktivt middel i rotter Ye Mingliang], Wu Haihuan, Peng Liyi et al. ; Institut for Farmakologi og Toksikologi, Academy of Military Medical Sciences, Beijing 100850 ( link til originalartikel (kinesisk), abstrakt .
