Ethanol
| Ethanol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Ethanol-molekyle |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikation | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC navn | Ethanol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
ethylalkohol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EF | 200-578-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-kode | D08 , V03 , V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB00898 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 702 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 16236 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E1510 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2419 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILE |
CCO , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C2H6O / c1-2-3 / h3H, 2H2,1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Udseende | farveløs væske med en karakteristisk lugt. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formel |
C 2 H 6 O [isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar masse | 46,0684 ± 0,0023 g / mol C 52,14%, H 13,13%, O 34,73%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolært øjeblik | 1,66 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekylær diameter | 0,469 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusion | −114 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kogning | 79 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighed | i vand: blandbar, Komplet i polære og ikke-polære opløsningsmidler ( acetone , diethylether ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighedsparameter δ |
26,0 MPa 1/2 ( 25 ° C ); 11,2 cal 1/2 · cm -3/2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumenmasse |
0,789
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Automatisk tænding temperatur |
423 til 425 ° C ; 363 ° C (afhængigt af kilderne) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | lukket skål: 13 ° C ren 17 ° C 95 % vol . 21 ° C 70 % vol . 49 ° C 10 % vol . 62 ° C 5 % vol . |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosionsgrænser i luft | Nedre: 3,3 % vol Øvre: 19 % vol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mættende damptryk | ved 20 ° C : 5,8 kPa
ligning:
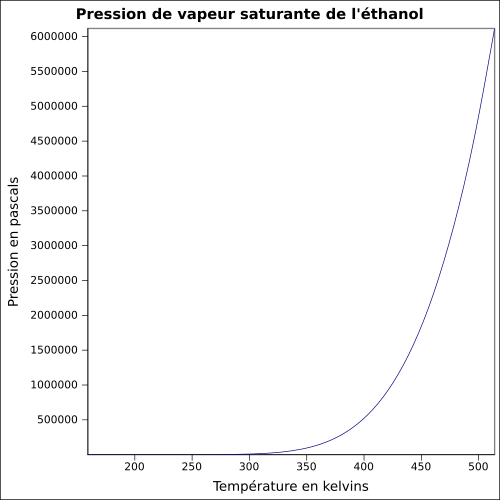
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynamisk viskositet | 1,20 × 10 −3 Pa s ved 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | 240,85 ° C , 6,14 MPa , 0,168 l mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lydens hastighed | 1162 m s −1 ved 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 væske, 1 bar | 159,86 J · mol -1 · K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | −235,3 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 væske | −277,0 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
111 J · K- 1 · mol -1
ligning:
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| STK | 1 366,8 kJ · mol -1 (væske) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ioniseringsenergi | 10,43 ± 0,05 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystallografi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalklasse eller rumgruppe | Pc | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mesh-parametre |
a = 5,377 Å b = 6,882 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bind | 298,57 Å 3 densitet = 0,7893 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brydningsindeks | 1.3594. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Fare H225, P210, P305 + P351 + P338, P370 + P378, P403 + P235, H225 : Meget brandfarlig væske og damp P210 : Holdes væk fra varme / gnister / åben ild / varme overflader. - Rygning forbudt. P305 + P351 + P338 : Ved øjnene: Skyl forsigtigt med vand i flere minutter. Fjern kontaktlinser, hvis offeret har dem på, og de let kan fjernes. Fortsæt med at skylle. P370 + P378 : I tilfælde af brand: Brug ... til udryddelse. P403 + P235 : Opbevares på et godt ventileret sted. Slap af. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 2 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
33 : meget brandfarlig væske (flammepunkt under 21 ° C ) UN-nummer : 1170 : ETHYLALKOHOL indeholdende mere end 24 volumenprocent ethanol; ETHYLALKOHOLOPLØSNING indeholdende mere end 24 volumenprocent ethanol ETHANOL indeholdende mere end 24 volumenprocent ethanol eller ethanolopløsning indeholdende mere end 24 procent ethanol, efter volumen Klasse: 3 Label: 3 : Brændbare væsker Emballage: Packing gruppe II : medium farlige stoffer;  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IARC- klassificering | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe 1: Kræftfremkaldende for mennesker | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Indånding | forgiftning, kvalme, opkastning | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hud | ingen effekt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Øjne | farligt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Indtagelse | forgiftning, kvalme, opkastning, ethylkoma (som kan føre til døden) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Økotoksikologi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 5 til 20 g kg −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CL 50 | 20.000 til 30.000 ppm i 4 til 6 timer | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -0,32 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lugtgrænse | lav: 49 ppm høj: 716 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Farmakokinetiske data | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Metabolisme | i leveren i ethanal og derefter eddikesyre ved ~ 100 mg kg -1 i timen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Psykotrop karakter | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori | Depressant | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Måde at forbruge |
Indtagelse |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Andre navne |
Alkohol (se alkoholholdige drikkevarer ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Risiko for afhængighed | Studerende | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheder af SI og STP, medmindre andet er angivet. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den ethanol, eller ethylalkohol (eller mere enkelt alkohol ) er en alkohol med strukturformlen CH 3 -CH 2 -OH. Det er en farveløs væske, flygtig , brandfarlig og blandbar med vand i alle forhold. Det er et psykotrop stof , og et af de ældste rekreative stoffer i form af en alkoholholdig drik . Ethanol bruges af fødevareindustrien (især til fremstilling af spiritus ), parfume og farmaceutiske lægemidler (som opløsningsmiddel ) såvel som i biobrændstof ( bioethanol ). Det bruges også i alkoholtermometre .
Formel
Ethanol er en to-carbon primære alkohol af det rå formel C 2 H 6 Oog af den semi-strukturformel CH 3 CH 2 OHeller CH 3 -CH 2 -OH, Hvilket indikerer, at carbon i methyl gruppe (CH 3 -) Er fastgjort til den methandiyl gruppe (-CH 2 -) selv bundet til hydroxylgruppen (-OH). Det er en konstitution isomer af methyletheren . Ethanol er normalt betegnet med forkortelsen ”EtOH”, den ethyl- gruppe (C 2 H 5 -) der ofte forkortes "Og" i organisk kemi .
Efternavn
Ethanol er det systematiske navn, der er defineret ved nomenklaturen for organiske forbindelser til et molekyle med to carbonatomer (præfiks eth- ) med en enkelt binding imellem (suffiks -an ) og bundet til en hydroxylgruppe (suffiks -ol ).
Historie
Den gæring af sukker til ethanol er en af de ældste bioteknologi anvendes af mennesker, især i alkoholindustrien og har været anvendt siden oldtiden til opnåelse alkoholiske drikkevarer . Kemiske analyser af organiske forbindelser absorberes i krukker stammer fra det bondestenalderen fundet i en landsby i provinsen Henan i Kina , viste, at blandinger af gærede drikkevarer bestående af ris, honning og frugt blev produceret fra VII th årtusinde BC. AD .
Selvom destillation er en teknik kendt alkymister græsk-egyptiske (som Zosimos af panopolis ), de første skriftlige optegnelser over produktion af alkohol fra vin går tilbage kun XII th århundrede med arbejdet i de alkymister i School of Medicine i Salerno . Den første omtale af sondringen mellem absolut alkohol og vand-alkohol-blandinger er rapporteret til XIII th århundrede af Raymond Lully . Bemærk dog, at de lærde persiske Rhazes har isoleret ethanol i den aktuelle X th århundrede.
I 1796 , Johann Tobias Lowitz opnås rent ethanol ved at filtrere destilleret ethanol gennem aktivt kul . Antoine Lavoisier fastslår, at ethanol er sammensat af carbon , oxygen og hydrogen , og i 1808 , Nicolas Théodore de Saussure bestemmer dens rå formel . I 1858 , Archibald Scott Couper offentliggjorde kemiske struktur af ethanol, som var en af de første strukturer bestemt.
Ethanol blev først fremstillet syntetisk i 1826 af det uafhængige arbejde af Georges Serullas i Frankrig og Henry Hennel i Det Forenede Kongerige . I 1828 , Michael Faraday syntetiseret ethanol ved syrekatalyseret hydratisering af ethylen , en syntese svarer til den industrielle proces, der anvendes i dag.
Ethanol blev også brugt som brændstof i lamper og som brændstof til biler indtil 1930'erne . For eksempel kunne Ford T køre indtil 1908 på ren ethanol.
Naturlig tilstedeværelse
Ethanol er et flygtigt biprodukt af gær stofskifte . Det er derfor til stede i disse organismeres levested og i vores atmosfære. Det findes også udsendt af modne frugter, og i mange planter på grund af naturlige anaerobe forhold under spiring, eller når planter, der mangler ilt (i tilfælde af oversvømmelse for eksempel), får energi fra gæring.
I begyndelsen af 2000'erne var dens atmosfæriske cyklus stadig dårligt forstået. Vi søger at kvantificere den ethanol, der udsendes af planter og gær, dens niveauer i atmosfæren og dens omdannelsesrate via luftens hydroxyl (ved titrering af methylchloroform ). Et første groft skøn gav en ethanolemissionshastighed fra planter på mellem 10 og 38 Tg / år, dvs. et stort bidrag til den estimerede samlede ethanol, der indføres i atmosfæren årligt (mellem 25 og 56 Tg / år). År). Derefter reviderede nyt arbejde emissioner fra planter opad: 70 Tg / år (fra 50 til 90 Tg / år), hvor omkring 75% af den ethanol, der blev introduceret fra luften, i virkeligheden blev ødelagt ved reaktion med hydroxylradikaler i tør eller fugtig luft. Der findes også tørre og våde aflejringer på tørt land.
Ethanol er også blevet påvist i rummet og dækker støvkorn i fast form i interstellære skyer .
Fysisk-kemiske egenskaber
Ethanol er en flygtig , farveløs væske, der har en lugt. Dens forbrænding er røgfri og giver en blålig flamme. De fysisk-kemiske egenskaber af ethanol kommer hovedsageligt fra tilstedeværelsen af hydroxylgruppen og den korte carbonkæde . Hydroxylgruppen kan danne hydrogenbindinger , hvilket gør ethanol mere tyktflydende og mindre flygtigt end organiske opløsningsmidler med ækvivalente molekylvægte . Den brydningsindeks af ethanol er højere end vands (1,3594 ved 25,0 ° C ). Den tredobbelte punkt ethanol observeres ved -123,15 ° C til et tryk på 4,3 × 10 -4 Pa .
Egenskaber som opløsningsmiddel
Ethanol er et polært protisk opløsningsmiddel . Det er blandbart med mange organiske opløsningsmidler , såsom chlorerede opløsningsmidler ( carbontetrachlorid , chloroform , trichlorethan , tetrachlorethylen ), alifatiske carbonhydrider ( pentan , hexan ), aromatiske opløsningsmidler ( benzen , toluen , pyridin ), eddikesyre , acetonen , diethyletheren , ethylenglycol eller nitromethan . Imidlertid blandbarheden af ethanol med alifatiske carbonhydrider tendens til at aftage med stigningen i længden af carbonkæden af alkan og faldet i temperaturen, for blandbarhed er for eksempel 13 ° C for dodecan. .
På grund af den polære karakter af hydroxylgruppen gruppe , kan ethanol også opløse ioniske forbindelser , såsom natrium- og kalium- hydroxider , magnesium , calcium og ammoniumchlorider, eller ammonium og natrium bromider. . Natrium- og kalium chlorider er kun lidt opløseligt i ethanol.
Den ikke- polære del af ethanol gør det muligt at opløse hydrofobe stoffer , især essentielle olier og mange lugtende, farvestoffer og medicinske forbindelser.
Ethanol kan anvendes som opløsningsmiddel i mange kemiske reaktioner under synteser , såsom i nukleofile S N 1 substitutioner , under katalytiske hydrogeneringer under aldolreaktioner , under Wittig-reaktioner , under Diels- reaktioner. Alder eller under diazotering reaktioner .
Ethanol er inert over næsten alle blødgjorte overflader i hverdagen, lakker (undtagen celluloselakker og dem med shellak ), akryl og glycerophthalic maling, mens det er et meget godt opløsningsmiddel. Dette gør det til et meget anvendt rengøringsmiddel alene eller i blanding med andre forbindelser.
Blandbarhed med vand
Vand-ethanolblandinger optager et volumen, der er mindre end summen af volumenet af de to komponenter taget individuelt. Blandingen af et volumen vand og et volumen ethanol giver f.eks. Et ækvivalent volumen på 1,92. Reaktionen mellem blanding af vand og ethanol er eksoterm , og ved 24,85 ° C kan der frigøres op til 777 J mol -1 . Ethanols polære natur gør den hygroskopisk , så meget, at den ren absorberer fugt fra luften.
En azeotrop dannes med vand ved 89,47 mol-% ethanol og 10,53 mol-% vand ved atmosfærisk tryk . Den kogepunkt ethanol er 78,4 ° C og 100 ° C for vand, men azeotropen koger ved 78,2 ° C , hvilket er under kogepunkterne for hver. Bestanddele. Andelene af den azeotropiske blanding varierer som en funktion af trykket.
| Tryk | Kogepunkt | Molær fraktion af etanol |
|---|---|---|
| 0,1 MPa | 78,35 ° C | 0,894 |
| 0,334 MPa | 112,6 ° C | 0,882 |
| 0,689 MPa | 135,7 ° C | 0,874 |
| 1,378 MPa | 164,2 ° C | 0,862 |
| 2.068 MPa | 182,6 ° C | 0,852 |
Tilsætning af et par procent ethanol til vandet sænker vandets overfladespænding drastisk . Denne egenskab hjælper med at forklare fænomenet vintårer . Når man hvirvler vin i et glas, fordamper ethanolen hurtigere i den tynde film langs siderne af glasset. Andelen af ethanol falder, så overfladespændingen øges, og filmen bliver til dråber. Dette fænomen kaldes Marangoni-effekten og blev beskrevet og forklaret i 1855 af James Thomson.
Den alkoholindhold , også kaldet alkoholisk grad er forholdet mellem mængden af alkohol indeholdt i blandingen, og det samlede volumen af blandingen til 20 ° C . Det bruges til at bestemme andelen af alkohol, det vil sige ethanol, i en alkoholholdig drik . Enheden, der bruges til at udtrykke titeren, er volumenfraktionen (% vol) eller grad (bemærket "°").
Vand-ethanolblandinger indeholdende mere end 50% ethanol er brandfarlige ved stuetemperatur , men ved opvarmning kan en blanding indeholdende mindre end 50% ethanol antænde. Den madlavning teknik bruger denne egenskab. Alkohol tilsat i en varm gryde brænder op i flammer og giver en kompleks reaktion. Temperaturen på den alkohol, der brænder, kan derefter overstige 240 ° C og fører til karamelliseringen af det tilstedeværende sukker .
Produktion
Ethanol kan produceres industrielt fra petrokemikalier ved hydrering af ethylen og ved alkoholfermentering af gær eller cellulose . Den mest økonomiske proces afhænger hovedsageligt af oliemarkedet .
Direkte katalyse
Denne proces, der blev udviklet i 1970'erne, har fortrængt andre produktionsmetoder fuldstændigt. Den således fremstillede ethanol anvendes af industrien som råmateriale eller som opløsningsmiddel . Den fremstilles ved petrokemikalier , under anvendelse af hydratisering af syre katalyse af ethylen , efter reaktionen:
H 2 C = CH 2+ H 2 O↔ CH 3 CH 2 OHDen mest anvendte katalysator er phosphorsyre , adsorberet på en porøs bærer, såsom silicagel eller celite . En stigning i trykket hjælper med at flytte ligevægten mod produktionen af ethanol efter Le Chateliers princip , og det er derfor at bruge en katalysator under højt vanddampstryk for at nærme sig ligevægt hurtigt. Slutproduktet er en vand-ethanolblanding indeholdende mellem 10 % og 25 % m ethanol.
Indirekte katalyse
En tidligere proces, men nu er forældet, udviklet i 1930'erne af Union Carbide , og vil blive brugt for meget af XX th århundrede . Den ethylen er forestret med svovlsyre til producere ethylsulfat , som derefter hydrolyseres til opnåelse af ethanol og svovlsyre, der således tjener som en katalysator i denne reaktion:
H 2 C = CH 2+ H 2 SO 4→ CH 3 CH 2 SO 4 H CH 3 CH 2 SO 4 H+ H 2 O→ CH 3 CH 2 OH+ H 2 SO 4Denne proces forbruger store mængder svovlsyre og kræver en gasblanding af god kvalitet som input.
Fermentering
Ethanol, der anvendes i alkoholholdige drikkevarer , produceres ved alkoholfermentering . Ligeledes kommer de fleste bioethanol fra gæringsbehandlingen af sukkerplanter, såsom rødbeder og sukkerrør eller korn, såsom majs og hvede . Visse typer gær , såsom Saccharomyces cerevisiae , metaboliserer sukker til ethanol og kuldioxid efter disse reaktioner:
C 6 H 12 O 6→ 2 CH 3 CH 2 OH+ 2 CO 2 C 12 H 22 O 11+ H 2 O→ 4 CH 3 CH 2 OH+ 4 CO 2Fermenteringen er gæren dyrkes under gunstige betingelser for at fremstille alkoholen, ved en temperatur på ca. 35 til 40 ° C . De mest resistente gærstammer kan overleve i en koncentration på ca. 15 vol% ethanol. Ethanols toksicitet over for gær begrænser den koncentration af alkohol, der kan opnås ved brygning , og højere koncentrationer kan opnås ved mutation eller destillation . Under fermentering dannes sekundære produkter, såsom glycerol , af ravsyre , eddikesyre og amylalkohol .
For at producere ethanol fra stivelse , for eksempel fra kornfrø, skal den først omdannes til sukker. Når brygning øl, er et frø lov til at spire ( maltning ), som muliggør produktionen af visse enzymer, såsom cytases , amylaser , phosphataser eller peptidaser , der er nødvendige for forsukring af stivelse. For bioethanol kan denne proces accelereres ved anvendelse af svovlsyre eller ved anvendelse af en amylase fremstillet af svampe.
Celluløs ethanol
Den Fermenteringen kan også opnås fra cellulose , men indtil for nylig omkostningerne ved cellulase , et enzym der er i stand til at nedbryde cellulose, ikke tillod industrien til at udvikle industrielt. I 2004 byggede det canadiske firma Iogen Corporation det første anlæg baseret på produktion af ethanol fra cellulose. Udviklingen af denne teknologi kunne gøre det muligt at bruge og genbruge en masse planteaffald fra landbruget, der indeholder cellulose, såsom savsmuld eller halm . Andre bioteknologiske virksomheder udvikler i øjeblikket svampe, der er i stand til at producere store mængder cellulase og xylanase for at omdanne andre landbrugsrester til cellulose, såsom majsaffald eller bagasse fra sukkerrør .
Oprensning
De forskellige ethanolproduktionsprocesser producerer vand-ethanolblandinger. Til brug i industrien eller som brændstof skal ethanol renses. Den fraktionerede destillation kan koncentrere ethanol til 95,6 vol-% (89,5 mol% ), og danner en blanding azeotrop med vand, hvis kogepunkt er 78,2 ° C . De sædvanlige fremgangsmåder til opnåelse af absolut ethanol indbefatter anvendelsen af tørremidler , såsom stivelse , glycerol eller zeolitter , azeotrop destillation og ekstraktionsdestillation .
Ethanol kvaliteter
Forskellige kvaliteter af ethanol er tilgængelige til forskellige anvendelser:
- den denaturerede alkohol er typisk ethanol, som tilsættes et denatureringsmiddel for at fremstille forkert blanding af madforbruget. De anvendte denatureringsmidler kan være isopropylalkohol , methanol , diethylphthalat , thiophen , diethylether eller ellers naturgaskondensater . Det bruges til rengøring, rengøring, desinfektion og i alkoholkomfurer . En møbelsnedkeres opløsningsmiddel til sine shellaklakker , det er også et affedtningsmiddel i branchen, værdsat for dets lave toksicitet på huden. Generelt ved 95 % vol ;
- methyleret spiritus er en blanding af ethanol og methanol . Methyleret spiritus er meget giftig på grund af tilstedeværelsen af methanol (generelt 5 til 10 % vol ). Det bruges til at rense vinduer og plastoverflader;
- den rektificerede alkohol er et destillat, der måler fra 70 til 96% vol. ethanol ved anvendelse af metoden fraktioneret destillation . Den maksimale koncentration, der kan opnås ved destillation af rå alkohol, er 96 % vol på grund af dannelsen af en vand-ethanol- azeotrop . Det bruges til fremstilling af likører eller vodka , men også til husholdningsvedligeholdelse, rengøring eller desinfektion;
- den absolutte ethanol er ethanol indeholdende maksimalt 1% vand, men de fleste af de største leverandører inden for kemi sælger under betegnelsen absolut ethanolethanol 99,8%. Det bruges som opløsningsmiddel til laboratorie- og industrielle anvendelser og som brændstof;
- vandfri ethanol er ethanol, hvorfra vand er fjernet så meget som muligt. For eksempel producerer reaktionen af absolut ethanol med metallisk magnesium efterfulgt af destillation ved atmosfærisk tryk ethanol ved 50 ppm vand (0,005 masseprocent vand eller 1 / 20.000). Denne klasse ethanol gør det muligt at bruge den i fugtighedsreaktioner.
Reaktivitet og reaktioner
Ethanol er en primær alkohol og en svag syre ( p K a = 15,5), hvis konjugerede base er ethanolat . Det er også en god nukleofil på grund af reaktiviteten af de ikke- oxygenbindende dubletter . Dens reaktivitet, hovedsageligt på grund af tilstedeværelsen af hydroxylgruppen , kan involvere reaktioner med dehydrering , dehydrogenering , oxidation og forestring .
Syre-base kemi
Ethanol er et neutralt molekyle, og pH i en opløsning af ethanol i vand er 7,00. Ethanol kan kvantitativt omdannes til sin konjugatbase , ethanolationen , ved at reagere med et alkalimetal , såsom natrium :
2 CH 3 CH 2 OH+ 2 Na→ 2 CH 3 CH 2 ONa+ H 2eller med en stærk base , såsom natriumhydrid :
CH 3 CH 2 OH+ NaH→ CH 3 CH 2 ONa+ H 2Forestring
Ethanol reagerer med carboxylsyrer i nærvær af en stærk syre ( katalyse ) til opnåelse ethyl- estere og vand ifølge den følgende reaktion:
RCOOH+ CH 3 CH 2 OH→ RCOOCH 2 CH 3+ H 2 ODenne reaktion er reversibel, og ligevægt nås langsomt, hvilket kræver anvendelse af sure katalysatorer , såsom svovlsyre , saltsyre , bortrifluorid eller paratoluensulfonsyre . For at opnå korrekte udbytter kræver denne reaktion, som anvendes i stor industri, fjernelse af vand fra reaktionsblandingen, når den dannes. Ethanol kan også danne estere med uorganiske syrer, og gør det muligt at fremstille forbindelser i vid udstrækning anvendes i organisk syntese , såsom som diethylsulfat (C 2 H 5 ) 2 SO 4eller triethylphosphat (C 2 H 5 ) 3 PO 4. Den nitrit ethyl CH 3 CH 2 O-N = Okan ligeledes fremstilles af ethanol og natriumnitrit og blev almindeligvis brugt som et vanddrivende middel eller et middel mod influenza eller forkølelse , før det blev trukket tilbage fra markedet i begyndelsen af 1980'erne .
Den forsæbning reaktion , som giver ethanol skal reformeres fra ethylestere i nærværelse af en syre eller en base til opnåelse af et carboxylat , anvendes til fremstilling af sæbe .
Dehydrering
Anvendelsen af stærke syrer kan gøre det muligt at dehydrere ethanol til dannelse af diethylether , og der produceres flere ton diethylether hvert år ved anvendelse af svovlsyre som katalysator . Reaktionen kan beskrives som følger:
2 CH 3 CH 2 OH→ CH 3 CH 2 OCH 2 CH 3+ H 2 O(ved 120 ° C )Den ethylen er hovedproduktet, når temperaturen overstiger 160 ° C :
CH 3 CH 2 OH→ H 2 C = CH 2+ H 2 OForbrænding
Den forbrænding af ethanol er røg og giver en blålig flamme. Forbrændingsreaktionen danner kuldioxid og vanddamp :
CH 3 CH 2 OH( l ) + 3 O 2( g ) → 2 CO 2( G ) + 3 H 2 O( g )Den brændværdi (Δ c H °) af forbrænding af ethanol er 1366,8 kJ mol -1 ved 25 ° C , og den specifikke varmekapacitet (C v ) er 2.438 kJ kg -1 K -1 .
Oxidation
Den oxidation (eller dehydrogenering ) i ethanol i nærværelse af katalysatorer gør det muligt at opnå ethanal (eller acetaldehyd ), ifølge den følgende reaktion:
CH 3 CH 2 OH→ CH 3 CHO+ H 2I hepatocytter i leveren omdanner enzymet alkoholdehydrogenase ligeledes ethanol til ethanal. Ethanal er mere giftigt end ethanol og kan være ansvarlig for mange tømmermænds symptomer , selvom det ikke er til stede i blodet under symptomer. I hjernen har alkoholdehydrogenase en mindre rolle i omdannelsen af ethanol til ethanal, og det er katalaseenzymet , der primært katalyserer denne reaktion.
De sidste faser af alkoholisk fermentering involverer omdannelse af pyruvat til ethanal af enzymet pyruvat decarboxylase efterfulgt af reduktion (eller hydrogenering ) af ethanal til ethanol af enzymet alkohol dehydrogenase , i dette tilfælde katalyserer den modsatte reaktion. Som en endogen metabolit er ethanal giftigt og er mistænkt kræftfremkaldende. Det beskadiger de hæmatopoietiske stamceller (ansvarlig for konstant fornyelse af blodet ); på den ene side er det kilden til brud i disse cellers dobbeltstrengede DNA (hvilket fremmer deres tilbagegang og skaber kromosomale omlejringer ), og på den anden side forhindrer det korrekt reparation ( s. 53 ) af denne skade, som forårsager maligniteter.
Halogenering
Ethanol reagerer med hydrohalogensyrer til frembringelse halogenalkaner , såsom chlorethan og bromethan , via en S N 2 reaktion :
CH 3 CH 2 OH+ HCI→ CH 3 CH 2 Cl+ H 2 ODenne reaktion kræver anvendelse af en katalysator , såsom zinkchlorid . De alkylhalogenider kan også syntetiseres under anvendelse af halogeneringsmidler, såsom thionylchlorid eller phosphortribromid :
CH 3 CH 2 OH+ SOCl 2→ CH 3 CH 2 Cl+ SO 2+ HCIHaloform reaktion
Den haloform reaktion er en kemisk reaktion , der består i at syntetisere en trihalogenomethane , såsom chloroform (CHC 3), Bromoform (CHBr 3) Eller iodoform (CHI 3), og er en af de ældste organiske reaktioner beskrevet som sådan. I 1822 , Georges Serullas rapporterede omsætningen af ethanol med diodine og natriumhydroxid i vand under dannelse natriumformiat og iodoform , derefter kaldt "carbon hydroiodid".
Ethanol reagerer med natriumhypochlorit for at give chloroform ifølge følgende syntese:
CH 3 CH 2 OH+ NaClO→ CH 3 CHO+ NaCl+ H 2 O CH 3 CHO+ 3 NaOCl→ CCl 3 CHO+ 3 NaOH CCl 3 CHO+ NaOH→ CHC 3+ HCO 2 NaLigeledes opnås henholdsvis bromoform og iodform fra natriumhypobromit og natriumhypoiodit. Ethanol er den eneste primære alkohol, der tillader denne reaktion.
brug
Brændstof
Ethanolen, der produceres over hele verden, bruges hovedsageligt som brændstof . Mængden af ethanol kan variere fra et par procent i benzin i Vesteuropa til 95 % vol i benzin i Brasilien , hvor 90% af nye køretøjer bruger flex-brændstofteknikken og kan køre på denne blanding. Over 66% af den ethanol, der anvendes som brændstof, kommer fra alkoholisk gæring .
E85- brændstof distribueret i Frankrig indeholder mellem 65% og 85% bioethanol, resten er benzin; satsen varierer mellem 65% og 75% om vinteren og når 85% om sommeren.
Associeret med vand var det brændstoffet for mange fly ( forbrændingsmotorer ) og raketter under Anden Verdenskrig for lande med få petroleumsressourcer.
I Frankrig er 1% af jorden afsat til bioethanol. Af de atten millioner hl produceret årligt i Frankrig bruges tolv millioner til fremstilling af biobrændstof, hvoraf 30% markedsføres uden for Frankrig. Af de otte millioner hl bioethanol beregnet til biobrændstof i Frankrig anvendes en million (eller 12%) i E85-brændstof . En lille mængde ethanol bruges også til fremstilling af ED95 (95% bioethanol og 5% pro-cetanadditiv) til specifikt motoriserede tunge godskøretøjer (inklusive busser).
Alkoholiske drikkevarer
Ethanolindholdet (eller graden af alkohol ) i alkoholholdige drikkevarer varierer med produktionsmetoden og råmaterialet. De fleste alkoholholdige drikkevarer kan klassificeres mellem gærede drikkevarer og spiritus . De vigtigste gærede drikkevarer er øl , produceret af korn eller andre stivelsesproducerende planter , vine og cider , fremstillet af frugtsaft og mjød , der er fremstillet af honning . De ånder produceres ved at destillere gærede drikkevarer . Vi kan skelne mellem forskellige typer spiritus , såsom whisky , destilleret fra gærede kornfrø, brandy , destilleret fra fermenteret frugtsaft eller rom , destilleret fra melasse eller juice af sukkerrør . Mange eaux-de-vie og likører fremstilles også ved at infundere frugt, urter og krydderier i spiritus , såsom gin, der er skabt ved infusion af enebær i rettet alkohol .
Andre metoder kan bruges til at øge alkoholniveauet , såsom fraktioneret størkning , som bruges til at fremstille applejack af æblejuice. Den berigede vin fremstilles ved at føje den til livsvandet eller andre spiritus til delvist gæret vin, hvilken metode dræber gæren, mens nogle af sukkerne opretholdes.
Alkoholiske drikkevarer bruges til madlavning efter deres duft, og fordi alkohol opløser hydrofobe lugtende forbindelser . Ethanolen fra disse drikkevarer bruges også til at producere eddike på samme måde som industriel ethanol bruges til produktion af eddikesyre .
Råmateriale
Ethanol er et vigtigt syntetisk mellemprodukt i den kemiske industri . Det anvendes især under fremstillingen af ethyl -halogenider , ethyl- estere, ethyl- aminer , diethylether , eddikesyre , og i mindre grad butadien .
Antiseptisk
Ethanol anvendes inden for det medicinske område i kompresser som et antiseptisk middel . Det anvendes også i hydroalkoholiske opløsninger i en koncentration på ca. 60 % vol . Ethanol dræber organismer ved at denaturere deres proteiner og opløse deres lipider. Det er effektivt mod de fleste bakterier og svampe , mange vira , men er ineffektivt mod sporer .
Opløsningsmiddel
Ethanol kan blandes med vand og er et godt opløsningsmiddel . Det kan findes i maling , industrielle nuancer, traditionelle lakker, alkoholholdige drikkevarer , markører og i kosmetik som parfume og deodoranter .
Medicinsk brug
Den absolutte ethanol injiceres undertiden i tumorer for at forårsage deres nekrose . Imidlertid har den ikke en målrettet aktivitet, da den uden forskel forårsager nekrose af sunde og kræftvæv.
Ethanol bruges også til behandling af methanol eller ethylenglycolforgiftning . I disse tilfælde konkurrerer ethanol med andre alkoholer, der metaboliseres af enzymet alkoholdehydrogenase , hvilket reducerer de toksiske derivater, der skyldes deres metabolisering til aldehyder og carboxylsyrer , og reducerer de toksiske virkninger på grund af krystallisationen af calciumoxalat (fra ethylenglycol ) i nyrerne .
Historiske anvendelser
Før udviklingen af moderne medicin blev ethanol brugt til forskellige medicinske formål, herunder behandling af depression og som et bedøvelsesmiddel . Det er også kendt at være i stand til at tjene som et sandhedsserum .
Som brændstof blev det brugt i raketmotorer kombineret med flydende ilt . Under 2. verdenskrig brugte det tyske " V2 " -missil ethanol blandet med 25 vol% vand for at sænke forbrændingskammerets temperatur . Den amerikanske " PGM-11 Redstone " ballistiske missil , inspireret af designet af den tyske V2, brugte også ethanol blandet med flydende ilt . Alkoholbaserede brændstoffer til raketter og missiler blev efterfølgende i brug, da nye brændstoffer blev udviklet.
Farmakologi
De to hovedveje for metabolisme af ethanol i leveren er alkoholdehydrogenase og oxidationssystem mikrosomal ethanol (in) . Ved lave ethanolkoncentrationer oxiderer alkoholdehydrogenase ethanol til acetaldehyd , men ved højere koncentrationer eller med gentagne doser ethanol er det mikrosomale ethanoloxidationssystem dominerende.
I den europæiske farmakopé betegner "ethanol" vandfri ethanol, det vil sige 100% ren, i modsætning til 95 % vol eller 70 % vol ethanol, som kan findes på apoteker . Hertil kommer kvaliteten ”alkohol Ph. Eur. "(For europæisk farmakopé ), der betegner en kvalitet af ethanol, for hvilken der er kvantificeret mange spor og urenheder.
Fysiologiske egenskaber
Der er forskellige virkninger af alkoholholdige drikkevarer , idet alkoholisme er det overdrevne forbrug af drikkevarer, der indeholder ethanol, hvilket fører til afhængighed, som klassificerer ethanol som et stof. Dette ville være det mest skadelige stof for samfund.
| Alkohol i blodet ( g · l –1 ) |
Alkoholindhold ( % vol ) |
Symptomer |
|---|---|---|
| 0,5 | 0,05 | Eufori, afslapning |
| 1.0 | 0,1 | Depression, kvalme, opkastning, nedsat sensoriske og motoriske færdigheder, nedsat kognition |
| > 1.4 | > 0,14 | Nedsat blodgennemstrømning til hjernen |
| 3.0 | 0,3 | Tab af bevidsthed |
| 4.0 | 0,4 | Mulig død |
| 5.5 | 0,55 | Død |
Alkohol i blodet
Den BAC er mængden af ethanol i blodet; det udtrykkes generelt i gram pr. liter blod. Alkoholniveauer i blodet på over 4,0 g L -1 kan være dødelige, og niveauet bliver dødeligt over 5,5 g L -1 . Lave doser ethanol, under 0,5 g L -1 , forårsager en følelse af eufori , hvor folk bliver mere snakkesalige, mindre hæmmede og viser reducerede analytiske færdigheder. Ved højere doser, over 1,0 g L -1 , fungerer ethanol som et depressivt middel på centralnervesystemet , symptomer, der involverer nedsat kognition , nedsat sensoriske og motoriske funktion, bevidsthedstab indtil døden.
Effekter på centralnervesystemet
Ethanol er et depressivt af det centrale nervesystem og betragtes som et lægemiddel psykotropisk . Det virker på centralnervesystemet ved hovedsageligt at interagere med GABA A- receptorer , hvilket øger den inhiberende virkning af neurotransmitteren γ-aminosmørsyre (eller GABA). GABA nedsætter neuronernes aktivitet (i modsætning til glutamat, som er en informationsaccelerator); således, ved at binde til GABA-receptorer, ethanol overdriver opbremsning af hjernen . Det fungerer derfor som en positiv allosterisk modulator . Ethanol virker også på receptorer for serotonin , glutamat , acetylcholin og dopamin . Dens negative virkninger kan forværres af bly, som forbedrer oxidativt stress . Bly forstærker alkoholens virkning på centralnervesystemet (CNS).
Langvarigt forbrug af ethanol kan derfor forårsage permanent skade på hjernen og andre organer. Den tilbagetrækning alkohol kan forårsage forskellige symptomer såsom uorden opmærksomhed underskud , øget svedtendens, takykardi , tremor (rysten af ekstremiteterne), undertiden kvalme eller opkastning, dehydrering, utilpashed , af hypertension . Nogle gange ledsages det af et anfald af epilepsi , visuelle, taktile eller auditive hallucinationer, det er delirium tremens i sin mest alvorlige form. Til sidst og i sjældne tilfælde kan der forekomme smerter fra kæben til kraniet. Ethanol har også vist sig at medføre ændringer i størrelsen af gråt stof, der er synligt med det blotte øje .
Virkninger på stofskiftet
Som sådan er ethanol et næringsstof . I menneskekroppen metaboliseres det til acetaldehyd af enzymet alkoholdehydrogenase . Acetaldehyd omdannes efterfølgende af acetaldehyddehydrogenase til acetyl-coenzym A , som er slutproduktet af kulhydrat- og lipidmetabolisme . Imidlertid er acetaldehyd i sig selv meget mere giftigt end ethanol og er delvis ansvarlig for de fleste kliniske effekter af alkohol, såsom tømmermænd . Især har det vist sig at øge risikoen for skrumpelever af leveren og er knyttet til mange former for kræft .
Langsigtede effekter
Ethanol er klassificeret som et teratogent middel og kan inducere føtal alkoholsyndrom , som er alkoholforgiftning af fosteret eller fosteret på grund af moderens alkoholforbrug under graviditet , og som forstyrrer udviklingsorganerne.
Det regelmæssige forbrug af alkohol er også en faktor, der bidrager til stigningen i triglyceriderne i blodet, hvilket favoriserer udseendet af hjerte-kar-sygdomme .
Ethanol i alkoholholdige drikkevarer betragtes som et klart kræftfremkaldende stof og er derfor et af IARC-gruppe 1 kræftfremkaldende stoffer .
Narkotikainteraktioner
Ethanol kan øge fænomenet sedation forårsaget af narkotika depressiva virker på centralnervesystemet , såsom barbiturater , de benzodiazepiner , den opioid , de phenothiaziner og antidepressiva .
Noter og referencer
- (fr) Denne artikel er helt eller delvist taget fra Wikipedia-artiklen på engelsk med titlen " Ethanol " ( se forfatterlisten ) .
- ETHANOL (ANHYDRO) , sikkerhedsark (er) i det internationale program for kemisk sikkerhed , hørt den 9. maj 2009
- (i) Y. Marcus , The Properties of Opløsningsmidler , Chichester, England, John Wiley & Sons , al. "Solution Chemistry" ( nr . 4),1998, 254 s. ( ISBN 978-0-471-98369-9 og 0471983691 , LCCN 98018212 , online præsentation ) , s. 95
- Marcus, 1998 , s. 88.
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- (i) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 978-0-387-69002-5 og 0-387-69002-6 , læs online ) , s. 294
- (in) Serban Moldoveanu, Præparatpræparation i kromatografi , Amsterdam / Boston, Elsevier ,2002, 930 s. ( ISBN 0-444-50394-3 ) , s. 258
- " Toksikologisk ark FT 48 - Ethanol " , på webstedet for det nationale forsknings- og sikkerhedsinstitut til forebyggelse af arbejdsulykker og erhvervssygdomme ,2011(adgang til 14. maj 2012 ) .
- (in) RH Perry og DW Green , Perrys kemiske ingeniørhåndbog , McGraw-Hill ,1997, 7 th ed. , 2640 s. ( ISBN 978-0-07-049841-9 , LCCN 96051648 ) , s. 2-50.
- (in) CA Faúndez og OJ Valderrama , " Modeller for aktivitetskoefficient til beskrivelse af damp-flydende ligevægt i ternære hydroalkoholiske opløsninger " , Chin. J. Chem. Eng. , Vol. 17, nr . 2april 2009, s. 259-267 ( ISSN 1004-9541 , DOI 10.1016 / S1004-9541 (08) 60203-7 )
- (i) William M. Haynes , Gummibibelen , Boca Raton, CRC Press / Taylor og Francis,1 st juli 2010, 91 th ed. , 2610 s. ( ISBN 9781439820773 , online præsentation ) , s. 14-40
- (in) O. Haida , H. Suga et al. , “ Kalorimetrisk undersøgelse af den glasagtige tilstand XII. Flertalsglasovergangsfænomener af ethanol ” , J. Chem. Termodynamik. , Vol. 9, nr . 12,December 1977, s. 1133–1148 ( ISSN 0021-9614 , DOI 10.1016 / 0021-9614 (77) 90115-X ).
- (i) J. Chao og FD Rossini , " forbrændingsvarme, træning og Isomerisering af alkanoler Nineteen " , J. Chem. Eng. Data , vol. 10, nr . 4,1965, s. 374–379 ( ISSN 0021-9568 , DOI 10.1021 / je60027a022 ).
- (i) Carl L. kæberne, Handbook of Termodynamiske Diagrams: Organic Compounds C8 til C28 , vol. 1, Huston, Texas, Gulf Pub. Co.,1996, 396 s. ( ISBN 978-0-88415-857-8 , LCCN 96036328 )
- (i) David R. Lide , Gummibibelen , Boca Raton, CRC Press,18. juni 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online præsentation ) , s. 5-89
- (i) David R. Lide , Gummibibelen , Boca Raton, CRC Press / Taylor og Francis,17. juni 2008, 89 th ed. , 2736 s. ( ISBN 9781420066791 , online præsentation ) , s. 10-205
- " Ethanol " , på reciprocalnet.org (adgang 12. december 2009 )
- [1]
- IARC-arbejdsgruppe om evaluering af kræftfremkaldende risici for mennesker, “ Globale evalueringer af kræftfremkaldende egenskaber for mennesker, gruppe 1: kræftfremkaldende for mennesker ” , på http://monographs.iarc.fr , IARC,16. januar 2009(adgang til 22. august 2009 )
- Sikkerhedsdatablad leveret af Sigma-Aldrich, hørt den 28.9.2019
- " Ethylalkohol " , på hazmap.nlm.nih.gov (adgang til 14. november 2009 )
- " ESIS " (adgang til 6. december 2008 )
- (in) GP Moss ( red. ), " Grundlæggende terminologi for stereokemi " , Pure Appl. Chem. , IUPAC , vol. 68, nr . 12,1996, s. 2193-2222 ( ISSN 0033-4545 og 1365-3075 , DOI 10.1351 / pac199668122193 ).
- (en) PE McGovern , J. Zhang et al. , “ Fermenterede drikkevarer fra det før- og prototehistoriske Kina ” , Proc. Natl. Acad. Sci. USA , bind. 101, nr . 51,21. december 2004, s. 17593-17598 ( ISSN 0027-8424 , PMID 15590771 , PMCID PMC539767 , DOI 10.1073 / pnas.0407921102 , læs online ).
- (da) RJ Forbes , En kort historie om destillationskunsten: Fra begyndelsen op til døden af Cellier Blumenthal , Leiden, Holland, Brill ,1970, 2 nd ed. ( 1 st ed. 1948), 405 s. ( ISBN 978-90-04-00617-1 , online præsentation , læs online ) , s. 89.
- " Mohammad Ibn Zakaria Razi (865-925), Den mest fremtrædende læge af islamiske civilisation - La Revue de Téhéran | Iran ” , på www.teheran.ir (adgang 9. juli 2016 )
- (i) " Alkohol " , på webstedet for Encyclopaedia Britannica ,1911(adgang til 12. maj 2012 ) .
- (in) AS Cut , " was New Chemical Theory " , Philos. Mag. , 4 th serier, vol. 16,1858, s. 104-116 ( ISSN 1478-6435 , læs online ).
- (i) H. Hennell , " Om den gensidige virkning af svovlsyre og alkohol, med bemærkninger til sammensætningen og egenskaberne af den resulterende forbindelse " , Philos. Trans. R. Soc. , Vol. 116,9. marts 1826, s. 240-249 ( DOI 10.1098 / rstl.1826.0021 , læs online ).
- (i) Joseph DiPardo, " Forventninger til biomasse Ethanol produktion og efterspørgsel " , på Energy Information Administration (adgang 14 maj 2012 )
- (i) VD Hunt , The gasohol håndbog , New York Industrial Press,nitten og firs, 580 s. ( ISBN 978-0-8311-1137-3 , online præsentation ).
- (in) R. Dudley , " Ethanol Fruit Ripening, and the Historical Origins of Human Primate Alcoholism in Frugivory " , Integr. Komp. Biol. , Vol. 44, nr . 4,2004, s. 315-323 ( ISSN 1540-7063 , DOI 10.1093 / icb / 44.4.315 ).
- Kreuzwieser J, Papadopoulou E & Rennenberg H (2004) Interaktion mellem fl ooderende og kulstofmetabolisme af skovtræer , Plant Biol., 6, 299-306, 2004
- Kimmerer TW & MacDonald RC (1987) Acetaldehyd og ethanolbiosyntese i blade af planter , Plant Physiol., 84, 1204-1209
- (in) S. Leblová E. Sineckáet et al. , “ Pyruvat metabolisme i spirende frø under naturlig anaerobiose ” , Biol. Plantarum , vol. 16, nr . 6,1974, s. 406-411 ( ISSN 0006-3134 , DOI 10.1007 / BF02922229 ).
- Kirstine WV & Galbally IE (2011) Det globale atmosfæriske budget ethanol revideret igen ; Atmosfærisk kemi og fysik 11 (1): 25909-25936 | September | DOI: 10.5194 / acpd-11-25909-2011
- (in) A. Schriver , L. Schriver-Mazzuoli et al. , “ En mulig oprindelse af ethanol i interstellært medium: Fotokemi af blandede CO 2 –C 2 H 6- film ved 11 K. En FTIR-undersøgelse ” , Chem. Phys. , Vol. 334, n knogle 1-3,2007, s. 128–137 ( DOI 10.1016 / j.chemphys.2007.02.018 ).
- (en) M. Windholz ( red. ), The Merck Index: An Encyclopedia of Chemicals and Drugs , bind. 9, Merck ,1976, 9. th ed. , 1835 s. ( ISBN 978-0-911910-26-1 ).
- (en) U. Dahlmann og GM Schneider , " (flydende + flydende) faseækvivalenter og kritiske kurver af (ethanol + dodecan eller tetradecan eller hexadecan eller 2,2,4,4,6,6,8,8-heptamethylnonan) fra 0 , 1 MPa til 120,0 MPa ” , J. Chem. Termodynamik. , Vol. 21, nr . 9,September 1989, s. 997–1004 ( ISSN 0021-9614 , DOI 10.1016 / 0021-9614 (89) 90160-2 ).
- (in) C. Reichardt og T. Welton , opløsningsmidler og opløsningsmiddeleffekter i organisk kemi , Weinheim, Wiley-VCH ,2010, 4 th ed. , 692 s. ( ISBN 978-3-527-32473-6 , DOI 10.1002 / 9783527632220 , online præsentation ) , “Tillæg” , s. 568.
- (en) JE Logsdon , Kirk-Othmer Encyclopedia of Chemical Technology , John Wiley & Sons ,2004( ISBN 978-0-471-23896-6 , DOI 10.1002 / 0471238961.0520080112150719.a01.pub2 , læs online ) , "Ethanol".
- (en) MJ Costigan , LJ Hodges et al. , “ Det isotermiske forskydningskalorimeter: Designmodifikationer til måling af eksotermiske enthalpier af blanding ” , Aust. J. Chem. , Vol. 33, nr . 10,1980, s. 2103-2119 ( ISSN 0004-9425 , DOI 10.1071 / CH9802103 ).
- (i) RW Rousseau , Handbook of Separation Process Technology , John Wiley & Sons ,1987, 1010 s. ( ISBN 978-0-471-89558-9 , læs online ) , s. 261-262.
- J. Vidal , termodynamik: anvendelse til kemisk teknik og olieindustrien , Paris, Éditions Technip ,1997, 500 s. ( ISBN 978-2-7108-0715-5 , LCCN 97194455 , læs online ) , s. 181.
- (i) J. Thomson , " er nogle nysgerrige bevægelser, der kan observeres på overfladerne af vin og andre alkoholholdige væsker " , Philos. Mag. , Vol. 10,1855, s. 330-333 ( læs online ).
- (en) GA Mills og EE Ecklund , " Alkoholer som komponenter i transportbrændstoffer " , Annu. Rev. Energi Ca. , Vol. 12,November 1987, s. 47-80 ( DOI 10.1146 / annurev.eg.12.110187.000403 ).
- (en) PB Morais , CA Rosa et al. , “ Produktion af brændstofalkohol ved Saccharomyces-stammer fra tropiske levesteder ” , Biotechnol. Lett , vol. 18, nr . 11,1996, s. 1351-1356 ( ISSN 0141-5492 , DOI 10.1007 / BF00129969 ).
- (i) PC Badger , J. Janick ( red. ) Og A. Whipkey ( red. ), Trends i nye afgrøder og nye anvendelser , Alexandria, VA, ASHS Press,2002, 599 s. ( ISBN 978-0-09-707565-5 , læs online ) , “Ethanol fra cellulose: En generel gennemgang” , s. 17–21.
- (in) MJ Taherzadeh og K. Karimi , " Syrebaserede hydrolyseprocesser for ethanol fra lignocellulosematerialer: En gennemgang " , BioRes. , Vol. 2 n o 3,2007, s. 472-499 ( ISSN 1930-2126 , læs online ).
- (in) MJ Taherzadeh og K. Karimi , " Enzymbaserede hydrolyseprocesser for ethanol fra lignocellulosematerialer: En gennemgang " , BioRes. , Vol. 2, nr . 4,2007, s. 707-738 ( ISSN 1930-2126 , læs online ).
- (in) SK Ritter , " Biomasse guld burst: Teknologi til at bruge planteafledt sukker til at producere kemiske råvarer er klar og venter ... " , Chem. Eng. Nyheder , vol. 82, nr . 22,Maj 2004, s. 31-34 ( ISSN 0009-2347 , læs online ).
- (in) " Brew Better Ethanol " på Popular Science Online ,2006(adgang til 18. maj 2012 ) .
- (in) DR Lide ( red. ), CRC Handbook of Chemistry and Physics , Boca Raton, FL, CRC Press ,2007, 88 th ed. , 2640 s. ( ISBN 978-0-8493-0488-0 ) , kap. 8 ("Analytisk kemi") , s. 42.
- (i) HD Hinton og JA Nieuwland , " Organic Reagerer med Boron Fluor. I. Fremstilling af estere ” , J. Am. Chem. Soc. , Vol. 54, nr . 5,1932, s. 2017–2018 ( ISSN 0002-7863 , DOI 10.1021 / ja01344a046 ).
- (in) " Rulemaking History for OTC Sweet Spirits of Nitre Drug Products " om Food and Drug Administration (adgang til 22. maj 2012 ) .
- (in) K. Schumann og K. Siekmann , Ullmann's Encyclopedia of Industrial Chemistry , Wiley-VCH Verlag ,2000( ISBN 978-3-527-30673-2 , online præsentation ) , "Sæber".
- Lide, 2007 , kap. 5 ("Termokemi, elektrokemi og kinetik"), s. 70.
- Lide, 2007 , kap. 15 (“Praktiske laboratoriedata”), s. 17 .
- (in) R. Swift og D. Davidson , " Alkohol Hangover: Mechanisms and Mediators ' , Alcohol Health Res. W. , bind. 22, nr . 1,1998, s. 54-60 ( læs online ).
- (i) L. Hipolito , J. Sanchez et al. , " Brain Metabolism of Ethanol and Alcoholism: An Update " , Curr. Drug Metab , vol. 8, n o 7,oktober 2007, s. 716-727 ( ISSN 1389-2002 , PMID 17979660 , DOI 10.2174 / 138920007782109797 ).
- (pdf) Toksikologisk ark nr. 120 fra INRS, konsulteret den 24. juni 2017
- Juan I. Garaycoechea & al. (2018) Alkohol og endogene aldehyder beskadiger kromosomer og muterer stamceller | Nature | doi: 10.1038 / nature25154 | offentliggjort online 3. januar 2018 | abstrakt
- (i) L. Kurti og B. Czako , Strategiske Applications of Navngivne Reaktioner i Organisk syntese , Academic Press ,2005, 864 s. ( ISBN 978-0-12-369483-6 , online præsentation ) , s. 264-265.
- GS Serullas , “ Carbonhydriodide . Særlige omstændigheder, hvor denne tredobbelte kombination fandt sted; måde at producere det med det samme ”, Annal. Chim. Phys. , Vol. 20,Maj 1822, s. 17-37 ( læs online ).
- " Den seneste ændring af superethanol E85..N645843 " , på usinenouvelle.com .
- (i) G. McDonnell og AD Russell , " Antiseptika og desinfektionsmidler: Aktivitet, handling og modstand " , Clin. Mikrobiol. Rev. , Vol. 12, n o 1,1999, s. 147–179 ( ISSN 0893-8512 , PMCID PMC88911 , læs online [PDF] ).
- (en) DG Barceloux , GR Bond et al. , " American Academy of Clinical Toxicology Practice Guidelines on the Treatment of Methanol Poisoning " , Clin. Toxicol. , Vol. 40, nr . 4,2002, s. 415-446 ( DOI 10.1081 / CLT-120006745 ).
- (i) YB Shvets , Washington station: Mit liv som KGB spion i Amerika , New York, Simon & Schuster ,1995, 298 s. ( ISBN 978-0-671-88397-3 ).
- (in) " V2 " om raket- og rumteknologi (adgang til 27. maj 2012 ) .
- (i) " Rocket Propellants " , på Internet Encyclopedia of Science (adgang 27. maj 2012 ) .
- (in) " A Brief History of Rocketry " på Kennedy Space Center (adgang til 27. maj 2012 ) .
- (i) LA Pohorecky og J. Brick , " Pharmacology of Ethanol " , Pharmacol. Ther. , Vol. 36, n knogle 2-3,1988, s. 335–427 ( ISSN 0163-7258 , PMID 3279433 , DOI 10.1016 / 0163-7258 (88) 90109-X ).
- (i) " Ethanolum anhydricum " om det europæiske direktorat for lægemiddelkvalitet (adgang til 28. maj 2012 ) .
- (i) DJ Nutt , THE Kong et al. , “ Stoffskader i Storbritannien: en analyse af flere kriterier ” , Lancet , vol. 376, nr . 9752,6. november 2010, s. 1558-1565 ( ISSN 0140-6736 , DOI 10.1016 / S0140-6736 (10) 61462-6 ).
- (da) DA Yost , “ Akut pleje af alkoholforgiftning. Vær forberedt på at overveje kliniske dilemmaer ” , Postgrad Med. , Vol. 112, nr . 6,2002, s. 14-26 ( ISSN 0032-5481 , PMID 12510444 , DOI 10.3810 / pgm.2002.12.1361 ).
- (i) V. Santhakumar , Mr. Wallner et al. , “ Ethanol virker direkte på ekstrasynaptiske undertyper af GABA A- receptorer for at øge tonisk inhibering ” , Alkohol , bind. 41, n o 3,Maj 2007, s. 211–221 ( ISSN 0741-8329 , PMID 17591544 , PMCID PMC2040048 , DOI 10.1016 / j.alkohol.2007.04.011 , læs online ).
- Virgolini, MB, Mattalloni, MS, Deza-Ponzio, R., Albrecht, PA og Cancela, LM (2019). Blyeksponering og indtag af ethanol: Oxidativ stress som en konvergerende handlingsmekanisme . I Neuroscience of Alcohol (s. 515-525). Academic Press ( abstrakt ).
- (en) Fein G, D Greenstein, Cardenas VA, Cuzen NL, Stein DJ et al. , " Kortikale og subkortikale volumener hos unge med alkoholafhængighed, men uden substans eller psykiatriske comorbiditeter " , Psychiatry Res , bind. 214, nr . 1,2013, s. 1-8. ( PMID 23916536 , PMCID PMC4203651 , DOI 10.1016 / j.pscychresns.2013.06.001 , læs online [html] )
- (in) Little G, P Maurage, Kornreich C Verbanck P, S Campanella, " Binge drinking in adolescent: a review of neurophysiological and neuroimaging research " , Alcohol Alcohol , vol. 49, nr . 22014, s. 198-206. ( PMID 24302160 , DOI 10.1093 / alcalc / agt172 , læs online [html] )
- (en) K. Nakamura , K. Iwahashi et al. , " Acetaldehyd-addukter i alkoholikernes hjerne " , Arch. Toxicol. , Vol. 77, nr . 10,2003, s. 591-593 ( ISSN 0340-5761 , DOI 10.1007 / s00204-003-0465-8 ).
Se også
Bibliografi
- (en) JE Logsdon , Kirk-Othmer Encyclopedia of Chemical Technology , John Wiley & Sons ,2004( ISBN 978-0-471-23896-6 , DOI 10.1002 / 0471238961.0520080112150719.a01.pub2 , læs online ) , "Ethanol".
- (en) LA Pohorecky og J. Brick , " Pharmacology of ethanol " , Pharmacol. Ther. , Vol. 36, n knogle 2-3,1988, s. 335–427 ( ISSN 0163-7258 , PMID 3279433 , DOI 10.1016 / 0163-7258 (88) 90109-X ).
Relaterede artikler
- Andre alkoholer: Alkohol , Primær alkohol , Methanol , Propanol og Butanol
- Egenskaber: Absolut alkohol , methyleret spiritus , denatureret alkohol og rektificeret alkohol
- Produktion: Alkoholisk gæring , Celluloseethanol
- Anvendelse: Alkohol , Bioethanol , Alkoholholdig drik , Spiritus , Alkoholindustri
- Historie: Historien om øl , historie vinstokke og vin
- Fysiologiske egenskaber: Alkohol-dehydrogenase , Alcoholemia , alkoholisme , tømmermænd , alkoholforgiftning , Føtalt alkohol syndrom
- Diverse: Beregning af alkoholtitler og -volumener , Graden af alkohol , Tårer af vin , Alkoholisk maceration










