Sulfurylchlorid
| Sulfurylchlorid | |
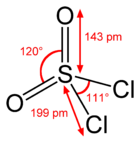  Struktur af sulfurylchlorid |
|
| Identifikation | |
|---|---|
| IUPAC navn | Sulfurylchlorid |
| Synonymer |
Svovlklorid |
| N o CAS | |
| N o ECHA | 100.029.314 |
| N o EF | 232-245-6 |
| Kemiske egenskaber | |
| Brute formel | SO 2 Cl 2 |
| Molar masse | 134,97 ± 0,01 g / mol Cl 52,53%, O 23,71%, S 23,76%, |
| Fysiske egenskaber | |
| T ° fusion | −54,1 ° C |
| T ° kogning | 69,4 ° C |
| Volumenmasse | 1667 kg · m -3 til 20 ° C |
| Forholdsregler | |
| Direktiv 67/548 / EØF | |
 VS Indeksnummer : Symboler : C : Ætsende R-sætninger : R14 : Reagerer voldsomt med vand. R34 : Forårsager forbrændinger. R37 : Irriterer luftvejene. S-sætninger : S26 : I tilfælde af kontakt med øjnene, skylles straks med rigeligt vand og læge kontaktes. S45 : I tilfælde af et uheld eller hvis du føler dig utilpas, søg straks lægehjælp (vis etiketten, hvor det er muligt). (S1 / 2) : Opbevares låst og utilgængeligt for børn. R-sætninger : 14, 34, 37, S-sætninger : (1/2), 26, 45, |
|
| Enheder af SI og STP, medmindre andet er angivet. | |
Den sulfurylchlorid er en uorganisk forbindelse af familien af oxider , af formlen SO 2 Cl 2. Det fremstår som en farveløs væske med en skarp lugt. Det findes ikke i naturen på grund af dets meget hurtige hydrolyse .
Det forveksles ofte med thionylchlorid SOCl 2, Men disse to svovl oxychlorider har forskellige egenskaber: thionylchlorid producerer chlorid ioner Cl - mens sulfurylchlorid giver chlor Cl 2.
Forberedelse og reaktioner
Sulfurylchlorid fremstilles ved omsætning af svovldioxid SO 2og chlor Cl 2i nærværelse af en katalysator , såsom aktivt kul :
SO 2+ Cl 2→ SO 2 Cl 2.Det opnåede produkt kan derefter renses ved fraktioneret destillation .
Sulfurylchlorid reagerer voldsomt med vand frigiver hydrogenchlorid HCI og giver svovlsyre H 2 SO 4 :
2 H 2 O+ SO 2 Cl 2→ 2 HCI + H 2 SO 4Det nedbrydes under varme omkring 100 ° C eller ca. 30 ° C over kogepunktet. Det nedbrydes også langsomt ved stuetemperatur til opnåelse af svovldioxid SO 2og chlor Cl 2ved oprindelsen af den svagt gule nuance af sulfurylchloridprøverne, som har haft tid til at "aldre".
Ansøgninger
For så vidt som sulfurylchlorid er flydende, findes det mere bekvemt at håndtere end klor , som er gasformigt, hvilket gør dets anvendelse som en klorkilde let at transportere, opbevares og måles. Det bruges også til at chlorinere alkaner , alkener , alkyner , arener og epoxider ifølge radikale reaktioner initieret af AIBN . Det kan også omdanne alkoholer til organiske klorer .
I industrien anvendes sulfurylchlorid hovedsageligt til fremstilling af pesticider.
sikkerhed
Sulphurylchlorid er giftigt, ætsende og tåregas. Den kan danne eksplosive blandinger med vand samt med dimethylsulfoxid O = S (CH 3 ) 2(DMSO) og dimethylformamid OHC - N (CH 3 ) 2 (DMF).
Noter og referencer
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .