Borsyre
| Borsyre | |
 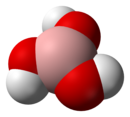 Repræsentationer af borsyremolekylet |
|
| Identifikation | |
|---|---|
| IUPAC navn |
borsyre hydrogen borat |
| Synonymer |
boracinsyre |
| N o CAS | |
| N o ECHA | 100.030.114 |
| N o EF | 233-139-2 |
| ATC-kode | S02 |
| PubChem | 7628 |
| ChEBI | 33118 |
| N o E | E284 |
| SMILE |
B (O) (O) O , |
| InChI |
InChI: InChI = 1 / BH3O3 / c2-1 (3) 4 / h2-4H InChIKey: KGBXLFKZBHKPEV-UHFFFAOYAI Std. InChI: InChI = 1S / BH3O3 / c2-1 (3) 4 / h2-4H Std. InChIKey: KGBXLFKZBHKPEV-UHFFFAOYSA-N |
| Udseende | farveløse krystaller eller lugtfrit hvidt pulver |
| Kemiske egenskaber | |
| Brute formel |
H 3 B O 3 [isomerer] |
| Molar masse | 61,833 ± 0,008 g / mol H 4,89%, B 17,48%, O 77,63%, |
| pKa | 9,28 til 24,85 ° C for B (OH) 3 / B (OH) 4 - , derefter 10,7 og 13,8 for de sidste to syrebasepar |
| Fysiske egenskaber | |
| T ° fusion | transformation ved orden 2 overgang mellem 169 ° C og 171 ° C i metaborsyre HBO 2 , sønderdeling ved 185 ° C , dannelsen af B 2 O 3 ved 300 ° C |
| Opløselighed | 47,2 g · l -1 (vand, 20 ° C ) |
| Volumenmasse | 1,435 g · cm -3 til 15 ° C |
| Mættende damptryk | 2,7 mbar ved 20 ° C |
| Termokemi | |
| S 0 gas, 1 bar | 295,23 J mol −1 K |
| S 0 fast | 88,7 J mol −1 K |
| Δ f H 0 gas | - 992,28 kJ mol −1 |
| Δ f H 0 faststof | - 1093,99 kJ mol −1 |
| Krystallografi | |
| Krystal system | triklinik |
| Optiske egenskaber | |
| Brydningsindeks | polyaksiale krystaller, dvs. 1,337, 1,461 og 1,462 |
| Forholdsregler | |
| SGH | |
 Fare H360FD, H360FD : Kan skade fertiliteten. Kan skade det ufødte barn. |
|
| WHMIS | |
 D2A, D2A : Meget giftigt materiale, der forårsager andre toksiske virkninger Oplysning om 0,1% ifølge klassificeringskriterier |
|
| Hud | mulige irritationer |
| Øjne | mulige irritationer |
| Indtagelse | Giftig. Opkastning og diarré i små doser, dødelig i høje doser |
| Enheder af SI og STP, medmindre andet er angivet. | |
Den borsyre , også kaldet syre boracic eller syre orthoboric er et organ uorganisk forbindelse med den empiriske formel H 3 BO 3 eller B strukturelle (OH) 3 , tidligere kaldet sassoline i det centrale Italien , opstår det naturligt i varme fumaroler og indskud med andre kondenserede dampe i lagoni i Toscana . Dette hvide faste stof, nogle gange let farvet, krystalliserer i et trikliniknetværk . Det er i form af et fast krystalliseret i perleflager.
Temmelig let opløseligt i vand, det er en svag syre . Det bruges ofte som antiseptisk, selvom det er giftigt, insekticid , neutronabsorber i atomkraftværker for at kontrollere fissionshastigheden af uran og som en forløber for andre kemiske forbindelser. Denne Lewis-syre tager sit navn fra en af dens komponenter, bor , dens rå formel er H 3 BO 3 eller bedre med at strukturen med kovalente bindinger B (OH) 3 .
Molekylær borsyre kan komme fra den enkle nedbrydning af det naturlige mineral kaldet sassolit, som beskrevet af sin formel B (OH) 3, er kun en samling plan af borsyre stabiliseret ved hydrogenbindinger. Det eksisterer som farveløse krystaller eller som et hvidt pulver, der opløses i vand .
Fremstilling
Borsyre fremstilles primært af boratmalm ved omsætning med svovlsyre . Den største kilde til borater i verden er en åben mine i Boron (i) .
Borsyre blev først produceret af Wilhelm Homberg (1652-1715) fra borax under indvirkning af mineralsyrer og fik navnet "sal sedativum Hombergi" .
I naturen
Fri syre er til stede i nativ eller regenereret form i nogle områder med granitbadolitter tæt på overfladen såsom Toscana, Lipari-øerne og Nevada, dens spildevand blandes med damp fra revner i jordskorpen. I Toscana udvindes borsyre i stråler med overophedet damp ( 100 til 215 ° C ) af vulkansk oprindelse, der bruges som energikilde; dampen, der hydrolyserer borater i dybden af jorden i denne region, indeholder faktisk borsyre og forskellige mineralsalte. Det, der frit slipper væk fra revner i jorden (soffioni), kondenseres simpelthen i bassiner (lagoni).
Tilstedeværelsen af borsyre eller dens salte er blevet påvist i havvand og ville også eksistere i planter og især i næsten alle frugter, hvor det kunne spille en bestemt rolle som naturligt insekticid.
Borsyre er det ultimative nedbrydningsprodukt (ofte ved hjælp af en stærk syre) af mange borater: borax , boracit , boronatrocalcit , colemanit , borocalcite, ascharit , kaliborit, kernit , kurnakovit , pinnait, pandermit , tunellit , larderellit, probertit, inderit , hydroboracit , etc. , men også howlit og bakerit, ud over mineraler, som delvis kan indeholde borsyre, såsom harkerit eller sassolit .
Ejendomme
Fortyndet i vand kaldes borsyre, en meget svag syre, boreret vand.
Opløselighed
Borsyre er ret dårligt opløseligt i koldt vand.
| Opløst masse (g) pr. 100 g vand |
Temperatur |
|---|---|
| 2.66 | 0 ° C |
| 3.57 | 10 ° C |
| 5,04 | 20 ° C |
| 6.6 | 30 ° C |
| 8,72 | 40 ° C |
| 11.54 | 50 ° C |
| 14,81 | 60 ° C |
| 16,73 | 70 ° C |
| 23,75 | 80 ° C |
| 30.38 | 90 ° C |
| 40,25 | 100 ° C |
Borsyre er meget mere opløselig i varmt vand og især i kogende vand. I vand ved almindelig temperatur opløses det under forudsætning af, at det deles fint op til et borindhold tæt på 4000 ppm, hvor begyndelsen af krystallisation observeres.
Borsyre er opløselig i glycerol (glycerin), eller 22,2 g til 100 g af opløsningsmiddel ved 20 ° C og 28 g ved 25 ° C . Det er også opløseligt i methanol , eller 20,2 g til 100 g ved 25 ° C . Det er markant mindre i ethanol ( 5,5 g pr. 100 g ved 25 ° C ), i ethylether ( 0,24 g pr. 100 g ved 25 ° C ). Det er uopløseligt i acetone .
Kemi
(Ortho) borsyre er fremstillet af kæde- eller cykliske (meta) borater , især borax . Det er faktisk nedbrydningsreaktioner med saltsyre og svovlsyre, der danner borsyre.
Borsyre er også produktet af hydrering af bor sesquioxide , en svag monobasinsyre, nemlig:
B 2 O 3 fast pulver + 3 H 2 O → 2 B (OH) 3 aq Syre-base ejendomBorsyre er en Lewis-syre , den accepterer elektroner fra hydroxylioner, derfor fanger den sidstnævnte ved at danne ioniske strukturer: tetraeder, pentakoordineret eller bipyramid geometrisk struktur, hexakoordineret struktur osv.
Således dissocieres borsyre ikke i vandig opløsning, men dens sure aktivitet skyldes dens interaktion med vandmolekyler:
B (OH) 3 + H 2 O → B (OH) 4 - + H + K a = 5,8 × 10 -10 mol / L ; pK a = 9,14.Polyboratanioner dannes langsomt ved pH 7,10, hvis borkoncentrationen er over 0,025 mol / L. Den bedst kendte af disse er tetraborationen med en cyklisk struktur, der findes i mineralet borax:
4B (OH) 4 - + 2H + → B 4 O 7 2− + 9H 2 OSammenfattende er borsyre i det væsentlige en svag monobasisk syre. Det er muligt at skrive, med konventionen sletning et vandmolekyle H 2 0 eller H 2 BO 3 - vandig for tetrahydroxyborate ion B (OH) 4 - , syre-base ligevægte:
H 3 BO 3 vandig → H + vandig + H 2 BO 3 - vandig H 2 BO 3 - vandig → H 2 O + BO 2 - vandigBorsyre kan bestemmes som standard med en natriumhydroxidopløsning, afhængigt af reaktionsdannende natriummetaborat, natriumsaltet af metaborinsyre :
H 3 BO 3 vandig + NaOH vandig → NaBo 2 vandig + 2H 2 ODenne dosering kan forbedres ved tilsætning til borsyreopløsningen af polyhydroxylerede organiske forbindelser af glycerol , mannitoltype , forskellige sukkerarter osv. , som øger styrken af borsyren og giver mulighed for i praksis bedre at kende med præcision slutningen af doseringen.
Kemi ved kogepunktet for vand og deroverOparbejdet og opbevaret ved kogepunkt ved 100 ° C , giver den vandige opløsning af borsyre et aflejr af metaborinsyre , her skrevet med en forenklet ækvivalent formel:
B (OH) 3 aq kogende → HBO 2 + H 2 O gasVed opvarmning til rødt omdannes metaborinsyre til boresquioxid og mister ækvivalenten med et vandmolekyle.
2 HBO 2 rødt opvarmet fast stof → B 2 O 3 fast stof + H 2 O gasSaltene af borsyre er komplekse.
På grund af en strukturel transformation ved en gradvis overgang initieret mellem 169 ° C og 171 ° C og generelt afsluttet omkring 185 ° C , dehydrerer tørt borsyre, der danner metaborinsyre HBO 2 . Den metaborsyre er en kubisk krystal, hvid og svagt opløseligt i vand. Det smelter ved omkring 236 ° C, og når det opvarmes over 300 ° C , dehydrerer det og danner tetraborinsyre eller pyroborinsyre, H 2 B 4 O 7 . Udtrykket borsyre kan henvise til en hvilken som helst af disse forbindelser. Ved en lidt højere temperatur dannes bor sesquioxide .
Toksicitet, økotoksicitet
- Tidligere ofte præsenteret som lidt mere giftigt end bordsalt (baseret på den anslåede dødelige dosis på 2660 mg · kg -1 kropsvægt) for mennesker, det har fungicid og insekticid aktivitet, hvilket antyder, at 'det ikke ville være neutralt for miljøet i i tilfælde af betydelig forurening.
- Giftig for mennesker (ifølge INRS for eksempel) ved fordøjelsesvej eller ved indånding. ANSM og lægemiddelovervågningscentre har advaret om den reprotoksiske natur såvel som for den akutte toksicitet. Nogle etniske grupper bruger det som et fødevaretilsætningsstof til mennesker eller kæledyr, men i Canada beder CFIA opdrættere og restauratører om ikke at bruge det på grund af "uacceptabel risiko for forbrugernes sundhed." (På grund af dødsfald blandt voksne eller babyer). I Frankrig på apoteker kræver brugen af borsyre arbejde under en hætte med handsker, briller og maske.
- I høje koncentrationer er det irriterende for øjnene, huden og luftvejene - i tilfælde af eksponering, endda kort - og det kan have virkninger på nyrerne i tilfælde af langvarig eller gentagen eksponering.
Der vides ikke meget om dets miljømæssige toksicitet, bortset fra insekter, mod hvilke det bruges som et insekticid, der er godkendt til visse anvendelser i visse lande. Insekter bliver forurenet ved at rense sig selv efter kontakt med dette produkt. Det virker på deres mave og fører til insektets død om cirka ti dage. Dens effektivitet vedvarer i flere år på tørre steder.
- Det er klassificeret reprotoksisk 2 (CMR) af Det Europæiske Fællesskab. Hans ansættelse er nu reguleret.
Anvendelser
I landbruget
Borsyre og salte deraf anvendes som gødning i konventionelt og organisk landbrug. Den bor-mangel er den mest almindelige mikronæringsstofmangel i verden og forårsager betydelige udbyttetab i kulturplanter og frugttræer.
I medicin og biologi
AntiseptiskDet kan bruges som et antiseptisk middel mod forbrændinger eller udskæringer og bruges undertiden i salver og salver eller bruges i en meget fortyndet opløsning som et øjenbad ( borvand ). Som en antibakteriel forbindelse kan borsyre også ordineres som en behandling for acne . Det bruges stadig som et antiseptisk middel til øret ved dykning med en dråbe på 2% boralkohol pr. Øre. Sodiumborat, et mildt antiseptisk middel, sammen med andre egnede komponenter kan også tilbydes til ekstern brug til øjensygdomme, såsom tørre øjne.
AntimykotiskBorsyre kan anvendes til behandling af gær og gær infektioner såsom candidiasis (vaginal gær infektion) ved at fylde æg med borsyrepulver der vil blive indsat i den vaginale hulhed ved sengetid i tre til fire på hinanden følgende nætter. I opløsning kan det ordineres til behandling af visse former for otitis externa ( øreinfektion ) hos mennesker eller dyr. Konserveringsmidlet i urinflasker (rød hætte) i Storbritannien er borsyre.
Det bruges også til forebyggelse af fodsvamp ved at indsætte pulveret i sokker eller strømper.
BufferopløsningDen lithium borat er saltet af lithium borsyre anvendes i laboratoriet som pufferopløsning til gel almindeligvis anvendes i elektroforesebuffer nukleinsyrer (såsom puffer TBE , SB og LB). Det kan bruges til elektroforese af DNA og RNA ved gel polyacrylamid og agarosegel .
InsekticidBorsyre bruges også ofte som et relativt lavtoksisk insekticid til udryddelse af kakerlakker , termitter , myrer , lopper og mange andre insekter . Det kan bruges direkte som et pulver til lopper og kakerlakker eller blandet med sukker eller gelé til myrer. Det er også en komponent i mange kommercielle insekticider . I denne anvendelse, især i tilfælde af kakerlakker, påføres borsyre i pulverform på områder, der besøges af insekter. De fine partikler klæber sig til insektbenene og forårsager efterfølgende livsfarlige kemiske forbrændinger. Borsyre markedsføres til denne anvendelse i boligområder i byområder inficeret med kakerlakker.
I den nukleare industri
Den bor har en høj kapacitet for at absorbere neutroner , men med den ulempe, at ud over en vis grænse, hvilket øger risikoen for radiolyse af vand.
- Som neutron absorber , tilsættes det i opløsning i form af borsyre til vandet i det primære kredsløb , som passerer gennem reaktoren af kernekraftværker , for at absorbere overskydende neutroner for at undgå enhver reaktion runaway (reaktioner kæde fission bestemmes i det væsentlige af mængden af tilstedeværende neutroner; neutroner fra tidligere fissioner). Den nøjagtige kontrol af niveauet af borsyre i vandet i det primære kredsløb er den vigtigste måde at kontrollere den grundlæggende reaktivitet af reaktoren under cyklussen. Borsyre tilsættes i begyndelsen af cyklussen, når reaktoren (re) starter op med nyt brændstof (i stand til at producere flere fissioner) og trækkes gradvist ud af det primære kredsløb, når brændstoffet bliver opbrugt i fissilt materiale.
- Af samme grund og i samme form, er det sprøjtes ind i storage pools indeholdende de brugt kernebrændsel samlinger , med en koncentration, som skal være tilstrækkelig til at opretholde puljen i sub- kritikalitet .
- Borsyre blev også brugt under den nukleare ulykke i Tjernobyl (26. april 1986). 40 tons blev droppet med helikopter i løbet af de første 11 dage efter katastrofen i flammerne for at begrænse spredning af stråling.
- Bor må ikke være til stede i store mængder, fordi det ud over en bestemt tærskel, der varierer alt efter temperaturen, trykket, den kemiske sammensætning og radioaktiviteten af vandet, forværrer vandets radiolysis (selv når denne radiolysis hæmmes ved tilsætning af hydrogen ved at vide, at denne inhibering er meget følsom over for brintkoncentrationen, men også for vandets temperatur, for strålingen og for den mulige tilstedeværelse af kemiske urenheder, f.eks. som følge af korrosion, som i sig selv kan forværres af radiolysis).
"En meget let ændring af en af disse parametre, når man er tæt på tærsklen, kan pludselig skifte radiolys af vand" . Borsyre anvendes traditionelt , men over en vis koncentration (tærskelværdi varierende i henhold til forskellige parametre inklusive temperatur og tryk) accelereres nedbrydningen af vand pludselig, "med dannelsen af hydrogen, d oxygen og hydrogenperoxid. Denne pludselige fænomen skyldes forgiftning af rekombinante kædereaktion H 2 og H 2 O 2. I nogle tilfælde er en mætning fænomen observeret: når koncentrationerne af O 2 og H 2 O 2øges for meget, stopper kædereaktionen. Denne mætning blev bekræftet af computersimuleringer ” .
Andet
Den borat og borsyre blev anvendt:
- fra det antikke Grækenlands periode til rengøring, konservering af mad og andre aktiviteter;
- i smykker industrien og traditionel lodning (VVS), har borsyre været eller er stadig anvendes i kombination med denatureret alkohol for at reducere overflade oxidation og graden af oxidation på metaller i løbet metallurgi og svejseoperationer ;
- den forseglende silikone blev oprindeligt fremstillet ved tilsætning af borsyre til silikoneolie . Nu indeholder mastikken, der markedsføres under forskellige mærker, også betydelige mængder af elementet silicium (silicium bundet til silikone gør det muligt at øge produktets elasticitet med 20%);
- borsyre bruges almindeligvis af amatørpyroteknikere - i opløsning i alkohol - for at give flammen en lysegrøn farve og for at forhindre amiddannelse under reaktionen mellem aluminium og nitrater: en smule borsyre tilsættes til sammensætningen for at neutralisere alkaliske amider, som kan reagere med aluminium ;
- det bruges også i Indien og overalt i verden til at slå støv ned på sportsbaner , for at mindske friktion og for at øge hastigheden i spillet med indisk billard ;
- som et biocid til behandling af poolvand, hvor det er en del af sammensætningen af langt størstedelen af klortabletter.
Forskrifter
Siden 2010 er dets markedsføring og anvendelse blevet reguleret i Europa til fordel for alternative produkter på grund af dets CMR - reproduktionstoksiske klassificering og dets integration i REACH- forordningen .
eksterne links
- International sikkerhedsdatablad
- Toksikologisk ark , INRS
- Anbefalinger , ANSM
- (en) ChemSub Online: Borsyre
Bibliografi
- Bilag XV overgangsrapporter. Borsyre , ECHA , 2008
- Borsyre , ECHA
Noter og referencer
- borsyre, sikkerhed ark (e) af det internationale program for sikkerhed for kemiske stoffer , hørt den 9. maj 2009
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- Indtastning "Borsyre" i den kemiske database GESTIS fra IFA (tysk organ med ansvar for arbejdsmiljø) ( tysk , engelsk ), adgang til 2. august 2010 (JavaScript nødvendigt)
- " CAS-registreringsnummer: 10043-35-3 " på ntp.niehs.nih.gov (adgang til 27. november 2009 )
- " Borsyre " i databasen over kemiske produkter Reptox fra CSST (Quebec-organisation med ansvar for sikkerhed og sundhed på arbejdspladsen), adgang til den 25. april 2009
- Sassolin kan således betegne så meget hydreret borsyre fra afkølede laguneaflejringer som borsyre opløst i varmt vand eller de forskellige stabile borater fordampet i overophedede dampe og fumaroler. Navnet borsyre blev foreslået af de franske kemikere Gay-Lussac og Thénard omkring 1810 [Fysisk-kemisk forskning udført på Davy-bunken (... og nedbrydning af boracinsyre), Bulletin de Pharmacy , bind 3, D. Colin , 1811, s. 221-225 ]. Det har fortrængt især boracinsyre og især en lang række andre med farlige indikationer, vitriol og andre, som tidligere eksisterede.
- Sassolit kunne tidligere skrives med den rå formel B 2 O 3 3 H 2 O, i virkeligheden dobbelt. Det er fortsat dets vigtigste direkte mineral , men det er muligt at opnå borsyre ved at behandle et stort antal borater.
- AH Allen, analytiker , 1904, 301
- Perrys Chemical Engineers' Handbook , 6 th ed.
- Bor er en umættelig elektronacceptor modsætning carbon, der adskiller deres to kemier med kovalente bindinger.
- Den rå molekylformel svarer til en tredobling af stof.
- " Pharmacovigilance - Borsyre og derivater (borax) " , på www.pharmacovigilance-tours.fr (adgang 20. maj 2017 )
- Canadian Food Inspection Agency - Kontoret for fødevaresikkerhed og forbrugerbeskyttelse - Brev til industrien - Borax (borsyre) solgt eller præsenteret som mad
- " US Borax: Banebrydende for elementerne i moderne liv med raffineret bor " , på farming.borax.com (adgang til 8. oktober 2020 ) .
- (i) DD-Camacho Cristobal J. Rexach González og A. Fontes, " Boron i planter: Deficiency og toksicitet " , Journal of Integrative Plant Biology , vol. 50,2008, s. 1247-1255 ( DOI 10.1111 / j.1744-7909.2008.00742.x ).
- B. Hickel, "La radiolysis de l'eau" , Phases Magazine , CEA / DSM, La lettre du DRECAM et du SPht nr . 17, december 1997
- T. Stolz, D. Ducret, S. Heinze, G. Baldacchino, J.-C. Colson, B. Dedieu, Th. Pelletier, Selvradiolysis af tritieret vand , Fusion Engineering and Design, bind. 69, nummer 1-4, september 2003, s. 57-60 , 22 nd symposium om Fusion Technology, DOI : 10,1016 / S0920-3796 (03) 00.236-9 ( abstrakt )