Butansyre
| Butansyre | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikation | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC navn | Butansyre | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
smørsyre |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.003.212 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EF | 203-532-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB03568 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2221 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILE |
CCCC (= O) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C4H8O2 / c1-2-3-4 (5) 6 / h2-3H2,1H3, (H, 5,6) / f / h5H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Udseende | farveløs, olieagtig væske med en karakteristisk lugt. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formel |
C 4 H 8 O 2 [isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar masse | 88,1051 ± 0,0044 g / mol C 54,53%, H 9,15%, O 36,32%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekylær diameter | 0,560 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusion | −7,9 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kogning | 164 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighed | i vand: blandbar, blandbar med ethanol , ether |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighedsparameter δ |
21,5 MPa 1/2 ( 25 ° C ); 25,1 J 1/2 · cm -3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumenmasse |
0,959 g · ml -1 til 20 ° C 0,964 g · ml -1 til 25 ° C ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Automatisk tænding temperatur | 452 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | 72 ° C (lukket kop) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosionsgrænser i luft | 2 - 10 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mættende damptryk | ved 20 ° C : 57 Pa
ligning:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | 52,7 bar , 354,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
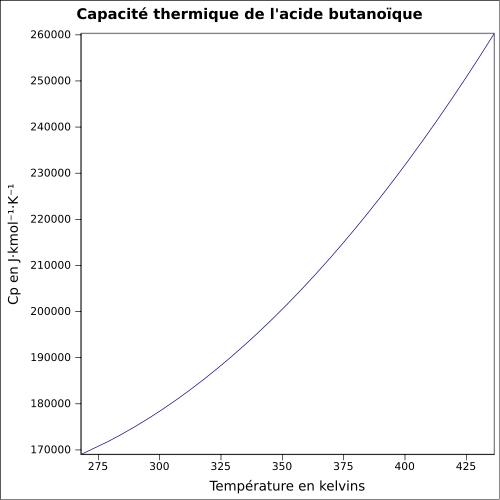
| C s |
ligning:
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ioniseringsenergi | 10,17 ± 0,05 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brydningsindeks | 1.398 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Fare H314, H314 : Forårsager svære forbrændinger af huden og øjenskader |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Uklassificeret produktKlassificeringen af dette produkt er endnu ikke valideret af Toxicological Directory Service Disclosure med 1,0% i henhold til listen over ingredienser |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 3 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2820 : BUTYRIC ACID |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Økotoksikologi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 8,79 g · kg -1 (rotter, oral) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 0,79 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheder af SI og STP, medmindre andet er angivet. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den butansyre , også kaldet smørsyre græsk βουτυρος ( smør ) er en carboxylsyre mættet med formlen CH 3 CH 2 CH 2 COOH
Det findes for eksempel i harskt smør , parmesan og gastrisk indhold , hvor det afgiver en stærk og ubehagelig lugt. Smørsyre kan ses fra omkring 5 til 40 pg / m 3 , afhængigt af kilden.
Under standardbetingelser , smørsyre er en lidt olieagtig væske, som størkner ved -8 ° C , og hvis kogepunkt er 164 ° C . Det er let opløseligt i vand , ethanol og ether og adskiller sig fra dets opløsningsmiddel ved tilsætning af calciumchlorid . Den kaliumdichromat og svovlsyre det oxidere i carbondioxid og eddikesyre , medens kaliumpermanganat alkalimetaloxid kun carbondioxid . Desuden dens isomer forfatning den 2-methylpropan , der skylder sit andet navn isosmørsyre.
Det er også en kortkædet fedtsyre, der findes i vegetabilske olier og animalsk fedt. Den glycerid ( ester af glycerol ) smørsyre omfatter 3% til 4% smør. Når smør bliver harsk, hydrolyseres glycerider , hvilket frigiver ubehagelig lugtende smørsyre. Normal smørsyre eller fermentering smørsyre findes også som en hexyl ester i olien af Heracleum giganteum og som en octyl ester i den for pastinak ( Pastinaca sativa ); det er også til stede i sved .
Det produceres normalt ved gæring af sukker eller stivelse forårsaget af tilsætning af rådnende ost , hvortil calciumcarbonat tilsættes for at neutralisere de syrer, der dannes i processen. Butyrisk gæring af stivelse letter ved direkte tilsætning af Bacillus subtilis .
Forskellige estere opnås fra smørsyre. Disse estere kaldes butyrat eller mere korrekt butanoat . Dem med lav molær masse, som methylbutanoat , har for det meste behagelige aromaer. De bruges således som tilsætningsstoffer til fødevarer eller i parfume.
Dens rå formel er den samme som for propylformiat .
Brug
Butansyre anvendes i fremstillingen af forskellige varianter ( butanoat estere ), lavmolekylær smørsyreestere, såsom methyl butanoat, har for det meste, behagelige aroma eller smag. Derfor bruges de som tilsætningsstoffer i mad og parfume.
Takket være sin stærke lugt bruges det også som tilsætningsstof til fiskeri agn. Mange smagsvarianter, der er tilgængelige på markedet for agn til almindelig karpe ( Cyprinus carpio ), bruger smørsyre som esterbase, men det er ikke klart, om fisk tiltrækkes af smørsyre i sig selv eller af andre tilsatte stoffer. Smørsyre er dog en af de få organiske syrer, der viser sig at være velsmagende for både tench og bille .
Anekdotisk er dette stof også blevet brugt som et ikke-toksisk, kvalme-fremkaldende, kød-ødelæggende hvalafstødende middel af Sea Shepherd-holdet mod de japanske hvalfangere fabriksskib og af anti-abortaktivister; nogle politistyrker overvejer også at vedtage det som et ikke-dødeligt våben .
Fremstilling af butyrater
Klassisk gæring
Butyrater eller korrekt butanoater, estere af butansyre, kommer fra gæringer, der involverer anaerobe bakterier . Denne proces blev opdaget af Louis Pasteur i 1861 . De vigtigste bakterier, der producerer butyrater, er:
- Clostridium butyricum ;
- Clostridium kluyveri ;
- Clostridium pasteurianum ;
- Fusobacterium nucleatum ;
- Butyrivibrio fibrisolvens ;
- Eubacterium limosum ;
- Clostridium tyrobutyricum .
Resultaterne af reaktionen er som følger:
C 6 H 12 O 6 → C 4 H 8 O 2 + 2 CO 2 + 2 H 2Det første trin i fremstillingen af butanoater følger den metaboliske kæde af glycolyse , der resulterer i dannelsen af to molekyler af pyruvat pr molekyle glucose . Det resulterende pyruvat oxideres derefter til ethanoat ( acetat i form af ethanoyl-coenzym A ) ved en unik enzymatisk proces, der involverer en række enzymer kaldet pyruvatdehydrogenase-komplekset med parallel dannelse af kuldioxid (CO 2).) som derefter forlader cellen ved diffusion og reduktion af NAD + til NADH.
- Ethanoyl-coenzym A konverterer til acetoacetyl-coenzym A. Det ansvarlige enzym er acetyl-CoA acetyl-transferase.
- Acetoacetyl-coenzym A konverterer til β-hydroxybutyryl-CoA. det ansvarlige enzym er β-ketoacyl-CoA-reduktase (coenzym: NADH).
- Β-Hydroxybutyryl CoA konverterer til crotonyl CoA. det ansvarlige enzym er β-hydroxyacyldehydratase.
- Den crotonyl-CoA bliver butyl-CoA (CH 3 CH 2 CH 2). det ansvarlige enzym er enoyl-CoA-reduktase (coenzym: NADH).
- En phosphatgruppe erstatter CoA for at danne et butylphosphat. Det ansvarlige enzym er phosphobutyrylase.
- Phosphatgruppen forbinder ADP til dannelse af ATP og butyrater; den ansvarlige enzym er butyrat kinase .
Aceton og gæring af butyrater
Nogle bakterier producerer acetone og butanol gennem en anden proces, der starter som en gæring af butyrater, såsom:
- Clostridium acetobutylicum : (det vigtigste, der anvendes i den kemiske industri)
- Clostridium beijerinckii
- Clostridium tetanomorphum
- Clostridium aurantibutyricum
Disse bakterier følger fermenteringsprocessen beskrevet ovenfor, men når pH er under 5, skifter de til produktion af butanol og acetone for at forhindre et yderligere fald i pH, som ville være fatalt for dem. To molekyler butanol produceres til et molekyle acetone. Modifikationen finder sted efter dannelsen af acetoacetyl CoA. Denne formidler kan under disse betingelser handle på to nye måder:
Fysiologisk aktivitet af butansyre
Smørsyre kan hæmme funktionen af histondeacetylase og derved øge andelen af acetylerede histoner, som har en lavere affinitet for DNA end den ikke-acetylerede form (på grund af elektrostatisk afstødningsårsager). Det er almindeligt accepteret, at binding af transkriptionsfaktorer til DNA er ugunstigt stillet ved tilstedeværelsen af ikke-acetylerede histoner (med lav affinitet for DNA). Det er derfor muligt at konkludere, at smørsyre øger cellens transkriptionsaktivitet i niveauet af promotorer, der er reguleret af histondeacetylaser.
Smørsyre produceres af tarmmikrobiota hos pattedyr. Dets produktion forstærkes af præbiotiske midler ( opløselige fibre ). Det fungerer som brændstof for tarmslimhinden og som et lokalt og systemisk immunstimulerende middel. Det ville tillade immunsystemet at skelne mellem kolonisering af symbiotiske bakterier og patogener såsom kolera .
I kationisk eller esterform har smørsyre antivirale, antifungale og antibakterielle egenskaber. Dens interesse i denne form ligger først og fremmest i dets potentiale til at regulere kræftceller og inducere celledifferentiering.
Kilde
- ( fr ) Denne artikel er helt eller delvist taget fra Wikipedia-artiklen på engelsk med titlen " Butyric acid " ( se listen over forfattere ) .
- BUTYRIC ACID , sikkerhedsark (er) fra det internationale program for kemisk sikkerhed , hørt den 9. maj 2009
- (in) Yitzhak Marcus, The Properties of Solvents , vol. 4, England, John Wiley & Sons Ltd,1999, 239 s. ( ISBN 0-471-98369-1 )
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- (i) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 0387690026 , læst online ) , s. 294
- (da) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- " Egenskaber ved forskellige gasser " på flexwareinc.com (adgang til 12. april 2010 )
- (i) Carl L. kæberne, Handbook of Termodynamiske diagrammer , Vol. 1, Huston, Texas, Gulf Pub. Co.,1996( ISBN 0-88415-857-8 )
- (i) David R. Lide, Handbook of Chemistry and Physics , CRC,2008, 89 th ed. , 2736 s. ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- Indeksnummer i tabel 3.1 i tillæg VI til EF-regulativ nr. 1272/2008 (16. december 2008)
- " Smørsyre " i databasen over kemiske produkter Reptox fra CSST (Quebec-organisation med ansvar for sikkerhed og sundhed på arbejdspladsen), adgang til den 25. april 2009
- " Kapitel 4, akutte, reprotoksiske risici og lugtopfattelse " , på invs.sante.fr
- (i) " Fryser Lokkemad " , Nutrabaits
- AO Kasumyan og KB Døving , “ Smagspræferencer i fisk ”, Fish and Fisheries , vol. 4,2003, s. 289–347 ( DOI 10.1046 / j.1467-2979.2003.00121.x )
- (in) " Japanske hvalfangere skadet af syreafgivende aktivister " , newser.com,2010
- (in) " Voldshistorie: Smørsyreangreb " , National Abort Federation, 1998
- PR Pouillart , " Rollen med smørsyre og dens derivater til behandling af kolorektal cancer og hæmoglobinopatier ", Life Sciences , bind. 63,1 st januar 1998, s. 1739-1760 ( ISSN 0024-3205 , PMID 9820119 , læst online , adgang 29. december 2015 )
- (en-US) “ Prebiotics: Tending Our Inner Garden | NutritionFacts.org ” (Adgang til 24. februar 2019 )
- Philippe R. Pouillart , Flore Dépeint , Afif Abdelnour og Laetitia Deremaux , “ Nutriose, et præbiotisk lavt fordøjeligt kulhydrat, stimulerer tarmslimhindeimmunitet og forhindrer TNBS-induceret colitis i smågrise ”, Inflammatory Towel Diseases , vol. 16,1 st maj 2010, s. 783-794 ( ISSN 1536-4844 , PMID 19998458 , DOI 10.1002 / ibd.21130 , læst online , adgang 29. december 2015 )
Bibliografi
Voet & Voet; John Wiley & Sons, 1995