Adenosintrifosfat
| Adenosintrifosfat | |
 Struktur af adenosintriphosphat ATP 4– , dominerende art i vandig opløsning   |
|
| Identifikation | |
|---|---|
| IUPAC navn | adenosin-5 '- (tetrahydrogen triphosphat) |
| Synonymer |
Adenosin-5'-triphosphat |
| N o CAS | |
| N o ECHA | 100.000.258 |
| N o EF | 200-283-2 |
| DrugBank | DB00171 |
| PubChem | 5957 |
| ChEBI | 15422 |
| SMILE |
Nc1ncnc2n (cnc12) [C @ @ H] 1O [C @ H] (COP (O) (= O) OP (O) (= O) OP (O) (O) = O) [C @ @ H] ( O) [C @ H] 1O , |
| InChI |
Std. InChI: InChI = 1S / C10H16N5O13P3 / c11-8-5-9 (13-2-12-8) 15 (3-14-5) 10-7 (17) 6 (16) 4 (26-10) 1-25-30 (21.22) 28-31 (23.24) 27-29 (18.19) 20 / h2-4.6-7.10,16-17H, 1H2, (H, 21.22) (H, 23.24) (H2,11,12 , 13) (H2,18,19,20) / t4-, 6-, 7-, 10- / m1 / s1 Std. InChIKey: ZKHQWZAMYRWXGA-KQYNXXCUSA-N |
| Kemiske egenskaber | |
| Formel |
C 10 H 16 N 5 O 13 P 3 [isomerer] |
| Molar masse | 507,181 ± 0,014 g / mol C 23,68%, H 3,18%, N 13,81%, O 41,01%, P 18,32%, |
| Enheder af SI og STP, medmindre andet er angivet. | |
Den adenosintriphosphat eller ATP , er en nukleotid dannet af et nukleosid til et triphosphat . I biokemi af alle kendte levende væsener tilvejebringer ATP den nødvendige energi til kemiske reaktioner i stofskiftet , til bevægelse , til celledeling eller til aktiv transport af kemiske arter over biologiske membraner . For at frigøre denne energi spaltes ATP-molekylet ved hydrolyse i adenosindiphosphat (ADP) og fosfat , en reaktion, der ledsages af en ændring i standardfri entalpi ΔG 0 ′ på -30,5 kJ mol -1 . De celler derefter regenererer ATP fra ADP grundlæggende tre måder: ved oxidativ phosphorylering i forbindelse med cellulære respiration , for photophosphorylation som en del af fotosyntesen , og ved phosphorylering på substratet under visse eksergoniske kemiske reaktioner , for eksempel under glycolyse eller Krebs 'cyklus . Således indeholder den menneskelige krop til enhver tid kun ca. 250 g ATP, men forbruger og regenererer hver dag i størrelsesordenen af sin egen vægt i ATP.
- I celler hydrolyseres ATP kontinuerligt til ADP og regenereres fra ADP.
ATP-molekylet er et triphosphat gruppe bundet til atomet af carbon 5 'for en rest af ribose , en pentose , herunder carbonatomet 1' er bundet til atomet af nitrogen 9 'af en rest af adenin , en basis purin . De to P - O - P phosphoanhydridbindinger i triphosphatgruppen er bindinger med højt overførselspotentiale, det vil sige, at deres spaltning ved hydrolyse frigiver en stor mængde energi: dette er en exergonisk reaktion . Koblingen af en sådan exergonisk reaktion med en endergonisk reaktion , det vil sige en, der absorberer energi, er i stand til at gøre sidstnævnte termodynamisk mulig. På denne måde kan metaboliske reaktioner, der kræver input af energi, såsom biosyntese- reaktioner , som spontant forekommer meget langsomt eller slet ikke, finde sted meget hurtigere i celler.
ATP er forløberen for et antal kofaktorerenzym , der er vigtigt som NAD + eller CoA . Det er også en overførsel gruppe phosphat coenzym forbundet ikke-kovalent med enzymer af kinase familien . Sidstnævnte er involveret i transduktion af visse celle signalveje , ved phosphorylering af target -proteiner og enzymer, hvis aktivitet er således reguleret, eller ved phosphorylering af lipider . ATP er også substratet for adenylatcyclase , som omdanner det til cyklisk AMP . Dette er en intracellulær sekundær messenger, der især overtager fra hormoner som glukagon og adrenalin for at virke på metabolismen af glykogen , kulhydrater og lipider generelt. Forholdet mellem koncentrationen af ATP og koncentrationen af AMP bruges af celler til at bestemme deres energibelastning, det vil sige den mængde energi, de har, hvilket gør det muligt for dem, afhængigt af tilfældet, at lede deres stofskifte mod produktionen lagring af metabolisk energi. Endvidere anvendes ATP af RNA-polymeraser i transkriptionsprocessen af DNA til ribosomalt RNA og til messenger-RNA .
ATP blev opdaget i 1929 af den tyske biokemiker Karl Lohmann og parallelt af amerikanske biokemikere Cyrus Fiske og indiske Yellapragada Subbarao (in) . Det var den tyske Fritz Albert Lipmann, der foreslog, at han spillede rollen som mellemmand mellem reaktioner, der frigiver energi, og reaktioner, der absorberer den. ATP blev først syntetiseret i laboratoriet i 1948 af Alexander Robert Todd .
Ejendomme
Fysik og kemi
ATP består af adenin- , ribose- og tre phosphatgrupper , der danner en triphosphatgruppe . Disse tre fosfatgrupper betegnes fra ribose og udefter med de græske bogstaver α ( alfa ), β ( beta ) og γ ( gamma ). ATP er derfor tæt beslægtet med AMP , en af monomerer af RNA , og til dAMP , en af monomerer af DNA . ATP er meget opløseligt i vand. Det forbliver relativt stabilt i vandig opløsning til pH mellem 6,8 og 7,4, men hydrolyseres hurtigt ved mere sur eller mere basisk pH . Derfor opbevares ATP bedst som et vandfrit salt .
ATP er derimod ustabil, så snart den ikke længere er i en neutral pH- bufferopløsning . Derefter hydrolyseres det til ADP og fosfat. Dette skyldes, at hydrogenbindingerne mellem vandmolekyler på den ene side og ADP og phosphat på den anden side er stærkere end P - O - P - phosphoanhydridbindingerne, der forbinder phosphatgrupperne med hinanden i ATP - molekylet. Derfor har ATP tendens til næsten at adskille sig i ADP og fosfat efter længere eller kortere tid, når det er i opløsning i vand.
I neutral vandig opløsning ioniseres opløst ATP fire gange til dannelse af ATP 4 - anionen med en lille andel af ATP 3 - ioner .
Fordi ATP har flere negativt ladede grupper i en neutral opløsning, kan det chelatere de kationer af metal med høj affinitet. Molværdien af bindingskonstanten for nogle af disse almindelige metalkationer er som følger:
Disse interaktioner er stærke nok til, at det meste af ATP 4– er til stede i celler, der er sammensat med Mg 2+ .
Termodynamik
Når et termodynamisk system er langt fra ligevægt, har det en fri entalpi, der gør det muligt at udføre arbejde i termodynamisk forstand . Levende celler opretholder et koncentrationsforhold mellem ATP og ADP tæt på 5, hvilket er ca. ti størrelsesordener højere end koncentrationsforholdet, der er etableret ved ligevægt, hvor næsten al ATP er dissocieret i ADP og fosfat. På grund af denne afvigelse fra ligevægt frigiver hydrolyse af ATP til ADP og fosfat en stor mængde energi.
Det er hydrolysen af de to phosphoanhydridbindinger, der binder de tilstødende phosphatgrupper af ATP, der frigiver energien i dette molekyle. Af denne grund kaldes disse phosphoanhydridbindinger af bekvemmelighed men forkert ofte som energirige bindinger. Denne egenskab er imidlertid vildledende, fordi disse bindinger ikke i sig selv indeholder mere energi end de andre, og deres brud kræver et bidrag af aktiveringsenergi som for brud på enhver anden binding; det er kun deres molekylære miljø, at deres hydrolyse er exergonisk , med en standardfri entalpi- variation på -30,5 kJ mol -1 (negativ, fordi energi frigives under reaktionen):
ATP + 2 H 2 O→ ADP + Pi + H 3 O + : ΔG 0 ′ = −30,5 kJ mol −1 .Omvendt er phosphoryleringsreaktionen af ADP til ATP endergonisk med en standardfri entalpiændring på 30,5 kJ mol -1 (positiv, fordi energi absorberes under reaktionen):
ADP + Pi + H 3 O +→ ATP + 2 H 2 O : ΔG 0 ' = 30,5 kJ mol −1 .Hydrolysereaktionen af ATP til AMP og pyrophosphat HP 2 O 7 3-er mere exergonisk, med en standardfri entalpi-variation på -45,6 kJ mol -1 :
ATP + 2 H 2 O→ AMP + PPi + H 3 O + : ΔG 0 ′ = −45,6 kJ mol −1 .Biologiske funktioner
Metabolisme, organisering og mobilitet af celler
ATP forbruges i celler ved biokemiske og fysiologiske processer, der kræver energi, kendt som endergonic , og regenereres kontinuerligt ved processer, der frigiver energi, kendt som exergonic . På denne måde tillader ATP at energi overføres mellem rumligt separate processer. Det er den vigtigste energikilde for langt størstedelen af cellulære funktioner, såsom metabolisme , biosyntese , aktiv transport gennem biologiske membraner eller endda cellernes bevægelighed og bevægelse af komplekse organismer ( muskelsammentrækning ).
ATP er også involveret i vedligeholdelse af cellestruktur såvel som i dets mobilitet ved at lette samling og demontering af elementerne i cytoskeletet . Ligeledes giver det energi til muskelsammentrækning ved at katalysere forkortelsen af actin- og myosinfilamenterne , hvilket er et væsentligt behov hos dyr , der er essentielt for deres bevægelse og åndedræt - både set fra synsvinklen fra ventilationen af deres lunger end fra den fungerende af deres hjerte , ansvarlig for at cirkulere deres iltede blod gennem kroppen .
Cellesignalering
ATP deltager i mekanismerne i cellesignalering i at blive genkendt af purinerge receptorer (i) , som er måske den mest rigelige receptorer i væv af pattedyr . Hos mennesker er denne rolle af cellesignalering vigtig både i centralnervesystemet og i det perifere nervesystem . P2-purinergiske receptorer aktiveres således ved frigivelse af ATP fra synapser , axoner og gliaceller . De P2Y-receptorer (i) er for eksempel koblede receptorer G-protein , der modulerer intracellulære niveauer af calcium og, til tider, at af cyklisk AMP .
Inde i celler bruges ATP af kinaser som kilder til fosfatgrupper til at udføre fosforyleringer . Phosphorylering af proteiner og membran- lipider er almindelige former for signaltransduktion . F.eks. Observeres en aktivering af proteiner ved kaskade-phosphoryleringer med MAP-kinaser . ATP er også substratet for adenylatcyclase , der producerer cyklisk AMP , en sekundær messenger, der udløser frigivelse af calcium fra dets intracellulære lagringspunkter. Denne form for signaltransduktion er særlig vigtig i hjernens funktion , skønt den også er involveret i en lang række andre cellulære processer.
- Konvertering af ATP til cyklisk AMP med adenylatcyclase .
DNA-replikation og transkription til RNA
I alle kendte levende væsener produceres deoxyribonukleotider, der udgør DNA , af en ribonukleotidreduktase (RNR) fra de tilsvarende ribonukleotider . Disse enzymer reducere den rest af ribose i deoxyribose med en gruppe sulfhydryl -SH af en rest cystein at danner en disulfidbinding med en anden cysteinrest i reaktionen. Deres reducerede form regenereres under virkningen af thioredoxin eller glutaredoxin .
Reguleringen af ribonukleotidreduktaser og beslægtede enzymer opretholder balancen i cellen mellem deoxyribonukleotider og ribonukleotider i forhold til hinanden. For lav koncentration af deoxyribonukleotider hæmmer DNA-reparation og replikation , som i sidste ende dræber cellen, mens et unormalt forhold mellem koncentrationerne af forskellige deoxyribonukleotider er mutagent på grund af den øgede sandsynlighed for at 'inkorporere en fejlagtig nukleinbase under DNA-replikation af DNA-polymeraser . Reguleringen eller forskellene i specificitet af ribonukleotidreduktaser er måske oprindelsen til ændringen af denne balance inden i puljen af deoxyribonukleotider observeret i en situation med cellulær stress såsom hypoxi .
Under transkriptionen af DNA i ribosomalt RNA og messenger-RNA er ATP et af de fire nukleotider, der er inkorporeret i RNA af RNA-polymeraser . Den krævede energi til at brænde denne polymerisation kommer fra hydrolysen af pyrophosphatgruppen i ATP. Processen er den samme som ved DNA-biosyntese bortset fra at ATP anvendes i stedet for deoxyadenosintriphosphat (dATP).
Regenerering
Den intracellulære koncentration af ATP er typisk af størrelsesordenen 1 til 10 mmol / l . ATP kan regenereres fra ADP ved hjælp af energi frigivet ved oxidation af kulhydrater eller lipider gennem et sæt processer kaldet cellulær respiration . Ca. 30 ATP-molekyler kan produceres for hvert oxideret glucosemolekyle . Oseserne (sukkerarterne) er allerede delvist oxiderede molekyler, så en fedtsyre kan generere flere ATP-molekyler pr. Carbonatom (16 for palmitat og 6 for glukose) og udgør størstedelen af reserverne og energiforsyningen til kroppen; men sukker, der er opløseligt i vand, er lettere tilgængeligt og oxideret. Det meste af ATP produceret af ikke- fotosyntetiske eukaryoter kommer fra oxidativ fosforylering i mitokondrier . Den β-oxidation og Krebs cyklus finder også sted i mitokondrierne, som kan besætte op til en fjerdedel af rumfanget af en celle; resten af ATP produceret af disse organismer regenereres ved phosphorylering på substratniveau , for eksempel under glykolyse eller ved fermentering i cytoplasmaet . De planter og fotosyntetiske bakterier , til gengæld producerer ATP væsentlige photophosphorylation .
Glykolyse
Den glucose omdannes til pyruvat af en metabolisk vej kaldet glykolyse . De fleste levende væsener realisere denne transformation i cytoplasma af deres celler , men nogle protozoer , såsom dem fra klassen af kinetoplastid , adfærd i organel specialiseret kaldet glycosome . Der produceres to ATP-molekyler for hvert molekyle glucose, der oxideres ad denne vej, på niveauet med to enzymer, som udfører phosphorylering på niveauet af substratet : phosphoglyceratkinase og pyruvatkinase . To NADH- molekyler produceres også af NAD + , som kan oxideres af åndedrætskæden og producere yderligere ATP-molekyler. Pyruvat produceret i slutningen af glykolysen er et substrat for Krebs-cyklussen .
Krebs cykler
I mitochondrier , pyruvat er oxideres ved pyruvatdehydrogenasekomplekset til dannelse acetyl-CoA . Sidstnævnte oxideres til CO 2, NADH og FADH 2ved Krebs-cyklussen , også med produktion af GTP , som energisk svarer til ATP.
NADH og FADH 2overføre deres elektroner med højt overførselspotentiale til åndedrætskæden , der producerer yderligere ATP-molekyler ved oxidativ phosphorylering , med en hastighed på 2 til 3 ATP-molekyler pr. NADH-molekyle og 1 til 2 ATP-molekyler pr. FADH 2. Det meste af ATP i ikke- fotosyntetiske celler produceres på denne måde. Selv Krebs cyklus ikke direkte kræver tilstedeværelse af ilt O 2, kan den ikke fungere uden den, fordi det er iltet, der tjener som den sidste acceptor af elektroner i åndedrætskæden, hvilket muliggør regenerering af NAD + og FAD fra NADH og FADH 2produceret af Krebs-cyklussen: i mangel af ilt ophører sidstnævnte med at fungere i mangel af NAD + og FAD.
Oxidativ fosforylering
Strømmen af elektroner gennem respirationskæden tillader protoner at blive pumpet ud af den mitokondrielle matrix , som genererer en membran elektrokemiske potentiale på tværs af indre mitokondrielle membran grund til den resulterende proton koncentrationsgradient . Spredningen af dette elektrokemiske membranpotentiale ved ATP-syntaser giver den nødvendige energi til phosphorylering af ADP til ATP: dette kaldes kemiosmotisk kobling mellem luftvejskæden og phosphorylering af ADP. ATP-syntase er et komplekst enzym, der har en molekylær rotor, der drives af tilbagesvaling af protoner fra mitokondrie-intermembranrummet, og som overfører sidstnævntes energi til niveauet for ADP-phosphorylering.
Regenerering af ATP i mitokondrier fra NADH produceret i cytosolen involverer at føre den indre mitokondrie membran gennem NADH til den mitokondrie matrix og NAD + i den anden retning. Faktisk kan disse molekyler ikke krydse denne membran alene, så det er deres elektroner med højt overførselspotentiale, der krydser den. Den eukaryote bruger i det væsentlige to måder at gøre dette på: shuttle malat-aspartat og i mindre grad shuttle af glycerol 3-phosphat .
- Malat-aspartat-shuttle involverer først en malatdehydrogenase , som reducerer et cytosolisk oxaloacetatmolekyle til malat . Sidstnævnte kan krydse den indre mitokondrielle membran ved at låne en antiport malate- α-ketoglutarat , og efter at have nået den mitokondrielle matrix , malat er oxideres igen til oxaloacetat af en mitokondrie isoform af mitokondriel malatdehydrogenase (mMDH), omdannelse af en molekyle af NAD + ind i NADH. Mitokondrie oxalacetat omdannes til aspartat under indvirkning af en mitokondrisk aspartataminotransferase (mast) ved overførsel af en amin gruppe fra glutamat , sidstnævnte derefter give α-ketoglutarat . Aspartat låner en glutamat-aspartat-antiport for at krydse den indre mitokondriale membran og slutte sig til cytosolen, mens α-ketoglutarat gør det samme ved hjælp af en malate- α-ketoglutarat- antiport . Cytosolisk aspartat omdannes til oxaloacetat af cytosolisk aspartataminotransferase (cAST), som også producerer glutamat fra α-ketoglutarat .
- Glycerol-3-phosphat-shuttle er mindre udbredt end den forrige, men kræver ikke krydsning af den indre mitokondrie-membran, hvilket gør det hurtigere, selvom det fører til dannelsen af mindre ATP pr. Molekyle NADH-oxideret, så det fortrinsvis anvendes af celler, der kræver hurtig mobilisering af store mængder energi, det vil sige hovedsageligt musklerne og hjernen . En opløselig glycerol-3-phosphatdehydrogenase ( EC ) omdanner først dihydroxyacetonphosphat (DHAP) til glycerol-3-phosphat , som regenererer NAD + fra NADH. En indre mitokondrie membran glycerol-3-phosphat dehydrogenase ( EC ) udleder elektroner fra glycerol-3-phosphat på et FAD- molekyle for at give FADH 2og regenerering af DHAP; FADH 2reducerer igen en ubiquinon , hvis elektroner derefter forbinder luftvejskæden på niveauet af coenzym Q - cytochrom c reduktase (kompleks III ).
ATP / ADP translokase
I lighed med det, der observeres for NAD + , forbruges ATP regenereret i mitokondrier hovedsageligt i cytoplasmaet og i kernen , hvor ADP dannes, som skal phosphoryleres til ATP i cellerne. Disse materialestrømme involverer cirkulation af ADP gennem den indre mitokondriemembran fra cytosolen til den mitokondriale matrix, mens ATP regenereret i mitokondrierne krydser denne membran i omvendt retning for at blive forbrugt i cytosolen og i kernen. Da den indre mitokondrielle membran også er uigennemtrængelig for ADP og ATP, skal disse molekyler låne integrerede membranproteiner kaldet ATP / ADP-translokaser for at krydse den.
I planter , er ATP produceret ved photophosphorylation i membranen af thylakoider inde i chloroplaster . Princippet svarer til det, der implementeres i forbindelse med oxidativ fosforylering , med kemiosmotisk kobling af samme art, med den forskel, at energien kommer fra fotoner fanget af de fotosyntetiske pigmenter og ikke fra oxidationen af kulhydrater og lipider . Noget af denne ATP indtages i kloroplasten for at producere kulhydrater gennem Calvin-cyklussen .
Kroppens ATP-lagre overstiger ikke et par sekunders forbrug. I princippet genbruges ATP konstant, og enhver proces, der blokerer for regenerering, forårsager hurtigt den forurenede organisme. Dette er for eksempel tilfældet med visse kampgasser, der er designet til dette formål, eller med giftstoffer, såsom cyanid , som blokerer cytokrom c- oxidasen i åndedrætskæden i mitokondrier eller arsen , som erstatter fosfor og gengiver ubrugelige fosformolekyler.
Den kreatin kan spille som en akkumulator lagre en høj potentiel phosphatgruppe overførsel fra et ATP-molekyle, der efterfølgende kan overføres til en ADP-molekyle til regenerere ATP:
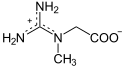
|
+ ATP ADP + |

|
| Kreatin | Phosphocreatin | |
| Kreatinkinase - EC | ||
ATP som sådan ikke kan lagres i celler, er så metabolisk energi lagres for eksempel som lipider i fedtvæv eller carbohydrater , såsom glycogen i dyr eller stivelse i dyr. Planter .
Regulering
Produktionen af ATP i en celle af eukaryot aerob reguleres tæt af allosterikum , ved feedback og ved koncentrationen af substrater til de forskellige enzymer i glykolysen og den oxidative phosphorylering . Kontrolpunkterne findes i reaktioner, der er så termodynamisk gunstige, at de faktisk er irreversible under fysiologiske forhold.
Glykolyse
Den hexokinase direkte inhiberes af produktet af reaktionen det katalyserer , nemlig glucose-6-phosphat , hvorimod pyruvatkinase inhiberes af ATP selv. Hovedpunktet for regulering af glykolyse er phosphofructokinase (PFK), som allosterisk hæmmes, når ATP er rigelig, men aktiveres, når AMP er rigelig. Hæmning af dette enzym med ATP er usædvanligt, da ATP er et substrat for den reaktion, det katalyserer. Den biologisk aktive form af dette enzym er en tetramer, der findes i to mulige konformationer, hvoraf kun den ene kan binde til fruktose-6-phosphat , som er det andet substrat for dette enzym. Det protein har to ATP-bindingssteder: det aktive sted er tilgængeligt i enten konformation, men ATP-binding til den inhiberende stedet stabiliserer konformationen som kun binder svagt til fructose-6-phosphat. Et bestemt antal andre små molekyler er i stand til at kompensere for den inhiberende virkning af ATP og således genaktivere phosphofructokinase; dette er for eksempel tilfældet med cyklisk AMP , ionerne ammonium , ioner phosphat , fruktosen 1,6-bisphosphat og fruktose 2,6-bisphosphat .
Krebs cykler
Den Krebs cyklus i det væsentlige reguleres af tilgængeligheden af dets vigtigste substrater , især forholdet mellem koncentrationen af NAD + og NADH , samt koncentrationerne af calcium , phosphat , ATP, ADP og AMP . Den citrat er en inhibitor af citratsyntase virkende gennem tilbagemelding og en inhibitor af phosphofructokinase , som binder reguleringen af Krebs cyklus til den af glycolyse .
Oxidativ fosforylering
Reguleringen af oxidativ phosphorylering er i det væsentlige baseret på cytochrom c oxidase , som er reguleret af tilgængeligheden af dets substrat, nemlig reduceret cytochrom c . Mængden af reduceret cytochrom c tilgængelig afhænger direkte af mængden af andre substrater:
1 ⁄ 2 NADH + oxideret cyt c + ADP + Pi 1 ⁄ 2 NAD + + reduceret cyt c + ATP,dermed ligningen nedenfor, udledt af denne ligevægt:
Således indebærer et højt [NADH] ⁄ [NAD + ] koncentrationsforhold eller et højt [ADP] [Pi] ⁄ [ATP] koncentrationsforhold (højre side af denne ligestilling) et [ reduceret cyt c ] ⁄ koncentrationsforhold [ oxideret cyt c ] (venstre lem), dvs. en høj koncentration af reduceret cytochrom c , og en stærk aktivitet af cytochrom c oxidase.
Et yderligere reguleringsniveau introduceres af hastigheden af ATP- og NADH-transport mellem mitokondrie-matrixen og cytosolen .
Proteinbindinger
Nogle proteiner, der binder til ATP, har en karakteristisk foldning kaldet Rossmann-folden , et generelt strukturmotiv af proteiner, der binder til nukleotider , såsom dem, der binder til NAD . De mest almindelige ATP-bindende proteiner, kaldet kinaser , deler nogle få fælles strukturelle træk. De proteinkinaser , som er den største gruppe af kinaser og andel specialiseret strukturelle træk i ATP-bindende og fosfat overførsler grupper.
ATP kræver generelt tilstedeværelsen af en divalent kation for at danne et kompleks med proteiner . Det er næsten altid en kation af magnesium Mg 2+ , der binder til phosphatgrupperne i ATP. Denne kation reducerer signifikant dissociationskonstanten for ATP - proteinkomplekset uden at påvirke enzymets evne til at katalysere dets kemiske reaktion, når ATP er bundet. Tilstedeværelsen af magnesiumkationer kan udgøre en mekanisme til regulering af kinaser.
ATP-analoger
In vitro- eksperimenter bruges ofte til at studere biokemiske processer, der involverer ATP, og hæmmere af enzymer, der bruger ATP, såsom kinaser , er nyttige instrumenter til at undersøge bindings- og overgangstilstande involveret i reaktioner, der involverer ATP. Anvendes ligesom ATP i røntgenkrystallografi til bestemmelse af proteinstrukturen danner et kompleks med ATP, ofte i kombination med andre substrater. De mest nyttige ATP-analoger er dem, der ikke hydrolyserer som ATP ville, og blokerer enzymet i en tilstand tæt på ATP - enzymkomplekset. Den adenosin 5 '- [γ-thio] triphosphat (ATPyS), for eksempel, er en analog af ATP meget almindeligt anvendt i laboratoriet: et af atomerne af oxygen af phosphat γ er erstattet med et atom af svovl , og ATPyS hydrolyserer med en betydeligt langsommere hastighed end ATP's, så den fungerer som en hæmmer af processer, der er afhængige af hydrolysen af et ATP-molekyle. Der er imidlertid enzymer, der er i stand til at hydrolysere dem med forholdsvis høje hastigheder, når de er i tilstrækkelig koncentration, hvilket indebærer at man med forsigtighed skal fortolke de opnåede resultater med sådanne inhibitorer.
I krystallografi, er hydrolyseprodukter overgangstilstande undersøgt under anvendelse komplekser af vanadat ioner .
Noter og referencer
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- (i) fri energi forandring , på stedet af Marc Kirschner (i) , Harvard Medical School .
- (in) ' ' Naturens batterier 'har måske hjulpet strøm til tidlige livsformer " på Science Daily , 25. maj 2010(adgang 23. august 2016 )
- (i) David E. Bryant, Katie ER Marriott Stuart A. Macgregor, Colin Kilner, Matthew A. Pasek og Terence P. Kee , " På præbiotisk potentiale Reduceret fosfor oxidationstilstand: H-phosphinat pyruvat-systemet " , Chemical Communications , bind. 46, nr . 21, 7. juni 2010, s. 3726-3728 ( PMID 20386792 , DOI 10.1039 / C002689A , Bibcode 2010LPICo1538.5264B , læs online )
- (i) Susanna Törnroth-Horsefield og Richard Neutze , " Åbning og lukning af porten metabolit " , Proceedings of the National Academy of Sciences i USA , vol. 105, nr . 50, 16. december 2008, s. 19565-19566 ( PMID 19073922 , PMCID 2604989 , DOI 10.1073 / pnas.0810654106 , læs online )
- (i) Eunus S. Ali, Hua Jin, Claire H. Wilson, George A. Tallis, Fiona H. Zhou, Y. Grigory Rychkov og Greg J. Barritt , " Den glukagonlignende peptid-1 analoge exendin-4 reverserer nedsat intracellulær Ca2 + signalering i steatotiske hepatocytter ” , Biochimica et Biophysica Acta (BBA) - Molecular Cell Research , vol. 1863 nr . 9, september 2016, s. 2135-2146 ( PMID 27178543 , DOI 10.1016 / j.bbamcr.2016.05.006 , læs online )
- (i) D. Grahame Hardie og Simon A. Hawley , " AMP-aktiveret proteinkinase: energibehovshypotesen revideret " , BioEssays , bind. 23, nr . 12, december 2001, s. 1112-1119 ( PMID 11746230 , DOI 10.1002 / bies.10009 , læs online )
- (i) Karl Lohmann , " Über die im Pyrophosphatfraktion Muskel " , Naturwissenschaften , vol. 17, nr . 31, August 1929, s. 624-625 ( DOI 10.1007 / BF01506215 , læs online )
- (i) Koscak Maruyama , " Opdagelsen af adenosin trifosfat og skabelsen af dens struktur " , Journal of History of Biology , vol. 24, n o 1, Marts 1991, s. 145-154 ( DOI 10.1007 / BF00130477 , JSTOR 4331161 , læs online )
- (in) AC Storer og A. Cornish-Bowden , " Koncentration af MgATP 2 og andre ioner i opløsning. Beregning af de sande koncentrationer af arter til stede i blandinger af associerende ioner ” , Biochemical Journal , bind. 159, nr . 1, Oktober 1976, s. 1-5 ( PMID 11772 , PMCID 1164030 , DOI 10.1042 / bj1590001 , læs online )
- (i) John E. Wilson og Arnold Chin , " Chelation of divalent kations by ATP Studied by titration calorimetry " , Analytical Biochemistry , vol. 193, nr . 1, 15. februar 1991, s. 16-19 ( PMID 1645933 , DOI 10.1016 / 0003-2697 (91) 90036-S , læs online )
- (in) ' Magnesium in cardiac energy metabolism " , Journal of Molecular and Cellular Cardiology , Vol. 18, nr . 10, Oktober 1986, s. 1003-1013 ( PMID 3537318 , DOI 10.1016 / S0022-2828 (86) 80289-9 , læs online )
- (i) Britton Chance, Howard Lees og John R. Postgate , " Betydningen af" omvendt Electron Flow "og" High Energy Electron "i biokemi " , Breve til Nature , vol. 238, nr . 5363, 11. august 1972, s. 330-331 ( PMID 4561837 , DOI 10.1038 / 238330a0 , læs online )
- Celleens molekylære biologi Af Harvey Lodish, Arnold Berk, Paul Matsudaira, James Darnell , Chris A. Kaiser, Pierre L. Masson - side 301
- (i) Neeti Sanan Mishra og Renu Tuteja Narendra Tuteja , " Signalering gennem MAP kinase netværk i planter " , Archives of Biochemistry and Biophysics , bd. 452, nr . 1, august 2006, s. 55-68 ( PMID 16806044 , DOI 10.1016 / j.abb.2006.05.001 , læs online )
- (i) Margarita Kamenetsky Sabine Middelhaufe, Erin M. Bank, Lonny R. Levin, Jochen Buck og Clemens Steegborn , " Molecular Detaljer af cAMP Generation i pattedyrceller: A Tale of Two Systems " , Journal of Molecular Biology , vol. 362, nr . 4, 29. september 2006, s. 623-639 ( PMID 16934836 , PMCID 3662476 , DOI 10.1016 / j.jmb.2006.07.045 , læs online )
- (i) Jacques og Nicole Udskyd Hanoune , " forordning og rolle adenylylcyclaseaktivitet isoformer " , Annual Review for Farmakologi og Toksikologi , bd. 41, April 2001, s. 145-174 ( PMID 11264454 , DOI 10.1146 / annurev.pharmtox.41.1.145 , læs online )
- (in) JoAnne Stubbe , " Ribonucleotide reductase: amazing and confusing " , Journal of Biological Chemistry , vol. 265, nr . 10, 5. april 1990, s. 5329-5332 ( PMID 2180924 , læs online )
- (i) Catherine M. Joyce og Thomas A. Steitz , " polymerase struktur og funktion: variationer over et tema? ” , Journal of bacteriology , bind. 177, nr . 22, November 1995, s. 6321-6329 ( PMID 7592405 , PMCID 177480 , læs online )
- (in) I. Beis og EA Newsholme , " Indholdet af adeninnukleotider, glykolytiske mellemprodukter og nogle fosfagener i hvilemuskler fra hvirveldyr og hvirvelløse dyr " , Biochemical Journal , bind. 152, nr . 1, Oktober 1975, s. 23-32 ( PMID 1212224 , PMCID 1172435 , DOI 10.1042 / bj1520023 , læs online )
- (en) PR Rich , “ The molecular maskiner of Keilins respiratory chain ” , Biochemical Society Transactions , vol. 31, nr . 6, december 2003, s. 1095-1105 ( PMID 14641005 , DOI 10.1042 / bst0311095 , læs online )
- http://biochimej.univ-angers.fr/Page2/COURS/Zsuite/3BiochMetab/8BetaOxydation/1BetaOxydation.htm
- (in) Marilyn Parsons , " glycosomes: parasites and the divergence of peroxisomal purpose " , Molecular Microbiology , Vol. 53, n o 3, August 2004, s. 717-724 ( PMID 15255886 , DOI 10.1111 / j.1365-2958.2004.04203.x , læs online )
- (i) Jan Pieter Abrahams Andrew GW Leslie Rene Lutter og John E. Walker , " struktur ved 2,8 Å opløsning af F1-ATPase fra bovine hjerte mitokondrier " , Nature , vol. 370, nr . 6491, 25. august 1994, s. 621-628 ( PMID 8065448 , DOI 10.1038 / 370621a0 , læs online )
- (i) John F. Allen , " Fotosyntese af ATP Electron, Proton Pumper, rotorer, og Poise " , Cell , vol. 110, nr . 3, 9. august 2002, s. 273-276 ( PMID 12176312 , DOI 10.1016 / S0092-8674 (02) 00870-X , læs online )
- (i) C. Dahout-Gonzalez, H. Nury, V. Trezeguet, GJ-M. Lauquin, E. Pebay-Peyroula og G. Brandolin , " Molecular, Functional, and Pathological Aspects of the Mitochondrial ADP / ATP Carrier " , Physiology , bind. 21, nr . 4, 25. juli 2005, s. 242-249 ( PMID 16868313 , DOI 10.1152 / physiol.00005.2006 , læs online )
- (in) ST Rao og Michael G. Rossmann , " Sammenligning af super-sekundære strukturer i proteiner " , Journal of Molecular Biology , bind. 76, nr . 2 15. maj 1973, s. 241, IN1, 251-250-256 ( PMID 4737475 , DOI 10.1016 / 0022-2836 (73) 90388-4 , læs online )
- (i) Eric D. Scheeff og Philip E. Bourne , " Structural Udviklingen i Protein kinase-Ligesom Superfamily « , PLoS Computational Biology , bd. 1, nr . 5, Oktober 2005, e49 ( PMID 16244704 , PMCID 1261164 , DOI 10.1371 / journal.pcbi.0010049 , læs online )
- (i) Phillip Saylor Chengqian Wang, John T. Hirai og Joseph A. Adams , " A Second magnesiumion Kritisk for ATP Binding i kinasedomænet af v-fps oncoprotein " , Biochemistry , vol. 37, nr . 36, 8. september 1998, s. 12624-12630 ( PMID 9730835 , DOI 10.1021 / bi9812672 , læs online )
- (i) Xiaofeng Lin, Marina K og Ayrapetov Gongqin Sun , " Karakterisering af interaktionen mellem de aktive sider af en proteintyrosinkinase og en divalent metalaktivator " , BMC Biochemistry , bind. 6, 23. november 2005, s. 25 ( PMID 16305747 , PMCID 1316873 , DOI 10.1186 / 1471-2091-6-25 , læs online )
- (in) Clive R. Bagshaw , " et overblik ATP-analoger " , Journal of Cell Science , vol. 114, n o Pt 3, Februar 2001, s. 459-460 ( PMID 11171313 , læs online )
- (in) SM Honigberg, DK Gonda, J. Flory og CM Radding , " Parring af nukleoproteinfilamenter med stabil aktivitet fremstillet af RecA-protein, enkeltstrenget DNA og adenosin 5 '- (gamma-thio) triphosphat " , af Journal Biological Chemistry , bind. 260, nr . 21, 25. september 1985, s. 11845-11851 ( PMID 3840165 , læs online )
- (da) JA Dantzig, JW Walker, DR Trentham et YE Goldman , " Afslapning af muskelfibre med adenosin 5 '- [gamma-thio] triphosphat (ATP [gamma S]) og ved laserfotolyse af buret ATP [gamma S] : bevis for Ca 2+ -afhængig affinitet hurtigt afmontering nul-force cross-broer ” , Proceedings of National Academy of Sciences i USA , vol. 85, nr . 18, September 1988, s. 6716-6720 ( PMID 3413119 , PMCID 282048 , DOI 10.1073 / pnas.85.18.6716 , JSTOR 32451 , Bibcode 1988PNAS ... 85.6716D , læs online )
- (in) T. Kraft, SC Yu HJ Kuhn og B. Brenner , " Effekt af Ca 2+ er svag inter-interaktion med actin i nærvær af adenosin 5 '- [gamma-thio] triphosphat) " , Proceedings of National Academy of Sciences i Amerikas Forenede Stater , vol. 89, nr . 23, December 1992, s. 11.362-11.366 ( PMID 1.454.820 , PMCID 50.550 , DOI 10,1073 / pnas.89.23.11362 , JSTOR 2.360.707 , bibcode 1992PNAS ... 8911362K , læse online )
- (i) Andrea M. og Joseph M. Resetar Chalovich , " Adenosin 5 '- (gamma.-thiotriphosphat.): En ATP-analog, der skal bruges med forsigtighed i muskelkontraktionsundersøgelser " , Biochemistry , vol. 34, nr . 49, 12. december 1995, s. 16039-16045 ( PMID 8519760 , DOI 10.1021 / bi00049a018 , læs online )

![{\ displaystyle {\ frac {[\ mathrm {cyt ~ c_ {reduceret}}]} {[\ mathrm {cyt ~ c_ {oxid}}]}} = \ venstre ({\ frac {[\ mathrm {NADH}] } {[\ mathrm {NAD}] ^ {+}}} \ højre) ^ {\ frac {1} {2}} \ venstre ({\ frac {[\ mathrm {ADP}] [\ mathrm {P_ {i }}]} {[\ mathrm {ATP}]}} højre) K _ {\ mathrm {eq}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/89e75ceb7b27981ba88688fe6369101117a55af0)