Dihydrogen
| Dihydrogen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikation | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC navn | brint | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
brint |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.014.187 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EF | 215-605-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E949 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMIL |
[HH] , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / H2 / h1H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Udseende | lugtfri, farveløs, komprimeret gas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formel |
H 2 [isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar masse | 2,01588 ± 0,00014 g / mol H 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusion | −259,1 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kogning | −252,76 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighed |
21,4 ml i 1 l vand (dvs. 1,92 mg / l ) ( 0 ° C ) 8,5 ml i 1 l vand ( dvs. 0,76 mg / l ) ( 80 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opløselighedsparameter δ | 6,9 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumenmasse |
0,089 88 g / l (gas, CNTP ), 0,070 8 kg / l (flydende, -253 ° C ), ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Automatisk tænding temperatur | 500 til 571 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | brandfarlig gas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosionsgrænser i luft | 4 - 76 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mættende damptryk |
ligning:
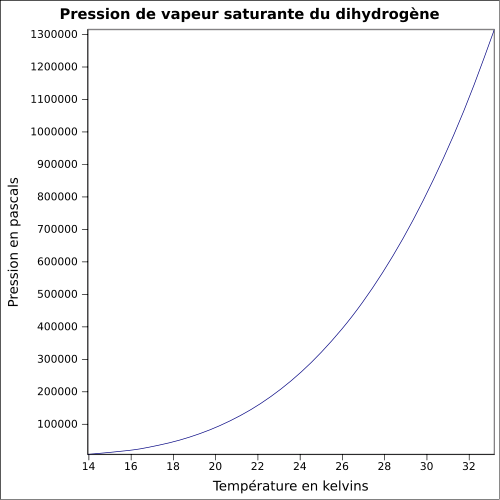
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | 13,0 bar, -239,95 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Triple point |
-259,3467 ° C ; 7,205 kPa abs |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varmeledningsevne | 42,5 × 10 −5 cal cm −1 s −1 K −1 til 16,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lydens hastighed | 1310 m s −1 ( 27 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gas, 1 bar | 130,68 J K −1 mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 0,058 68 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 0,90 kJ mol −1 ( 1 atm , −252,76 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s | 14266 J kg −1 K −1 til 293 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| STK | 285,8 kJ / mol ( 25 ° C , gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | 242,7 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Fare H220 H220 : Yderst brandfarlig gas |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, B1, A : Kritisk komprimeret gas kritisk temperatur = −239,9 ° C B1 : Brandfarlig gas nedre antændelsesgrænse = 4,0% Oplysning ved 1,0% ifølge klassificeringskriterier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| gas:
4
0
0
kølet væske: 4 3 0 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : brandfarlig gas UN -nummer : 1049 : KOMPRIMERET HYDROGEN Klasse: 2.1 Klassificeringskode: 1F : Komprimeret gas, brandfarlig; Mærkat: 2.1 : Brandfarlige gasser (svarer til de grupper, der er betegnet med store bogstaver F); 
223 : nedkølet flydende gas, brandfarlig FN-nummer : 1966 : VÆSKEN KØLESKYDD VÆSKE Klasse: 2.1 Klassificeringskode: 3F : Kølet flydende gas, brandfarlig; Mærkat: 2.1 : Brandfarlige gasser (svarer til de grupper, der er betegnet med store bogstaver F);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Indånding | kvælning | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheder af SI og STP, medmindre andet er angivet. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den dihydrogen er den form molekylære af grundstoffet hydrogen , der eksisterer som gas til standardbetingelser . Molekyler har to hydrogenatomer; dens kemiske formel er H 2 . Det kaldes også "molekylært brint" eller, i gasform, "hydrogengas". I dagligdagens sprog, når der ikke er nogen tvetydighed med det kemiske element med samme navn, kaldes det meget ofte simpelthen som "brint", og vi taler undertiden blot om "brintmolekyle" til brintmolekylet.
Det blev brugt i Zeppelin- typen luftskibe , ved hjælp af egenskaberne af Archimedes' fremstød , inden de blev erstattet af helium , som er mindre farligt, fordi det ikke er brændbart. I dag er det globale forbrug af brint omkring 50 millioner ton om året. Det meste af produktionen af brint forbruges på stedet, hovedsageligt i den kemiske og petrokemiske industri: syntese af ammoniak (50%), raffinering og afsvovling af kulbrinter (37%), syntese af methanol (12%). Det er lavet 96% af kulbrinter (methan, råolie, kul) og 4% ved elektrolyse af vand . Denne produktion ledsages i 2020 af produktionen af 830 millioner tons CO 2om året eller ca. 2% af de globale emissioner .
Det er en let gas, som Jordens tyngdekraft ikke kan holde tilbage. Det brænder i luften og producerer vand , deraf dets navn sammensat af præfikset "hydro", fra det græske ὕδωρ (hudôr), der betyder "vand", og med endelsen "gen", fra det græske γεννᾰν (gennen), "Beget" . Det er især blevet brugt til konservering af kød . Dihydrogen har en fordampningstemperatur på 20,27 K og en smeltetemperatur på 14,02 K . Under meget høje tryk , som dem, der findes i centrum af gaskæmperne , adskiller disse molekyler sig, og brint bliver et flydende metal . I rummet er skyer af H 2 grundlaget for stjernedannelsesprocessen .
Historisk
Den første kendte videnskabsmand, der har beskrevet produktionen af dihydrogen, var den schweiziske Paracelsus (1493-1541). Han gjorde denne opdagelse ved at hælde vitriol løbet jern pulver , men forstod ikke den nøjagtige karakter af den gas, der afgives under forsøget .
Den engelske kemiker Henry Cavendish (1731-1810), der gentager forsøgene med Paracelsus med flere forskellige metaller , opdager, at den således producerede gas er forskellig fra luft, er brandfarlig og har en lav densitet. Han kaldte denne gas "brandfarlig luft" (på engelsk: brandfarlig luft ) og konstaterer, at dens forbrændingsprodukt af vandet . Den dioxygen bliver ham navnet "vital luft".
Den franske kemiker Antoine Lavoisier, der har bekræftet forsøgene med Cavendish, foreslår ordet "brint" for at erstatte udtrykket "brændbar luft". Dette ord er udformet med præfikset hydro (fra græsk ὕδωρ (hudôr), ”vand”) og suffikset genet (fra græsk γεννᾰν (gennen), ”for at generere”). Ordet brint betyder derfor, at der genereres vand .
Efterfølgende på det videnskabelige område, ordet "hydrogen" blive anvendt til at navngive grundstof H og ordet "hydrogen" vil blive anvendt til molekylet H 2 .
Kemiske egenskaber
Anerkendelsestest
For at teste for tilstedeværelsen af dihydrogen kontaktes en flammende log til et reagensglas indeholdende dihydrogen. Den kemiske reaktion ved forbrænding af hydrogen med ilt i luften, initieret af varmekilden, frembringer en karakteristisk støj kaldet "gøen" eller "gøen".
Forbrænding
Den forbrænding af hydrogen i dioxygen , som producerer vand , er 2 H 2 (g) + O 2(g) → 2 H20(det). Den er særlig voldelig (se genkendelsestest) og meget eksoterm : dens brændværdi er 141,86 MJ / kg [eller 141,79 MJ / kg ] (ved 25 ° C [eller 15 ° C ] under 1 atm ) eller en standard forbrændingsentalpi ved 25 ° C , på -285,84 kJ / mol , ved 100 ° C , på -283,45 kJ / mo l (H 2 gas, O 2 gas, men H 2 O væske , som højere brændværdi eller PCS), men af 120,1 MJ / kg [eller 119,93 MJ / kg ], dvs. en forbrændingsentalpi ved 100 ° C på −242,8 kJ / mol (H 2 gas, gasformig O 2 , H 2 O damp , som lavere brændværdi eller NCV , tæller 40,660 kJ / mol til fordampning af vand ved 100 ° C ) mod f.eks. kun 49,51 MJ / kg for butan . Denne ejendom gør det til et valgfrit brændstof til rumfartøjer, men gør dets opbevaring farlig.
Den samme oxidation langsommere bruges til at producere elektricitet i brændselscellen .
Ortho og para former
Hydrogengas er en blanding af to typer af isomere molekyler, som adskiller sig fra hinanden i spin- af deres atomkerner . Disse to former kaldes ortho- og para-hydrogen , og ortho-formen svarer til en ophidset tilstand, der ikke eksisterer i sin rene tilstand. Under normale temperatur- og trykbetingelser , ved termisk excitation, består hydrogen af 75% af ortho-formen og 25% af para-formen. Ved 77 K er blandingen ved ligevægt (nået spontant i flere dage, men på få timer med katalysatorer) ved 50%. Men ved meget lav temperatur omdannes ortho-formen fuldstændigt til paratilstanden (antiparallel spins, singlet-tilstand) over tid. De to former har lidt forskellige energiniveauer og derfor lidt forskellige fysisk -kemiske egenskaber . For eksempel er para-hydrogens smeltepunkt og kogepunkt ca. 0,1 K lavere end ortho- .
Brintkilder
Dihydrogen er en meget let gas. Da Jordens tyngdekraft ikke kan holde den tilbage, flygter den naturligt fra Jordens atmosfære. Derfor er det kun til stede i spormængder (0,5 ppmv ) i luft . Denne atmosfæriske knaphed betyder, at alt det anvendte dihydrogen fremstilles industrielt ved forskellige processer, fra molekyler, hvor hydrogenatomer er kemisk bundet.
Der er dog et par geologiske sammenhænge, hvor dihydrogen naturligt kommer fra jorden . Hydrogenet, der stammer fra disse zoner, er betegnet med udtrykket naturligt brint .
Kunstigt brint
Den produktion af hydrogen omfatter mange forskellige processer , den hydrogen -atom danner en række molekyler ( vand , carbonhydrider , sukkerarter , etc. ).
Historisk produktionsmetodeHistorisk set i XIX th århundrede blev dihydrogen opnået ved emission af vanddamp (H 2 O) i en tønde fyldt med jernspåner og chips. Vanddampen oxiderede metallet og skabte jernoxid på den ene side og frigav brint på den anden. Sidstnævnte forlod derefter tønden, hvor den blev filtreret i en anden tønde fyldt med vand, derefter opbevaret direkte i en aerostat . Denne enhed tillod hæren at blæse en observationsballon overalt og i løbet af få timer .
Nuværende metoderI 2015 blev brint produceret industrielt ved forskellige processer:
- for 49% ved dampreformering fra kulbrinter (især fra metan , se Reformering af metan );
- for 29% ved delvis oxidation af råolie
- for 18% ved forgasning af kul
- for 4% ved elektrolyse af vand .
Andre processer undersøges også, fra revner eller delvis oxidation, som har fordelen ved at være eksoterm .
Reform af kulbrintedampDen dampreforming af kulbrinter er den metode, som ved begyndelsen af det XXI th århundrede, er den mest anvendte på industrielt niveau. Dets princip er baseret på reaktionen af kulbrinter (metan osv.) I nærværelse af vanddamp og varme. Den globale reaktion er skrevet:
.Det energieffektivitet er omkring 40 til 45% i nogle installationer . I industriel praksis er det nødvendigt at fremskynde reaktionen ved hjælp af katalysatorer eller brændere. Det har ulempen ved at producere kuldioxid , en drivhusgas .
Katalytiske teknologier, eller mere innovative teknologier, såsom plasma reformatorer, er i øjeblikket under undersøgelse.
VandelektrolyseDen elektrolyse af vand er en teknologi, der består i at lede en elektrisk strøm (direkte) i vand (til hvilket et elektrolyt såsom kaustisk soda tidligere er blevet tilsat ) for at opnå den dissociation af vandmolekylerne i brint og ilt .
Reaktion ved anoden :
2 H 2 O(l) → O 2(g) + 4 H + (aq) + 4 e -Reaktion ved katoden :
4 H 2 O(l) + 4 e - → 2H 2 (g) + 4 OH - (aq)Reaktion i vand:
4 H + (aq) + 4 OH - (aq) → 4 H 2 O (det)Samlet reaktion:
2 H 2 O(l) → 2H 2 (g) + O 2 (g)hvor (l), (g) og (aq) betyder henholdsvis "i flydende fase", "i gasfase" og "i vandig opløsning".
Denne teknologi kræver store mængder elektricitet. Ifølge Ademe i 2020 er effektiviteten af brintkæden i Power-to-H2-to-Power 25%, mens den for elektriske batterier er 70%. Det er derfor relativt lidt brugt.
Delvis oxidation af kulbrinterDenne reaktion er et ”rigt” forbrænding i den forstand, at målet er at producere en gas rig på H 2 og CO (syntesegas); i stedet for de ”klassiske” CO 2 og H 2 O produkter.
Reaktionen er skrevet:
.Det meste af tiden bruges luft som en oxidator. Vi har derefter:
.Reaktionen er eksoterm: for eksempel er entalpi af reaktionen med metan -35,7 kJ mol -1 .
Ligesom dampreformeringsreaktionen er det nødvendigt at katalysere reaktionen.
Interessen for den delvise oxidationsreaktion ligger i dens eksoterme natur (i modsætning til dampreformeringsreaktionen), som hjælper med katalyse (temperaturstigning).
Den store ulempe ligger i det faktum, at de procentdele af H 2 er lavere end dem, der opnås ved dampreformering, fordi størstedelen tilstedeværelsen af nitrogen i luften. Derudover er der en risiko for at opnå NO x .
Virkning af en syre på et metalDihydrogen produceres ved indvirkning af en syre på et metal. Eksempel:
.Dihydrogen kan også produceres ved omsætning af natriumhydroxid med aluminium ifølge formlen:
Produktion ved fotosyntese (cyanobakterier)Nogle cyanobakterier kan kemisk nedbryde vand til ilt og brint ved hjælp af fotosyntetiske reaktioner. Dette ville gøre det muligt at producere brint ved hjælp af solenergi . Forskning er i gang på dette område, især med hensyn til genteknologi .
Naturligt brint
Hydrogen produceret på jorden naturligt i modsætning til hydrogen produceret kunstigt ved reformering af metan eller carbonhydrider siges at være naturligt hydrogen eller nativt hydrogen .
Fordeling, produktionskapacitet og fysisk-kemiske mekanismer i sine kilder eller indskud Den er stadig genstand for forundersøgelser i begyndelsen af XXI th århundrede. I april 2019 blev sen4H2-forskningsprojektet således lanceret og samfinansieret af Den Europæiske Rumorganisation , der har til formål at opdage naturlig brintemission ved hjælp af satellitbilleder.
Kilder til naturligt brintProduktionen af naturligt brint i rygraden har været kendt siden 1970'erne og studeret for nylig. Disse er serpentinization reaktioner ( redox af olivin ) mellem vand og vulkanske klipper flugter med jordens kappe , lettes af varmen fra disse eksotermiske reaktioner : ilt af H 2 O molekyler.fanget af jern i klippen, hydrogenatomerne frit kan associere i H 2. Det således producerede brint undslipper gennem hydrotermiske udluftninger og kan eventuelt reagere igen til dannelse af metan og derefter tungere kulbrinter. For dybt kan disse indskud ikke udnyttes i 2018
Brintemissioner er også blevet opdaget midt på kontinentale kratoner af den russiske geolog Nicolay Larin efter hans arbejde med den hydratiserede jordhypotese. De IFP Energies Nouvelles har bekræftet denne opdagelse i 2013, rapporterer lokalt vigtige spørgsmål, på de fleste kontinenter, Rusland , de Forenede Stater , i Brasilien , i Oman eller Mali .
Fænomenet er stadig dårligt forstået, og debatten om den nøjagtige mekanisme, der genererer disse emissioner, er endnu ikke afgjort. Det kunne dreje sig om hydrering af jern med infiltreret vand, hvor denne er til stede i bælterne af greenstone , der er til stede i kratoner. I Kansas , nær Junction City , blev der således identificeret et depositum i 1980'erne og blev genstand for fornyet interesse i 2000'erne; dihydrogenet ville blive opnået der fra sådanne reaktioner ved oxidation af jern. I Rusland anslog IFP i 2010 den daglige strøm af en enkelt depression til flere titusinder kubikmeter eller det tilsvarende forbrug på 500 taxaer. En original geologisk eller hydrogeologisk fremgangsmåde er også gældende for frigivelser af brint undersøgt i Brasilien, i nogle feekredse placeret i bassinet i São Francisco .
I Yanartaş , Tyrkiet, ville "tusindårsbrande" på Mount Chimera være forbrænding af en gas bestående af metan (87%), brint (7,5 til 11%) og dinitrogen (2 til 4,9%), der har en dobbelt oprindelse: serpentinisering på den ene side, en termogen gas på den anden side. De ville være den oprindelige kilde til den olympiske flamme .
Den Mali er, i 2015, det eneste land, hvor den naturlige brint udnyttes, i landsbyen Bourakébougou , 60 kilometer nord for Bamako . Gassen ville komme fra en "overmodning af olie", der sandsynligvis blev begravet i nærheden, og dens reserver anslås til ca. 1,5 milliarder kubikmeter . Trykket i brøndene aftager ikke, så udfyldningen fyldes konstant, hvilket muliggør bæredygtigheden af denne operation.
De vulkanske gasser indeholder ofte spor af brint. Således på Hawaii viste et spektroskopisk studie udført på en vulkansk gasbrand, at det var en forbrænding af dihydrogen.
Enhver vulkansk sten ville indeholde brint, op til ca. 5 l / m 3 ; derfor viser alle borehullerne brintafgasning. Under det russiske eksperiment med sg3-boring blev mudderet, der blev ekstraheret fra hullet, beskrevet som boblende med denne gas .
UdfordringerI modsætning til kunstigt brint, som kræver, at der produceres energi, hvilket reducerer det til bare at være en energibærer , er naturligt brint en reel energikilde , som forbrænding ikke kun producerer vand. Derudover kunne samproduktioner være mulige med geotermisk energi eller heliumudvinding , hvilket kunne hjælpe sektoren med at være konkurrencedygtig. I 2020 kvantificeres det industrielle potentiale imidlertid ikke nøjagtigt, og mineloven tager ikke brint i betragtning i mange lande. Påvisning af hydrogen in situ er faktisk vanskelig, selvom der er blevet udviklet mere effektive detektorer.
Industrielle anvendelser
Det globale brintforbrug er i dag omkring 50 millioner tons om året. Det meste af brintproduktionen forbruges på stedet, hovedsageligt i den kemiske og petrokemiske industri: syntese af ammoniak (50%), raffinering og afsvovling af carbonhydrider (37%), syntese af methanol (12%).
De vigtigste industrielle anvendelser af brint er:
- den metode Haber-Bosch (produktion af ammoniak ), den hydrogenering af fedtstoffer og olier og fremstilling af methanol ;
- fremstilling af saltsyre , svejsning , brændstof til raket og reduktion af malm af metal;
- det flydende dihydrogen bruges til forskning ved meget lave temperaturer, herunder undersøgelse af superledningsevne ;
- brint bruges som en sporgas til at udføre lækagedetekteringsoperationer på forskellige områder (olieraffinering, biler, varmeinstallationer, vanddistributionsnet, flytanke osv.);
- brint er et fødevaretilsætningsstof, der er godkendt under kode E949 , i kategorien sporstoffer
- brint bruges også som varmeoverføringsfluid i visse maskiner med høj effekt (f.eks. synkron kraftværksgenerator);
- brint blev brugt i aerostater, fordi det er fjorten gange mindre tæt end luft, men det er af sikkerhedsmæssige årsager blevet erstattet af helium; den bruges stadig til nogle vejrballoner på fjerntliggende stationer.
- Dihydrogen blev testet som brændstof til luftfart under en flyvning den 15. april 1988 med Tupolev Tu-155.
Visse isotoper af brint har også en særlig industriel eller teknologisk anvendelse:
- den deuterium ( 2 H) anvendes i nukleare programmer som en moderator ( tungt vand eller D 2 O) til at bremse de neutroner . Deuteriumforbindelser bruges også i kemi og biologi til at studere eller bruge den isotopiske effekt ;
- den tritium ( 3 H) en anden isotop, fremstilles i kernereaktorer og anvendes til konstruktion af atombomber . Det bruges også som en isotop markør i biovidenskab og som en kilde til stråling i selvlysende maling;
- deuterium og tritium smelter også sammen i forskningsreaktorer og betragtes som kontrollerede atomfusionsprojekter på Jorden.
Indtil i dag overvejes tre hovedmetoder til lagring af brint om bord på et køretøj:
- opbevaring i form af komprimeret gas;
- opbevaring i flydende form ved lav temperatur;
- opbevaring i fast form, idet hydrogenet derefter bindes til andre komponenter (ved adsorption eller i form af en kemisk forbindelse).
Komprimeret gas
Det er den mest almindelige form for lagring af brint.
Gaslagring i komprimeret form (i øjeblikket 350 bar) gør det muligt at opnå en tilfredsstillende massefylde med sammensatte tanke. Lagervolumendensiteten forbliver lav: Et tryk på 700 bar er uundgåeligt for at gøre teknologien konkurrencedygtig.
Teknologien findes og bruges ofte. Dens ulempe ligger i den krævede energi til kompression og i den lave effektivitet med hensyn til størrelse sammenlignet med andre metoder. Denne ujævnhed er en af vanskelighederne ved anvendelse af dihydrogen i form af komprimeret gas til bilindustrien.
Ved komprimering er tætheden af brint ved 20 MPa ( 200 bar) ca. 16,8 kg / m 3 , ved 35 MPa ( 350 bar) ca. 23 kg / m 3 og ved 70 MPa ( 700 bar)) på ca. 38 kg / m 3 . Dette svarer til en energitæthedstæthed på 767 kWh / m 3 (27 ° C, 35 MPa) og stadig til en energitæthedstæthed på 33,3 kWh / kg.
Væskelagring ved 20 K ( -253 ° C ) under 10 bar gør det muligt at opnå interessant volumen og massefylde, men kræver tanke med høj varmeisolering for at minimere fordampning.
Teknologien er der. Den har en bedre volumeneffektivitet end opbevaring af komprimeret gas ( 70 kg / m 3 mod 10 kg / m 3 ved 115 bar og 0 ° C ). Denne fordel modereres imidlertid af det relativt store volumen af de nødvendige isoleringsindkapslinger.
På den anden side kræves en betydelig mængde energi for at skifte til den flydende fase: fortætning forbruger 30 til 40% af energiindholdet i gassen, og tabet i reel brug er signifikant (i øjeblikket 1,25 pr. Tusind i timen), stærkt straffe opbevaringen ud over en uge.
Denne teknik anvendes især i rumsektoren, hvor påfyldningen på trods af den korte implementeringstid er kontinuerlig indtil sidste øjeblik.
Metalhydrider
Opbevaring på substrater i adsorberet form, især på metalhydrider , har en meget interessant volumendensitet, men en lav vægtfylde. Derudover forbliver kinetik, temperatur og cykeltryk svære punkter at kontrollere.
Brintatomer opbevares i nogle metalforbindelser. Hydrogenet genvindes ved opvarmning eller reducering af trykket. Denne teknik er dårligt forstået i dag. Det har den ulempe, at det kræver et ekstremt rent dihydrogen for at undgå at ødelægge hydriders absorptionskapacitet. Opvarmning for at genvinde gas er også et handicap. Denne type opbevaring, som fortsat er genstand for forskning, er i den industrielle udviklingsfase, og visse demonstrationsprojekter er planlagt, for eksempel med opstartsprogrammet McPhy, der udvikler magnesiumhydridteknologi (teknologi fra CNRS, NEEL Institute) .
Opbevaringskapacitet for visse hydrider.
| Hydride | Masseprocentdel af H 2 indhold |
|---|---|
| LaNi 5 H 6.5 | 1.4 |
| ZnMn 2 H 3.6 | 1.8 |
| TiFeH 2 | 1.9 |
| Mg 2 NiH 4 | 3.6 |
| VH 2 | 3.8 |
| MgH 2 | 7.6 |
Et meget undersøgt metal er palladium, der via dets hydrid PdH 2har evnen til at absorbere en stor mængde brint i dets krystalgitter. Ved stuetemperatur og atmosfærisk tryk kan palladium absorbere op til 900 gange dets volumen brintgas, idet processen er reversibel.
Den adsorption på carbon gør det muligt at lagre på overfladen af visse carbon- strukturer , såsom aktiveret carbon eller nanorør , molekylerne af hydrogen. Det gør det muligt at lagre 0,05 til 2 vægtprocent dihydrogen .
Denne type opbevaring er på forskningsstadiet.
Produktion og anvendelser
I en rapport offentliggjort i juni 2019, bemærker Det Internationale Energiagentur alsidigheden af brint, som kan produceres fra alle fossile brændstoffer, vedvarende energi og nukleare, kan transporteres i gasform eller flydende form og omdannes til elektricitet eller i metan til en bred vifte af anvendelser.
Vi kan skelne mellem tre kategorier af brint, der produceres, afhængigt af hvordan det produceres (se afsnittet Aktuelle metoder ):
- den brintgrå , produceret ved omdannelse af fossile brændstoffer uden kulstofopsamling og -lagring ;
- den hydrogen blå , produceret af omdannelse af fossile brændstoffer med opsamling og lagring;
- det grønne brint produceret af elektricitet fra vedvarende kilder eller atomkraft ( lilla for nogle, gul for andre).
Hydrogen, der produceres i jordskorpen (ved diagenese og radiolysis ), såvel som primært brint (til stede siden jordens dannelse ) er andre mulige kilder, men som endnu ikke er blevet undersøgt.
I 2020 er omkostningerne ved gråt brint mellem 1 og 2 € / kg mod 4 til 7 € / kg for grønt brint produceret på en industriel måde. Ifølge Julien Chauvet, direktør for Hydrogen France i Engie Solutions , "giver kiloet dig mulighed for at rejse 100 km, hvilket sætter det på niveau med benzin og ligner diesel til lette køretøjer" .
Industriel produktion
Brint produceres i øjeblikket næsten udelukkende fra naturgas , olie og kul .
Til sine egne behov producerer branchen brint ( f.eks. I Frankrig mere end 900.000 t / år brint, især til afsvovling af petroleumsbrændstoffer og til fremstilling af ammoniak i nitratgødning ; brint er derefter et kemisk input og ikke en energi transportør ). Den billigste industrielle proces til produktion af dette brint i 2018 er reformering af kulbrinter , oftest ved dampreformering af naturgas (som hovedsagelig består af metan ). Ved en temperatur mellem 700 og 1.100 ° C , vanddamp til reagerer med metan giver carbonmonoxid og hydrogen. Oprensningen af brint er lettere under højt tryk, reformeringen udføres under et tryk på tyve bar . Hydrogen / carbonmonoxidblandingen omtales sædvanligvis som " syntesegas ". Hvis reaktionen udføres i nærværelse af overskydende vanddamp, oxideres kulilte til det højere oxidationsniveau , hvilket fører til kuldioxid , hvilket øger produktionen af brint .
Virksomheden Air Liquide har en særlig beherskelse af denne proces. I 2015 bestilte den i Saudi-Arabien på Yanbu- stedet en enhed med en samlet brintproduktionskapacitet på 340.000 m 3 / h ved CNTP .
I 2019 vil Australian Renewable Energy Agency (ARENA) yde 9,41 millioner australske dollars (8,5 mio. € ) til et projekt fra Hazer -gruppen (australsk vedvarende energiselskab), der har til formål at konvertere biogas fra metanisering af spildevandsslam til brint og grafit . Hazer ønsker at bygge et demonstrationsanlæg på 15,8 millioner dollars i Munster (Western Australia).
Hydrogensektor og udfordringer for bæredygtig udvikling
Den “traditionelle” industrielle produktion af brint fra fossile kulbrinter har et dårligt CO2-fodaftryk og udsender en masse drivhusgasser og når op på 830 millioner tons CO 2.om året i 2020, dvs. omkring 2% af de globale emissioner og næsten lige så meget som luftfartssektoren eller søtransport. I Frankrig udgør disse emissioner næsten ti millioner tons CO 2 -ækvivalent.årligt omkring 2015-2017, dvs. 7,5% af drivhusgasemissionerne fra den franske industri, ifølge ADEME . Produktionen af brint fra vedvarende elektricitet, som er mere dydig, kunne se omkostningerne falde med 30% inden 2030 takket være boom i vedvarende energi og de dermed forbundne stordriftsfordele .
Den brint sektor producerer, oplagrer, fremmer og forbedrer brint og brint forskning. I 2015 er eksperimenter med grønt (kulfrit) brint i gang, men denne gas fremstilles stadig "hovedsageligt fra naturgas ( fossil ) og bruges som en kemisk komponent i industrielle processer" , med en dårlig kulstofbalance og et betydeligt bidrag til drivhuseffekt . Sektoren præsenteres ikke desto mindre som interessant for bæredygtig udvikling , Fordi:
- hvis det produceres ved elektrolyse af vand og på en kulstoffri måde ved at genvinde intermitterende vedvarende elektricitetsoverskud (hovedsagelig vind- og solceller), kan denne energivektor lagres, især i sæsonbetingede cyklusser, derefter anvendes til metanisering og / eller injiceres i gasnetværket (6 til 20 volumen% afhængigt af forholdene), hvilket letter balancen og fleksibiliteten i elnettet ;
- elektricitet, der kan lagres takket være dens omdannelse til gas (brint eller metan) ville gøre det muligt at lagre "af størrelsesordenen en terrawattime om året" og op til flere titalls terawatt-timer om året el ifølge ADEME , når indtrængningshastigheden for vedvarende energi i elmixet vil nå 80%og som sådan kunne "yde et vigtigt bidrag til overgangen til en lavemissionsmodel, især i energilagringssektoren" ;
- brint kan bruges til at producere elektricitet lokalt, men med et tab af effektivitet; den for vand elektrolysen nærmer 70%, men den samlede effektivitet af el-produktion fra H 2 ville være omkring 25% ifølge Ademe i 2020;
- brint er kompatibelt med selvforbruget af et hjem, en ø eller et distrikt, hvilket muliggør opbevaring over flere dage, uger eller måneder ud over batterier, der er mere nyttige til kortvarig opbevaring. Det ville allerede være økonomisk berettiget I områder, der ikke er forbundet til det kontinentale elnet ( f.eks .: isolerede øer, franske oversøiske samfund, hvor elproduktion stadig afhænger af brændstof til høje omkostninger, til 225 € / MWh i gennemsnit i 2013 i henhold til til ADEME);
- brint kan brænde visse flåder af professionelle køretøjer uden at kræve et dyrt netværk med flere hundrede servicestationer over hele landet. Ifølge Ademe er "den økonomiske model for en station til en flåde tilgængelig til et dagligt forbrug på mere end 80 kg H 2 / dag til markedsføring af brint på mindre end 10 € / kg " . I dette tilfælde har det fordelene ved en hurtig opladningstid og en stor autonomi;
- brint kan bruges i stålindustrien som erstatning for kul eller naturgas til reduktion af jernmalm. Brug af denne proces i Frankrig ville forbruge 700.000 tons brint, men ville undgå emission Af 22 MtCO 2/ år eller næsten 5% af landets emissioner angiver den franske sammenslutning for brint- og brændselsceller (Afhypac).
det 8. juli 2020, fremlægger Europa -Kommissionen et program for udvikling af grønt brint, der sætter det mål, at brint skal dække 12 til 14% af energibehovet inden 2050 for at afkulstoflægge visse sektorer inden for industri og transport. Det er afhængigt af brint til at bidrage til energiomstillingen og til reduktion af drivhusgasemissioner. Samtidig annoncerer EU-kommissæren for intern handel, Thierry Breton, oprettelsen af brintalliancen.
I FrankrigDen ADEME overvejer en elmix til 40% består af "vedvarende" i år 2035, derefter til 60% og 70% i 2050 (mod næsten 18% i 2017, mens hovedparten af vandkraft kilde).
Sektoren søger at industrialisere sine processer for at reducere sine omkostninger (især brændselscellens ). Udviklingen af "brintmobilitet" hæmmes også af et stadig meget lavt antal ladestationer (og deres stadig lave kapacitet: 10 til 80 kg H 2 / d ved 350 bar). Brint kan forbedre køretøjets effekt, udvide dets rækkevidde og forbedre genopladningshastigheden sammenlignet med batterier.
Ademe mener, at brint vil have en vigtig rolle i energiovergangen, som en vektor til optimering af energinetværk, til lagring af energi i solforbrug eller solcelleanvendelse og for visse erhvervskøretøjer, på betingelse af at det dekarboniserer sin energi. Produktion gennem elektrolyse ved hjælp af grøn elektricitet og omdannelse af biomasse ( dampreformering af biogas , pyrogasificering af fast biomasse). Sektorens miljøpræstationer vil først og fremmest afhænge af "den primære kilde, der bruges til fremstilling af brint". Agenturet opfordrer til at begrænse brintransportafstanden mellem fremstillingsstedet og distributionsstationen til mindre end hundrede kilometer. Batteridrevne køretøjer bør foretrækkes, når det er muligt (rækkevidde, tilgængelighed osv.), I betragtning af denne lagers bedre ydeevne og energibesparelser er fortsat en prioritet. En af de muligheder for udvikling (i øjeblikket testet i 2018/2019) er injektion i gasnettet i Frankrig via to demonstranter: GRHYD og Jupiter 1000 , for at fjerne de tekniske hindringer, der stadig findes.
I juni 2018, den franske regering giver Ademe mandat til at lancere den "nationale plan for udrulning af brint" (eller " brintplanen ") for at give drivkraft til denne sektor, hvis "høje potentiale" opfattes af offentlige aktører. Regeringens mål er "at skabe en kulstoffri fransk industrisektor, at åbne nye perspektiver for lagring af vedvarende energi og at udvikle nul-emissionsløsninger til transport" . Et år senere foretog det offentlige agentur flere indkaldelser af projekter , herunder "brintmobilitetsøkosystemer", som gjorde det muligt at vælge projekter "i alle områder" og diversificerede, såsom "last mile levering i byområder., Kollektiv passagertransport med bus- eller søtransport, biludlejning, affaldsindsamling, erhvervs- og samfundsflåder eller endda brug af tunge godskøretøjer som anlægskøretøjer ” .
Den CEA lover en ny industriel elektrolyse teknologi, kaldet RSOC med en enkelt ædelmetal: Indium (et metal, der anvendes i LCD -skærme ), med lavere temperaturer (fra 700 ° C til 800 ° C ) og en nedre temperatur. Strømforbrug. Det er også reversibelt, hvilket gør det muligt at producere brint eller at genoprette elektrisk energi, såsom en brændselscelle.
I slutningen af 2019 slog Air Liquide og Engie sig sammen med Durance-Luberon-Verdon Agglomeration (DLVA) for at producere, opbevare og distribuere "grønt brint" (som en del af projektet "HyGreen Provence", der blev lanceret i 2017, målrettet 1.300 GWh solenergi og flere tusinde tons: år med brint produceret ved elektrolyse Flere titusinder af tons vedvarende brint om året kunne produceres på lang sigt, som kan opbevares i et lokalt saltvandskavitet .
Det franske firma McPhy , som allerede har installeret 17 MW brintproduktionskapacitet ved elektrolyse under tryk, inklusive 6 MW hos Audi i Tyskland, annoncerer i januar 2020 underskrivelsen af ingeniørkontrakten for et produktionsprojekt på 20 MW industrielt grønt brint , det største projekt til dato i Europa, der ligger i Delfzijl i Holland inden 2022. Anlægget producerer 3.000 ton brint pr. år ved elektrolyse af vand med vindkraft og vil blive brugt til fremstilling af bioethanol. Projektet drager fordel af 15 millioner euro i tilskud fra EU og en hollandsk fond. Ifølge McPhy vil den rigtige skala være 100 eller 200 MW for at opnå en konkurrencedygtig pris i branchen.
Den Energi Klima lov november 2019 giver regeringen et år til at oprette en støttemekanisme til "brint fra vedvarende energi eller ved elektrolyse af vand ved hjælp af kulstoffattig elektricitet." . Før 2023 har det flerårige energiprogram til formål at dekarbonisere 10% af det brint, der forbruges i industrien, hvilket kræver produktion af 90.000 ton grønt brint. I januar 2020 lancerer regeringen en opfordring til interessetilkendegivelser , der skal teste industriernes appetit på emnet, der modtager mere end 160 projekter. Eksempelvis indgav H2V Industry i januar byggetilladelsesansøgninger til to brintproduktionsanlæg i industriområdet Port-Jérôme, i Normandiet og på den store søhavn i Dunkerque fra vedvarende elektricitet; hvis de formår at drage fordel af en støttemekanisme, kan deres idriftsættelse finde sted i 2023-2024, og de vil producere 56.000 ton brint. De store franske industrielle aktører (Engie, EDF, Air Liquide, Vinci osv. ) Har også positioneret sig.
Castex-regeringen annoncerede i september 2020 en meget mere ambitiøs plan end den, der blev præsenteret af Nicolas Hulot i 2018, udstyret med 100 mio. 2021 og 2022 som en del af genopretningsplanen. Regeringen planlægger at subsidiere produktionen af grønt brint gennem udbud, der er baseret på vedvarende energikilder, og opførelse af brændselscelleanlæg til brintkøretøjer. Partnerskaber med Tyskland, der afslørede en brintplan på 9 mia. € i juni, overvejes for at undgå dobbeltarbejde.
Denne brintplan inkluderer en første komponent på 1,5 mia. Euro afsat til fremstilling af elektrolysatorer for at reducere omkostningerne ved at forbedre den og øge volumener til en kapacitet på 6,5 GW . Den anden komponent på næsten en milliard euro vil blive brugt i 2023 til at udvikle et tungt brintmobilitetstilbud ved at reducere omkostningerne og forbedre effektiviteten af brændselsceller til tog, lastbiler, busser og fly via flere indkaldelser af projekter (350 millioner euro til demonstranter, 275 millioner til regionale forsøg osv.). Endelig vil bistand til forskning og innovation blive stimuleret med en kuvert hævet til 650 millioner inden 2023. Bruno Le Maire håber, at denne plan vil skabe mellem 50.000 og 150.000 direkte og indirekte arbejdspladser. Regeringen overvejer samarbejde med Tyskland beskrevet som "Airbus til elektrolyse" som "Airbus til batterier". Frankrig har sat sig som mål at producere 600.000 tons om året grønt brint fra kulstoffri elektricitet, af vedvarende eller nuklear oprindelse. I modsætning til Tyskland vil Paris dog ikke subsidiere opsamling af kulstof fra "gråt" brint. Bruno Le Maire håber at se "fremkomsten af en fransk elektrolysesektor": sammen med giganter som Air Liquide er der også mange start-ups, såsom Lhyfe , der er baseret i Nantes, som udvikler grønne produktionssteder for brint til producenter og lokale myndigheder, eller endda McPhy , en Drôme-producent af elektrolysører, hvor EDF er aktionær.
I BelgienEt KUL-team designer en prototype 1,6 m 2 fotoelektrokemisk celle, der i gennemsnit producerer 250 liter brint pr. Dag fra atmosfærisk vanddamp. Enheden omdanner 15% af solenergien til brint og ilt. Og denne teknologi bruger ikke ædle metaller eller andre dyre materialer. Med tyve paneler ville et velisoleret hus være selvforsynende med el og varme i et år.
Colruyt Group (en stor belgisk forhandler) ønsker at afkarbonisere sine aktiviteter så meget som muligt. I 2018 var et af dets logistikcentre udstyret med 75 elevatorer drevet af "kulstoffrit" brint, og dets lastbilflåde skal konverteres inden 2030. Med en gasafspiller forberedes et installationsprojekt på 12 til 25 MW . (Udvides) at konvertere elektricitet fra offshore vindmøller vindmøller til brint , i industriel skala.
I JapanI slutningen af 2017 bekræftede Japan, en stor energiimportør, at det ønskede at blive førende som et " brintfirma " med et mål om "omkostningsparitet" med benzin og LNG til elproduktion. Som med atomkraft tidligere præsenteres brint som et vigtigt middel til afkulning af energi, men pilotprojekterne vil give deres konklusioner omkring 2020. I 2018 er Japan i spidsen for brintmobilitet med næsten 2.500 biler med brintbrændstofceller i cirkulation og mere end hundrede brintstationer (mod 45 i Tyskland, 42 i USA og omkring 20 i Frankrig på samme tid). Landet sigter mod at opdele produktionsomkostningerne med mere end tre inden 2030, derefter med 80% inden 2050. Mellem 2013 og 2017 har den japanske stat allerede investeret 1,5 mia. Dollars i F&U og udvikling af brint.
I CalifornienI oktober 2019, Californien har 7.570 registrerede brintbiler og 42 amerikanske offentlige stationer.
I TysklandDen tyske regering vedtager en ambitiøs plan for udviklingen af "grønt" brint, udstyret med 9 milliarder euro.
Brintmotor
Kernefusion: H-bombe- og fusionsreaktorer
Farer, risici og forholdsregler
Dihydrogen er en gas klassificeret som "ekstremt brandfarlig ". Det er kendetegnet ved et meget bredt antændelsesområde (fra 4 til 75% af volumenet i luft), hvilket forårsager en deflagration fra en meget lav aktiveringsenergiindgang (en gnist er tilstrækkelig, hvis den giver en. Energi på 0,02 millijoules (mJ), mens det tager 0,29 mJ at udløse en eksplosion af metan ). Dihydrogen blandet med ilt i støkiometriske proportioner er et kraftigt sprængstof . Dihydrogen i luft er en eksplosiv blanding , når H 2 / luft volumenforhold er mellem 13 og 65%
Historien om dets anvendelse i luftskibe er fyldt med alvorlige ulykker, hvoraf den mest berømte er Hindenburg-katastrofen . De LS 129 zeppeliner , oppustet med 200.000 kubikmeter brint (fordi USA havde erklæret en embargo mod Tyskland for helium ) brændte6. maj 1937ved ankomsten til Lakehurst Airfield , nær New York ). 36 mennesker døde ud af i alt 97 indledte. Mediebilledet afslørede bredt billederne af katastrofen, hvilket førte til offentlig utilfredshed med ballonerne. Undersøgelserne af ulykkens oprindelse lettet af overflod af fotografiske dokumenter inkriminerede imidlertid ikke en eksplosion af brint, men en antændelse ved sammenhæng fra en brand i konvolutten (sandsynligvis forårsaget af statisk elektricitet). Sammensætningen af den vandtætte belægning af konvolutten (butyrater og aluminium) ville have begunstiget en voldsom aluminoterm reaktion . Ulykken ville dog have været meget mindre voldelig, hvis ballonen var blevet oppustet med helium.
Udskiftningen af brint med helium (meget dyrere og tættere) producerede ikke den forventede genoplivning. Frygten for brint forblev; den ”Hindenburg syndromet” har formentlig uretfærdigt straffet branchen.
Dihydrogen reagerer endnu mere voldsomt med chlor for at danne saltsyre (HCl), selv uden aktivering, og med difluorid til dannelse af farlig flussyre (HF), selv ved temperaturer, hvor hydrogen er flydende og fluorfast, sidstnævnte reaktion er den mest eksoterme kemiske reaktion der er.
Den standard sikkerhed styrkes for at imødegå de risici, som den passage i tunneller og parkering i garager eller parkeringskældre.
Globale køretøjsregler udvikles i FN -regi på baggrund af forslag fra producenter, men med hensyn til dihydrogen er japanske, amerikanske og europæiske producenter ikke enige. Europa -Kommissionen kan træffe afgørelse om foreløbige fællesskabsbestemmelser.
I Frankrig arbejder INERIS og CEA sammen med Den Internationale Standardiseringsorganisation ( ISO ) i et teknisk udvalg ved navn TC 197 om brintrisiko. Et europæisk Hysafe- projekt behandler også spørgsmålet, hvor INERIS kritiserede udkastet til forordning ved at foreslå en mere global og systemisk tilgang og ikke efter komponent til godkendelse af hybridbiler . I 2015 udarbejdede MEDDE en opdatering af reglerne for tankstationer og flåder af køretøjer, der kører på brint.
Ozonlagsfare
En massiv frigivelse af brintgas har rejst hypotesen om en risiko for ozonlaget .
Sikkerhedsforanstaltninger
Følgende punkter er bemærkelsesværdige:
- brint er ikke iboende giftigt;
- den er otte gange lettere end metan. Dens meget lille molekyle giver det en meget god diffusionskoefficient i luften (fire gange metan); i et ubegrænset miljø har brint derfor en tendens til at stige og hurtigt fortyndes i luften (det er en sikkerhedsfaktor i det fri og en farefaktor på lukkede steder);
- det er den mest energiske kemiske art pr. masseenhed (120 kJ / g ); men pr. gasvolumen er den teoretiske eksplosive energi 3,5 gange lavere for brint end for naturgas;
- dens nedre antændelsesgrænse er 4 volumenprocent, sammenlignelig med naturgas (5 volumenprocent); men dens øvre grænse for inflammation er signifikant højere (75% mod 15%); dette betyder, at hydrogen i tilfælde af lækage antændes meget lettere end naturgas eller flydende brændstoffer;
- energien, der kræves for at antænde den ved støkiometri, er også betydeligt lavere (ca. 10 gange) end naturgas eller propan;
- brintflammen, lyseblå, er næsten usynlig i løbet af dagen (risiko for nødtjenester)
- brintflammen formerer sig cirka syv gange hurtigere end naturgas, og risikoen for detonation (eksplosion med en meget kraftig sprængningseffekt) forværres af dens høje diffusivitetskoefficient.
Antændelighed kan yderligere reduceres ved at fortynde brint i helium, selv ved meget høj temperatur.
FN -reference for transport af farligt gods
- Navn (fransk): Komprimeret brint
- Klasse: 2
- nummer: 1049
- Navn (fransk): Kølet flydende brint
- Klasse: 2
- nummer: 1966
- Navn (engelsk): Brint i en metalhydridlagringsenhed
- Klasse: 2
- nummer: 3468
Noter og referencer
- HYDROGENE , sikkerhedsark (er) til det internationale program for sikkerhed for kemiske stoffer , hørt den 9. maj 2009
- beregnet molekylmasse fra " Atomic vægte af elementerne 2007 " på www.chem.qmul.ac.uk .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 s. , Indbundet ( ISBN 978-1-4200-9084-0 ).
- Jean-Louis Vignes ( dir. Og medlem af Chemical Society of France) et al. , " Dihydrogen: Physico-Chemical Data " , salgsfremmende og uddannelsesmæssigt websted vedrørende kemiske grundstoffer (fra det periodiske system af Dmitri Mendeleïev ), på lelementarium.fr , Paris og Puteaux , Société Chimique de France og Frankrig Chimie (adgang til 3. november 2019 ) .
- Pierre Ravarini (kemiingeniør & hydrolog), " Gaz-Hydrogen " , sted for videnskabelig, teknisk og økologisk information om vand, Côte de Nacre ( Calvados ), 2019(adgang til 3. november 2019 ) .
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 978-0-387-69002-5 og 0-387-69002-6 , læs online ) , s. 294
- (da) Robert H. Perry og Donald W. Green , Perrys kemiske ingeniørhåndbog , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- " Egenskaber ved forskellige gasser " på flexwareinc.com (adgang til 12. april 2010 )
- Referat af Den Internationale Komité for Mål og Vægt , 78 th Session, 1989, pp. T1-T21 (og s. T23-T42, engelsk version).
- (i) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 s. ( ISBN 978-1-4398-2077-3 ) , s. 14-40.
- (i) David R. Lide , Gummibibelen , Boca Raton, CRC Press,18. juni 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online præsentation ) , s. 5-89
- Magalie Roy-Auberger, Pierre Marion, Nicolas Boudet, Forgasning af kul , red. Ingeniørens teknikker, reference J5200 , 10. december 2009, s. 4
- " Kontoret for stråling, kemisk og biologisk sikkerhed (ORCBS) " (adgang til 16. april 2009 )
- EF-forordning nr . 1272/2008 , 16. december 2008 [PDF] om EUR-Lex , s. 923 : Bilag VI, tabel 3.1, indeksnummer .
- " Hydrogen " i databasen over kemiske produkter Reptox fra CSST (Quebec-organisation med ansvar for arbejdsmiljø), adgang 23. april 2009
- "brint" , på ESIS , tilgås 15 februar 2009
- " Opdagelsen af brintkilder åbner vejen til en ny energi " , Le Monde .
- ” Naturlig brint, en energi El Dorado? » , Sciences et Avenir .
- Lavoisier eksperimenter , på lavoisier.cnrs.fr
- " Hydrogen energi " , om viden om energier ,30. august 2011(adgang 10. december 2019 ) (opdateret9. april 2015).
- Hydrogenkædeudbytte (teknisk blad), Ademe ,januar 2020( læs online [PDF] ).
- " Påvisning af naturlige brintudstråling ved hjælp af satellitbilleder - Start af sen4H2-projektet " , på IFP Énergies nouvelles (adgang til 6. april 2019 ) .
- “ Dybhavsmineralressourcer ” på Ifremer (adgang 28. oktober 2019 ) .Artiklen præsenterer et kort over havbunden, der giver den kendte slangefordeling langs højderygge.
- Sylvestre Huet , ” Naturligt brint, en ny energikilde? » , På sciences.blogs.liberation.fr , Liberation ,23. april 2013(adgang til 28. oktober 2019 ) .
- " Seawater-mantle reaction: serpentine formation " , om Ifremer (adgang til 28. oktober 2019 ) .
- " Syntese af brint, metan og kulbrinter i dybhavet, mod nye energiressourcer ... " , på Ifremer (adgang 28. oktober 2019 ) .
- " Hydrogen, ja, men naturligt brint " , på La Tribune ,28. juni 2018(adgang til 3. oktober 2020 ) .
- Naturligt brint: et bidrag til energimixet? , IFP Nye energier ,11. april 2013.
- Julia Guélard , Karakterisering af naturlig brint udstrømninger i en intracratonic sammenhæng: eksempel på en gas / vand / rock interaktion i Kansas (doktorafhandling geokemi), Pierre-et-Marie-Curie University og IFP Energies Nouvelles ,2016( online præsentation , læs online ).
- (i) J. Guélard , V. Beaumont , V. ROUCHON og F. Guyot , " Natural H2 i Kansas: Dybt guld overfladisk oprindelse? » , Geokemi, Geofysik, Geosystems , vol. 18, nr . 5,3. april 2017, s. 1841–1865 ( ISSN 1525-2027 , DOI 10.1002 / 2016GC006544 , abstrakt , læst online , adgang til 28. oktober 2019 ).
- Alain Prinzhofer, Eric Deville, Natural hydrogen - Den næste energirevolution? , Ed. Belin, 2015 ( ISBN 978-27011-83848 ) .
- J. Guélard et al. , “ Naturlig H2 i Kansas: Dyb eller lavvandet oprindelse? ", Geokemi Geofysik Geosystems ,april 2017( DOI 10.1002 / 2016GC006544 , online præsentation , læs online [PDF] , tilgås 25. oktober 2109 ).
- (i) Isabelle Moretti, Emyrose Brouilly, Keanu Loiseau, Alain Prinzhofer Eric Deville, " Hydrogen Dampe i Intracratonic Områder: New retningslinier for tidlig screening Basin Exploration " på hmdpi.com ,22. marts 2021(adgang 16. juni 2021 )
- (in) Maria Rosanne Fabian Rupin Louis Gorintin Julio Aguilar, Helena-Fog, Werly Julien Olivier Lhote, Xi Yao, " PARHYS SYSTEM: EN NY TILGANG TIL H2 KONCENTRATIONSMÅLINGER I OVERFLADEN " på hnatsummit.com ,26. april 2021(adgang 16. juni 2021 )
- (i) H. Hosgormez G. Etiope og MN Yalcin , " Nye beviser for et blandet uorganisk og organisk oprindelse Olympic brand Chimaera (Tyrkiet): en bred-shore sivning af gas abiogenic " , Geofluids , vol. 8, nr . 4,25. november 2008, s. 263–273 ( DOI 10.1111 / j.1468-8123.2008.00226.x ).
- " Bourakébougou: løftet om et brintkraftværk " ,18. februar 2013(adgang til 28. oktober 2019 ) .
- " Brint ifølge Isabelle Moretti - Sciences et Avenir " , Sciences et Avenir (adgang til 2. juni 2021 ) .
- (in) "Vulkanske gasser: brændstof med brændstof ved vulkanen Kilauea, Hawaii" på mendeley.com.
- (en) Deep Hydrogen på astrobio.net.
- (en) GJ MacDonald (1988). “Store spørgsmål om dybe kontinentale strukturer” Dybboring i krystallinsk grundfjeld, v. 1 : 28-48 s., Berlin: Springer-Verlag. .
- " Naturligt brint er en meget vigtigere kilde end antaget ifølge CNRS " , på http://erh2-bretagne.mystrikingly.com ,11 maj 2019(adgang til 12. november 2019 ) .
- Isabelle Moretti, " Naturligt brint: geologisk nysgerrighed eller større energikilde i fremtiden?" » , Om viden om energier .
- " Den 15. april 1988 flyver Tu-155 på brint " , på Aerobuzz ,2. oktober 2020(adgang til 12. november 2020 )
- Hydrogen, nye energiteknologier. CEA-tasterne, nr . 50/51, Vinter 2004-2005, ( ISSN 0298-6248 )
- europæiske projekt StorHy rapport, s. 8, brinttabshastighed
- Tribune-artikel Europa finansierer kæmpe batteri til opbevaring af vedvarende energi
- (in) T. Mitsui, MK Rose E. Fomin, DF Ogletree og M. Salmeron, " Dissociativ hydrogenadsorption er palladium kræver aggregater med tre eller flere ledige stillinger " , Nature , bind. 422,17. april 2003, s. 705-707 ( DOI 10.1038 / nature01557 , læs online [PDF] ).
- (da) Fremtiden for brint - udnyttelse af nutidens muligheder [PDF] , International Energy Agency , juni 2019.
- (in) Gasdekarboniseringsveje 2020-2050 , Gas til klima,april 2020, 226 s. ( læs online [PDF] ) , s. 17.
- " Genopretningsplan: hvad sted for energi? » , På connancedesenergies.org ,4. september 2020.
- (in) " Hydrogen produceret fra atomkraft vil blive betragtet som" lavemissions ", siger EU-embedsmand " ["Hydrogen produceret fra atomkraft vil blive betragtet som" lavt kulstofaftryk ", ifølge en EU-embedsmand»], Om EURACTIV ,19. november 2020.
- " Den franske brintplan bekræfter diskret genstart af atomkraft " , på Reporterre ,2. februar 2021.
- " Naturligt brint: en geologisk nysgerrighed eller en stor energikilde i fremtiden?" » , På connancedesenergies.org ,22. maj 2020.
- “ Grønt brint, det manglende led i overgangen ” , Alternatives économique (adgang 8. august 2020 ) .
- Interaktioner (brev til Air Liquide -aktionærer), Air Liquide , september 2015 [PDF] , s. 5 .
- (i) Liz Gyekye [ https://biomarketinsights.com/australia-backs-tech-that-converts-biogas-into-hydrogen-and-graphite/ "Australien rygge tech der konverterer biogas til hydrogen og grafit"] Biomarketing seværdigheder , 4. sep. 2019.
- Jérôme Marin, " Lhyfe vil producere grøn brint med vindmøller " , La Tribune ,17. januar 2020.
- "The Ademe lister de" store bidrag "fra brint til energiovergangen" , Connaissance des energies , 4. april 2018.
- Brintvektoren i energiovergangen , udtalelse fra ADEME, april 2018 [PDF] .
- Séverine Fontaine, " Ademe ønsker brint fra vedvarende energi ", L'Automobile & L'Entreprise , nr . 5,februar 2016( læs online ).
- " Europa -Kommissionen afslører sin grønne brintudviklingsplan " , på EnerGeek ,10. juli 2020(adgang 11. juli 2020 ) .
- Brint i energiomstillingen , Ademe , februar 2016, 7 sider [PDF] .
- Joseph Martin , " Udvikling af brint, ADEME tager status " , på RSE Magazine (adgang til 17. maj 2019 ) .
- " Grenoble forskere optimerer kunstig fotosyntese til at producere brint " , på placegrenet.fr ,21. april 2018(adgang til 30. marts 2019 ) .
- Véronique Pouzard, " Høj temperatur elektrolyse af CEA båret af opstarts Sylfen " , Les Échos ,26. februar 2019(adgang til 30. marts 2019 ) .
- AFP (2019) “Grønt” brint: samarbejde mellem Air Liquide, Engie og Durance, Lubéron, Verdon agglomeration ; 13. november 2019
- McPhy i centrum for den største brintproduktionsenhed uden kulstof i Europa , Les Échos , 22. januar 2020.
- Genopretningsplan: Frankrig ændrer skala i brint , Les Échos , 3. september 2020.
- Brint: Frankrig beskriver sin plan til 7 milliarder euro , Les Échos , 8. september 2020.
- Brint: regeringen vil oprette en "Airbus til elektrolyse" , Les Échos , 8. september 2020.
- (in) " KU Leuven-forskere knækker koden for overkommelig, miljøvenlig brintgas " på KU Leuven (adgang til 31. oktober 2019 ) .
- " Belgiske forskere udvikler et solpanel, der producerer brint " , på RTBF Info ,1 st marts 2019(adgang til 31. oktober 2019 ) .
- " Colruyt Group: indsatsen på brintmobilitet " , på RTBF Info ,8. oktober 2018(adgang til 31. oktober 2019 ) .
- " Colruyt og Fluxys ønsker at bygge et brintanlæg, et første i Belgien " , Le Soir ,8. oktober 2019(adgang til 31. oktober 2019 ) .
- " Kørsel på brint: vores erfaring " , Le Moniteur-bil (adgang til 31. oktober 2019 ) .
- (en) Monica Nagashima (Institute of Energy Economics, Japan), Japans brintstrategi og dens økonomiske og geopolitiske konsekvenser , Institut français des relations internationales , oktober 2018 [PDF] .
- "Japans" brintstrategi " , viden om energier, 9. oktober 2018.
- (in) " Alternativt brændstofdatacenter: brintbrændstofstationsferie " , om alternativt brændstofdatacenter , USAs energiministerium (adgang til 31. oktober 2019 ) .
- Benoît Le Floc'h, “ Hvad med brint til lette erhvervskøretøjer? » , Om Caradisiac ,29. november 2018(adgang til 30. marts 2019 ) .
- " Californien passerer milepælen om 7.500 brintbiler i omløb " , på www.h2-mobile.fr (adgang 31. oktober 2019 ) .
- (i) " tyske regering vedtager brintstrategi " [ "Den tyske regering vedtager strategi for brint"], om forbundsregering (Tyskland) ,10. juni 2020.
- Hydrogen accidentology , Ministeriet for økologi, energi, bæredygtig udvikling og regional planlægning , 18 s. ( læs online [PDF] ) , s. 4.
- Radisson, Laurent (2015) Brintrisici: Økologiministeriet arbejder på nye tekster; ; News env, offentliggjort 21. oktober 2015
- T. Rahn, JM Eiler, KA Boering, PO Wennberg, MC McCarthy, S. Tyler, S. Sc Chauffage, S. Donelly, E. Atlas, Extreme deuterium berigelse i stratosfæren hydrogen og den globale atmosfæriske budget H2 , Nature 424 , 918-921, 2003.
- TK Tromp , RL Shia , Mr. Allen , JM Eiler og YL Yung , " Potentiel miljøpåvirkning af en brintøkonomi på stratosfæren ," Science , nr . 300,2003, s. 1740-1742 ( DOI 10.1126 / science.1085169 ).
- Céline Duguey, " En eksplosiv oplevelse " , på Espace des Sciences ,september 2009(adgang til 16. april 2020 ) .
- (i) Florent Tonus Mona Bahout , Paul F. Henry og Siân E. Dutton , " Anvendelse af i situneutron diffraktion til at overvåge høj temperatur, faststof / H2-gas-reaktioner " , Chemical Communications , n o 18,21. april 2009, s. 2556–2558 ( ISSN 1364-548X , PMID 19532888 , DOI 10.1039 / B822419F , læst online , adgang til 16. april 2020 ).
Se også
Bibliografi
- Yver, Camille, Kvantificering af jordens anvendelse af brint: fra lokal til global skala , 2011 DOI: 10.4267 / 2042/47372 ( resumé - Prix Prud'homme 2011.
- Stephen Boucher, Hydrogenrevolutionen. Mod ren og effektiv energi? , forord af Thierry Alleau, Paris, Éd. du Felin, 2006, 160 s. , ( ISBN 2-86645-616-5 ) .
- Alain Prinzhofer, Eric Deville, Natural hydrogen - Den næste energirevolution? , Belin, 2015 ( ISBN 978-27011-83848 )
Relaterede artikler
eksterne links
- Fransk brintforening
- Europæisk netværk / Kompetencepol
- H2 -udvikling
- CEA Technologies, Hydrogen, nye energiteknologier , Clefs CEA nr . 50-51), 23. marts 2005
- Hydrogen set af CEA
- INERIS: oplev feedback i forbindelse med opbevaringsvanskeligheder
- Hydrogen set af French Chemistry Society
- Kontroversen om brugen af brint som brændstof
- Alt om brintalternativet, med en presseanmeldelse, internetlinks og videoer








