Myasthenia gravis
Myasthenia gravis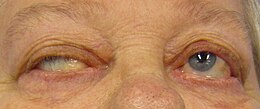 Ptosis hos en person med myasthenia gravis, der forsøger at åbne deres øjne.
Ptosis hos en person med myasthenia gravis, der forsøger at åbne deres øjne.
| Specialitet | Neurologi |
|---|
| ICD - 10 | G70.0 |
|---|---|
| CIM - 9 | 358,0 |
| OMIM | 254200 |
| Sygdomme DB | 8460 |
| MedlinePlus | 000712 |
| e-medicin | 1171206, 793136, 261815 og 1216417 |
| e-medicin |
neuro / 232 emerg / 325 (nødsituation), med / 3260 (graviditet), oph / 263 (øje) |
| MeSH | D009157 |
| Medicin | Pyridostigmin , neostigmin , ciclosporin , cyclophosphamid , prednison , azathioprin , rituximab , eculizumab , mycophenolatmofetil ( d ) , prednisolon , tacrolimus , distigmin ( d ) og pyridostigmin |
| UK patient | Myasthenia-gravis-pro |
De gravis (græsk μύς "muskel" og ἀσθένεια "svaghed"), i Latin gravis er en neuromuskulær sygdom autoimmun kronisk , manifesteret i varierende grader ved svaghed og træthed overdreven af tværstribet skeletmuskulatur , c dvs. dem, som aktiveres frivilligt. Det skylder sit navn til den tyske neurolog Friedrich Jolly (1844-1904) og har også et eponymt navn : Erb - Goldflam sygdom , til ære for de to klinikere, der gav den mest komplette beskrivelse. Det er forårsaget af antistoffer, der cirkulerer, at de i mere end tre ud af fire tilfælde målretter mod receptorer af acetylcholin i neuromuskulær forbindelse , og derved hæmmer den excitatoriske virkning af denne neurotransmitter .
Historisk
Det var sandsynligvis Thomas Willis, der først beskrev en patient med myasthenia gravis. Jolly navngiver sygdommen ved at opfinde udtrykket “ myasthenia gravis pseudoparalytica ” og fremhæver den elektrofysiologiske forringelse. Mary Walker foreslog i 1934 behandling med fysostigmin . Abnormiteter i thymus i forhold til MG er kendt, og thymektomi praktiseret fra begyndelsen af det XX th århundrede , før forståelsen af patofysiologien og identifikation af autoimmun genese.
Epidemiologi
Dens udbredelse varierer fra 5 til 10 pr. 100.000 indbyggere og dens forekomst mellem 2 og 20 pr. År og pr. Million indbyggere afhængigt af serien. Kan forekomme i alle aldre, dets højeste forekomst vedrører aldersgruppen 20 til 30 år. Kønsforholdet mellem patienter, 3 kvinder til 2 mænd, varierer efter aldersgruppen (2 kvinder til 1 mand for dem under 50, 1 kvinde til 1 mand for dem over 50). I det væsentlige sporadisk sygdom er familiens former usædvanlige.
Patofysiologi
Den formodede patofysiologi af myasthenia gravis består af beskadigelse af de postsynaptiske membranproteiner i det neuromuskulære kryds ved cirkulerende autoantistoffer . Det primære antistofmål matchede acetylcholinreceptor (en neurotransmitter ), der fungerede som en konkurrencedygtig hæmmer af acetylcholin og fremskyndede nedbrydningen af receptoren ved antigen modulering. Dette resulterer i en stigning i antallet af acetylcholin-kvanta, der kræves for at producere depolarisering af den postsynaptiske membran, hvilket fører til en hurtigere og dybere nedbrydning af presynaptisk acetylcholinlagre og klinisk resulterende i muskeltræthed.
På mellemlang sigt kan tilstedeværelsen af disse antistoffer via aktivering af komplementsystemet inducere anatomiske ændringer af den postsynaptiske membran, hvilket yderligere reducerer dets ophidselse. På dette stadium i de mest alvorlige former kan der opstå permanente underskud.
Med undtagelse af D-penicillamin og allogen marvstransplantation er der ikke identificeret noget eksogent middel, der fremmer udbruddet af myasthenia gravis. Der er en lille genetisk disposition, især HLA B8 (en) og DR3 (en) grupperne med DR1 (en) mere specifik for okulær myasthenia gravis. Mange andre autoantistoffer er for nylig blevet identificeret som patogener, der alle er målrettet mod en komponent i den postsynaptiske membran: anti-MuSK ( muskelspecifik kinase ) antistoffer, anti-agrin antistoffer, anti-LRP4 antistoffer. Thymusens rolle i patogenesen demonstreres. Det er sæde for T-lymfocytmodning . Under stimulering af sidstnævnte transformeres B-lymfocytterne til plasmaceller, der udskiller antistoffer.
Kliniske manifestationer
De kliniske træk kan beskrives som følger:
kardinal symptom og afgørende for diagnosen er træthed ved anstrengelse. Symptomerne svinger derfor, intensiveres med anstrengelse og forbedres i hvile. De er ofte mere markerede i slutningen af dagen og kan forværres i stressende situationer: infektion, kirurgi, varme ... Endelig kan den kliniske undersøgelse derfor være strengt normal eller ikke meget forstyrret, stresstest giver derefter anomalier mulighed for at blive demaskeret.
Muskellokaliseringen og de resulterende symptomer er variable:
- i 50% af tilfældene er den oprindelige klage ptosis , diplopi eller begge dele. Disse symptomer er ofte svingende, som regel opstår eller forværres i slutningen af dagen, eller når du læser eller kører et køretøj. Dette er den klage, der er mest stemningsfuld af diagnosen og tillader den eneste specifikke kliniske diagnostiske test. Udseendet af en ptose med oftalmoparese (hængende øjenlåg med konvergensbesvær) ved den excentriske fiksering af blikket forlænget et par minutter hos en tidligere asymptomatisk patient er faktisk karakteristisk. Hos en symptomatisk patient er isterningstesten (forbedring af ptosis efter placering af is i et par minutter på det symptomatiske øjenlåg) mindre specifik, men meget stemningsfuld;
- i 20% af tilfældene vedrører den oprindelige klage en træthed i lemmerne, ofte i dens proximale dele, hvilket kan føre diagnosen til myopati. Gentagne stresstest kan afmaskere segmental træthed, men er ikke særlig specifikke;
- i 10% af tilfældene består den oprindelige klage af isoleret asteni (generaliseret træthed, ofte forvekslet med ægte muskelsvaghed), som ikke skulle antyde diagnosen som den første hensigt, medmindre ægte muskelsvaghed er blevet objektiviseret af en læge og lader træthed være forgrunden. Dette er den mest uspecifikke klage, og kliniske tests har kun ringe nytte;
- ganske sjældent vil de indledende klager bestå af svingende lidelser med at tygge, synke eller svaghed i nakkeforlængerne;
- observationen af en global oculo-cephalisk involvering, der producerer de "myastheniske facies" er sjælden, men meget stemningsfuld (asymmetrisk palpebral ptose, hængende underlæbe, sletning af pande rynker, mulige ekstrinsiske oculomotoriske lidelser og svaghed i nakkeforlængerne) Den fluktuerende karakter af disse ansigter gør det muligt at skelne den fra mange andre årsager til ansigtsdiplegi og at bekræfte diagnosen.
Per definition er symptomerne kun motoriske, og sensoriske klager er fraværende. På grund af overdreven kompenserende indsats kan patienten dog fremhæve følsomme, smertefulde klager (myalgi, artralgi, paræstesi), der fører diagnosen til reumatisk patologi, myopati, stofskifteforstyrrelse, polyneuropati eller myelopati.
Ved undersøgelse er myotatiske reflekser normale, og atrofi observeres kun i alvorligt avancerede former.
Man skelner mellem generaliserede former, bulbarformer og rene okularformer. Forskellige kombinationer kan dannes (oculo-bulbar former). Rene okulære former er begrænset til svækkelse af ekstern oculomotricity og ptosis. Ti til tyve procent (10 til 20%) af okulære former forbliver på dette stadium, deaktiverende men mild form af sygdommen, mens de andre udvikler sig til generaliseret myasthenia gravis.
De indledende bulbarformer (15%) inkluderer en næsestemme med vanskeligheder med at artikulere, tyggesvaghed med en tendens til at tabe kæben, sværhedsvanskeligheder (dysfagi) med falsk mad eller spytveje.
Sygdomsforløbet opstår typisk gennem en række forværringer og remissioner, muligvis blandet med ægte “myastheniske kriser” for generaliserede former. Disse kriser, ægte medicinske nødsituationer, defineres ved en pludselig forværring med akut respirationssvigt, dyspnø med overbelastning, synkeforstyrrelser med risiko for aspiration eller alvorlig generaliseret svaghed med impotens, der ikke giver plads til hvile.
Stadiet med maksimal sværhedsgrad nås inden for tre år hos mere end tre fjerdedele af patienterne.
I 1 til 5% af tilfældene erklæres sygdommen af en indledende myasthenisk krise. Diagnosen er så yderst vanskelig og skal fremkaldes i tilfælde af en uforholdsmæssighed mellem den formodede kausale patologi og den kliniske sværhedsgrad eller i tilfælde af uforklarlige gentagne fejl i forsøg på at fravænne mekanisk ventilation, den anden diagnose skal fremkaldes i sådanne situationer. er en akut polyradiculoneuritis.
Osserman Clinical Classification eller MGFA (Myasthenia Gravis Foundation of America)
Denne klassificering beskriver flere faser:
- fase I : svaghed i øjenmuskelen, mulig ptose. Ingen anden muskelsvaghed
- fase II : svaghed i øjenmuskler af enhver sværhedsgrad, mild svaghed i andre muskler
- fase IIa : overvejende svage lemmemuskler eller trunkmuskler
- trin II b: dominerende svaghed i åndedrætsmusklerne eller synkeforstyrrelser
- trin III : svaghed i øjenmuskler af enhver sværhedsgrad, moderat svaghed i andre muskler
- fase IIIa : overvejende svage lemmemuskler eller trunkmuskler
- trin III b: Overvejende svaghed i åndedrætsmusklerne eller synkeforstyrrelser
- trin IV : svaghed i øjenmuskler af enhver sværhedsgrad, svær svaghed i andre muskler
- trin IV a: overvejende svaghed i lemmemuskler eller trunkmuskler
- trin IV b: dominerende svaghed i åndedrætsmusklerne eller synkeforstyrrelser. Kan også omfatte et behov for et nasogastrisk rør uden intubation
- trin V : intubation er nødvendig for at opretholde vejrtrækningen
Særlige former
Forskellige former for myasthenia gravis fortjener at blive individualiseret af deres præsentation og deres særlige ledelse.
Autoimmun føtal og neonatal myasthenia gravis
Moderkagen er gennemtrængelig for antistoffer. Ti til tyve procent (10 til 20%) af børn af mødre med myasthenia gravis har neonatal myasthenia gravis, der forekommer inden for de første 3 dage og forsvinder normalt inden for få uger (maksimalt 3 måneder). Symptomer, der varierer fra barn til barn, inkluderer: hypotoni, svagt gråd, forstyrret sugning eller synke, ptose, diplegi i ansigtet og åndedrætsbesvær. Behandlingen er baseret på symptomatisk behandling i en neonatal intensivafdeling indtil opløsning og administration af antikolinesterase-lægemidler. Udviklingen er generelt gunstig. I de mest alvorlige former kan en exsanguinotransfusion udføres.
Fosterformer er sjældnere og kan resultere i intrauterin væksthæmning. Undtagelsesvis forekommer svære kliniske manifestationer (hydramnios, arthrogryposis, død in utero).
Infantil og ung autoimmun myasthenia gravis
Myasthenia gravis begyndende inden 15 år, denne form fortjener at blive individualiseret ved den vanskelige skelnen fra medfødte ikke-autoimmune myasthenia gravis og behovet i betragtning af alderen at begrænse brugen af kortikosteroider og immunsuppressiva så meget som muligt.
Autoimmun iatrogen myasthenia gravis
Enestående, deres diagnose er generelt tydelig på baggrund af klinisk historie. De involverer de samme autoantistoffer og reagerer på de samme behandlinger som klassisk myasthenia gravis. Imidlertid vil de sandsynligvis reagere på specifik behandling. Indtil videre er kun blevet demonstreret:
- D-penicillamin-induceret myasthenia gravis. Det vedrører 1% af patienterne behandlet med D-penicillamin. Genopretning efter standsning af D-penicillamin inden for 6 måneder er reglen;
- myasthenia gravis induceret af allogen margtransplantation med transplantat versus værtssygdom.
Tilknyttede patologier
Visse patologier på grund af hyppigheden af deres tilknytning til myasthenia gravis eller alvorligheden af deres iboende spontane prognose bør undersøges systematisk.
Thymiske tumorer
I 10 til 15% af tilfældene med myasthenia gravis med anti-acetylcholinreceptorantistoffer findes et thymom . Thymomer er tumorer i den forreste mediastinum, ofte godartede, variabelt forbundet med myasthenia gravis.
Anti-titin er en markør for eksistensen af disse thymomer hos patienter under 60 år. Den kirurgiske indikation er vigtig. Det giver mulighed for at specificere, om thymom er godartet (2/3 tilfælde) eller ondartet i henhold til dets invasive karakter eller ej.
I 50-70% af den unge form af myasthenia gravis med anti-acetylcholinreceptorantistof findes thymisk hyperplasi. Denne anomali skal altid betragtes som godartet (hvilket ikke udelukker ablation af thymus).
Mellem 15 og 20% af patienterne med thymom viser også kliniske tegn på myasthenia gravis, og 25% af patienterne har anti-acetyl-cholinreceptor antistoffer (anti-ACh-R antistoffer) uden at vise symptomer. Enhver patient med et thymom med tegn på myasthenia gravis har positive antistoffer, og enhver asymptomatisk mediastinal masse forbundet med anti-ACh-R-antistoffer er et thymom. Mens den statistiske sammenhæng antyder en sammenhæng mellem de to patologier, forbliver den nøjagtige årsag og virkningsmekanisme diskuteret, og flere hypoteser overvejes:
- udvælgelse af defekte T-lymfocytter i thymoma, der er ansvarlig for hypersekretionen af autoantistoffet;
- defekt præsentation af autoantigener til thymiske celler, hvilket fører til ikke-eliminering af T-lymfocytter, der genkender dem;
- tilstedeværelse af specifikke kimcentre inden for det tymiske parenkym, der lettere producerer autoantistoffer;
- hos ældre, tilstedeværelse af uspecifik autoimmunitet.
Ikke alle histologiske typer af thymomer er forbundet på samme måde med myasthenia gravis, nogle er aldrig engang forbundet med det:
- type A: 0%
- type AB: 6,8%
- type B1: 40%
- type B2: 55,6%
- type B3: 10%
- thymisk carcinom: 0%
Autoimmune sygdomme
I 5 til 15% af tilfældene, afhængigt af serien, identificeres mindst en anden autoimmun sygdom i myasthenics. Dette er rapporter om signifikante foreninger, idet der ikke er påvist nogen patofysiologisk forbindelse bortset fra hypotesen om en "dysimmun grund". Disse patologier er autoimmun dyroidhyroidisme, reumatoid arthritis, systemisk lupus erythematosus, Sjögrens syndrom, polymyositis, kronisk inflammatorisk tarmsygdom, Biermers anæmi, autoimmun hæmolytisk anæmi, binyreinsufficiens.
Yderligere tests
Supplerende undersøgelser, ud over dem, der sigter mod at udelukke alternative diagnoser, sigter mod at bekræfte eller udelukke diagnosen og i tilfælde af diagnostisk bekræftelse at lede efter tilknyttede patologier. Disse eksamener er:
Til diagnostiske formål
BiologiKun anti-acetylcholinreceptorantistoffer, og hvis de er fraværende, søges anti-MuSK-antistoffer i klinisk praksis. Deres specificitet er 99%. Deres samlede følsomhed er over 90%, og mindre end 10% af myasthenia gravis defineres derfor som "seronegativ". Mere præcist er følsomheden af anti-receptorantistoffer over for acetylcholin 90% for generaliseret myasthenia gravis og 50% for okulær myasthenia gravis. Forudsat at testen for anti-acetylcholinreceptorantistoffer er negativ, er følsomheden af anti-MuSK-antistoffer 40% for generaliseret myasthenia gravis og marginal for okulær myasthenia gravis.
Deres fremragende specificiteter gør dem til den bedste test til bekræftelse af diagnosen i tilfælde af stærk klinisk mistanke (positiv forudsigelsesværdi på kun 1% for den generelle befolkning).
For nylig er det også i tilfælde af dobbelt negativ myasthenia gravis muligt at analysere LRP4-antistoffer.
Elektrofysiologiske undersøgelserTo elektrofysiologiske undersøgelser er nødvendige:
- en elektromyografisk undersøgelse, der inkluderer:
- et rutinemæssigt elektromyogram, som normalt er normalt. Re-innerveringsaktiviteter kan dog observeres i alvorlige fremskredne tilfælde,
- en elektromyografisk undersøgelse med gentagen supra-maksimal stimulering af en motorisk nerve. Testen betragtes som positiv, når amplitudeforringelsen af motorenhedens potentiale (PUM) er større end 10%. Denne test er ikke-specifik og har en følsomhed på 79% for generaliseret myasthenia gravis og 50% for okulær myasthenia gravis,
- en "enkeltfiber" elektromyografisk undersøgelse med måling af en jitter (variation af latenstiden mellem stimuleringen og motorenheden Potentiale for en given fiber under gentagen stimulering af en motorisk nerve) betyder studiet af mange fibre, der kræver en erfaren eksaminator og specialiseret udstyr. Testen betragtes som positiv, når en stigning i denne jitter observeres over laboratoriestandarderne for den undersøgte muskel. Denne test er ikke-specifik og har en følsomhed på 98% for generaliseret myasthenia gravis og 80% for okulær myasthenia gravis,
- en undersøgelse af nerveledningshastigheder. Denne undersøgelse skal være normal for at elektromyogramafvigelser kan betragtes som relevante.
Den fremragende følsomhed ved elektromyografi gør det til den bedste test at udelukke diagnosen i tilfælde af lav klinisk mistanke (ubestemmelig negativ forudsigelsesværdi, hvis andelen af patienter i undersøgelsesgruppen er større end 1%).
Farmakologisk testProstigmin anvendes enten som en terapeutisk test per os, eller i IM eller især IV foran et klinisk symptom, der ikke talte på det elektrofysiologiske niveau eller i hastetilfælde (ptose, diplopi, tale eller respiratoriske lidelser). Testen er betragtes som positiv, hvis det resulterer i forbedring af symptomer eller elektrofysiologiske tegn. Det sammenlignes undertiden med en placebo-test.
På jagt efter tilknyttede patologier
BiologiMarkørerne for autoimmune patologier, der potentielt er forbundet med myasthenia gravis, måles systematisk. Dette inkluderer markører for inflammation, skjoldbruskkirtelhormoner og anti-pyroperoxidase-antistoffer, anti-nukleare faktorer, anti-nukleare antistoffer, hæmatogram, ionogram, lever- og nyrefunktion, vitamin B12 og folat.
Thorax CT-scannerSystematisk udført for at lede efter et thymom (følsomhed 99%, specificitet 95%) og thymisk hyperplasi (følsomhed 50%, specificitet 95%).
Differential diagnose
Differentialdiagnosen er bred og afhænger af den kliniske præsentation. Vi kan især nævne:
- andre myastheniske syndromer: medfødt myasthenia gravis , Lambert-Eaton myasthenisk syndrom , botulisme , visse slangegift , organophosphor eller magnesiumforgiftning;
- myopatier;
- perifere neuropatier;
- reumatiske patologier
- væske- og elektrolytforstyrrelser;
- endokrinopatier;
- anæmi
- erhvervet, medfødt og traumatisk ptose;
- dekompenseret strabismus;
- funktionelle lidelser, psykiatriske lidelser og kronisk træthedssyndrom.
Prognose
Prognosen er specifik for hver patient. Vi kan dog beskrive nogle generelle egenskaber:
Sværhedsgraden af myasthenia gravis er forbundet med forekomsten af myastheniske kriser med åndedrætsbesvær og livstruende. Denne risiko er højest i starten af sygdommen, hvor 75% af anfaldene opstår i de første to udviklingsår.
Venstre ubehandlet kan forløbet af generaliseret myasthenia gravis være dødelig. Den vitale prognose for former, der forbliver okulære, er ikke involveret.
I meget sjældne tilfælde er der spontane remissioner af sygdommen, hvis varighed er variabel.
10 til 20% vil reagere lidt eller ikke på behandling og vil udvikle variabel motorisk impotens. Faktorerne for dårlig prognose og dårlig terapeutisk respons er: tilstedeværelsen af et thymom, tilstedeværelsen af anti-MuSK-antistoffer og de sero-negative former.
Terapeutisk pleje
Håndteringen af myasthenia gravis kan deles skematisk i symptomatisk behandling, grundlæggende behandling og krisebehandling af sygdommen, behandling af tilknyttede patologier og generelle tiltag. De generelle principper er:
Symptomatiske behandlinger for myasthenia gravis
Anti-cholinesterase-lægemidlerHæmmere af acetylcholinesterase, et enzym, der nedbryder acetylcholin , de udgør den første linje symptomatisk behandling. De mest anvendte er pyridostigmin (Mestinon) og ambenoniumchlorid (Mytelase). Brugen af andre anticholinesterase-lægemidler (såsom neostigmin ) er blevet marginal bortset fra myasthenisk krise. Deres virkning ved seronegativ myasthenia gravis eller med anti-MuSK-antistoffer er ikke påvist.
Langvarig behandling af myasthenia gravis
Kortikosteroider og immunsuppressive midlerKortikosteroider - såsom et progressivt regime af prednison (Cortancyl) eller prednisolon (Solupred) - immunsuppressiva - azathioprin (Imurel), der har vist sig at være effektiv - og mycophenolatmofetil (Cellcept) er den næstvigtigste behandling. Kortikosteroider kan startes i meget lave doser og med tæt klinisk revurdering, hvor forbigående klinisk forværring er almindelig.
Det er nu blevet demonstreret, at tilsætningen af en kombineret behandling med kortikosteroider og immunsuppressiva til generaliseret myasthenia gravis, der er utilstrækkeligt kontrolleret under anticholinesterase-lægemidler, forbedrer den kliniske status efter to år sammenlignet med tilsætningen af kortikosteroider eller immunsuppressiva hver for sig. Nogle eksperter anbefaler, at de anvendes som en førstelinjebehandling for seronegative former eller med anti-MuSK-antistoffer.
Immunsuppressiva er ikke særlig effektive til okulære former.
Marginalt er biologiske behandlinger såsom rituximab (Mabthera), et kimært monoklonalt antistof målrettet mod CD20-molekylet specifikt udtrykt af B-lymfocytter , blevet anvendt med en vis succes i svære former.
Intravenøs plasmaferese og immunglobulinDisse behandlinger har lidt plads bortset fra myastheniske kriser ( se nedenfor ). De anvendes dog undtagelsesvis til de mest alvorlige former, der er resistente over for andre behandlinger eller i tilfælde af hurtig klinisk nedbrydning.
Behandlinger for associerede patologier
Thymektomi og adjuvansbehandlingerOpdagelsen af et thymom er en absolut indikation for thymektomi og kræver langvarig radiologisk opfølgning på jagt efter neoplastiske gentagelser. I tilfælde af ufuldstændig resektion, infiltration af nærliggende væv eller opdagelse af metastaser, bør der tilbydes adjuverende behandling bestående af strålebehandling og / eller kemoterapi.
Den kliniske fordel ved thymektomi i fravær af thymom drøftes stadig. Det anbefales dog i tilfælde af opdagelse af thymisk hyperplasi med tilstedeværelsen af anti-acetylcholinreceptorantistoffer hos patienter under 40 år. En randomiseret undersøgelse fra 2016 fandt også klinisk forbedring af symptomer på myasthenia gravis efter thymektomi, selv i fravær af thymisk hyperplasi.
En forbigående post-kirurgisk symptomatisk forværring er mulig. I de første måneder efter thymektomi kan lægemiddelafbrydelse forsøges, hvis der opstår symptomatisk forbedring eller endda remission.
Andre behandlingerSpecifikke behandlinger er nødvendige i tilfælde af opdagelse af en associeret autoimmun patologi.
Styring af myastheniske kriser
Støttende plejeEnhver hurtig indtræden af åndedrætssvigt, dyspnø med bronkial overbelastning, synkeforstyrrelser eller generaliseret svaghed, der er objektiveret af en læge, berettiger en medicinsk overførsel til en hospitalsinstitution med en intensivafdeling. Ved optagelse foretages en vurdering af luftveje, respiration, cirkulation og neurologi samt en måling af vital kapacitet (CV). En bevidsthedsforstyrrelse, en vital kapacitet mindre end 25% af den teoretiske værdi eller klinisk respirationsudmattelse retfærdiggør intubation og overførsel til en intensivafdeling for mekanisk ventilation og mulig hæmodynamisk stabilisering. Almindelig pleje med regelmæssig vurdering af vital kapacitet er tilstrækkelig i andre tilfælde.
Korrektion af reversible udløsende og promoverende faktorerDisse faktorer skal undersøges og rettes, så snart vitale manøvrer udføres. Disse er hovedsageligt iatrogene årsager (se lægemiddelkontraindikationer), infektioner, dekompensation af andre kroniske patologier hos patienten og temperaturforhøjelser, endogene eller eksogene.
Tilfældet af krampeanfald under graviditeten er specielt, og muligheden for, at de forekommer, skal have været drøftet på forhånd med patienten. Alvorlige anfald, der ikke reagerer på symptomatisk behandling, kræver passende behandling.
Udeluk en overdosis af anticholinesteraserDen vigtigste differentiale diagnose af myasthenisk krise er overdosering med anticholinesterase. Det mistænkes systematisk i tilfælde af en daglig indtagelse af mere end 480 mg pyridostigmin eller muskarine symptomer: bradykardi, bilateral miose, hypersekretion, fækal nedbrydning osv. I tvivlstilfælde vil klinisk forværring efter administration af neostigmin bekræfte diagnosen overdosering. Ledelsen er derefter rent støttende bortset fra administrationen af atropin for dets antimuskarine virkning.
Symptomatiske behandlingerIndgivelse af neostigmin er den første symptomatiske behandling. Hvis der opstår muskarine symptomer, skal atropin tilsættes.
I tilfælde af klinisk forværring under behandlingen bør en overdosis af anticholinesterase-lægemidler overvejes.
I tilfælde af dårlig terapeutisk respons (svigt af detubation) er andenlinjebehandlingen baseret på gentagelse af plasmaferese og / eller intravenøs immunoglobulin-kur.
Hvis dette mislykkes, er kortikosteroider og immunsuppressiva tredjelinjebehandling. Deres indikationer skal dog nøje stilles, idet en forbigående klinisk forværring er almindelig.
Generelle foranstaltninger og para-medicinsk behandling
Medicinsk kontraindikationer Myasthenisk kortDet franske sundhedsministerium har udgivet et pleje- og nødkort til mennesker med myasthenia gravis. Det anbefales stærkt, at patienten bærer dette kort med hans sygdom, hans behandling, hans sidste vaccinationer og listen over lægemidler, der er kontraindiceret i myasthenia gravis. De kan få det fra referencekonsultationerne eller ved at kontakte AFM-téléthon].
LivsstilSom med enhver kronisk patologi kræver myasthenia gravis, at patienten er uddannet om sin sygdom og især til de faktorer, der favoriserer myastheniske kriser. Deltagelse i moderat fysisk træning, tilpasset øjeblikket, bør tilskyndes med hyppig hvile.
Para-medicinsk behandlingI alvorlige former eller modstandsdygtige over for dybdegående behandling kan social støtte og af specialister i fysioterapi, taleterapi, ergoterapi, rehabilitering eller psykologi vise sig nødvendig, ligesom patientens henvisning til en kombination af terapi.
Forbered dig på graviditeter og operationerSamlet set er graviditet og kirurgi en væsentlig årsag til myastheniske anfald, som forekommer i 30% af tilfældene. For at minimere risiciene anbefaler nogle forfattere præ-partum og præ-kirurgisk udførelse af plasmaferese-sessioner eller immunoglobulin-kur samt en evaluering inklusive funktionelle respiratoriske tests. En fødsel skal altid finde sted på en hospitalsinstitution med en intensivafdeling og en nyfødt genoplivningsenhed. Detubation bør aldrig udføres, før patientens evne til at deltage er bekræftet.
Under graviditet skal kortikosteroider og immunsuppressiva anvendes i samråd med en gynækolog.
Noter og referencer
- (i) MB Walker , " Behandling af myasthenia gravis med physostigmin " , Lancet , Vol. 1,1934, s. 1200-1201 ( DOI 10.1016 / S0140-6736 (00) 94294-6 )
- (i) Phillips LH, "The epidemiologi myasthenia gravis " Ann NY Acad Sci. 2003; 998: 407-12
- College of Teachers of Neurology. Myasthenia gravis
- (i) Carr AS, Cardwell CR, PO McCarron, J McConville, "En systematisk gennemgang af befolkningen baseret epidemiologiske undersøgelser i myasthenia gravis" BMC Neurol. 2010; 10:46.
- (en) Bradley et al. Neurologi i klinisk praksis , 5 th udg., Butterworth-Heinemann, 2007
- Goulon-Goeau et al. "Myasthenia gravis and myasthenic syndromes" EMC-Neurologie , 17-172-B-10, 2002, Elsevier, online resume
- B. Eymard “Antistoffer i myasthenia gravis” Neurologisk gennemgang 2009; 165 (2): 125-205 DOI : 10.1016 / j.neurol.2008.11.020
- (i) Zhang B, C Shen, Bealmear B, Ragheb S, Xiong toilet, Lewis RA, Lisak RP, Mei L. " Autoantistoffer til agrin i myasthenia gravis patienternes ' PLoS One , 2014, 3: e91816 DOI : 10,1371 /journal.pone.0091816
- (i) W. Allan. “Patogenese af myasthenia” Opdateret , 2012
- (i) Howard et al. “Kliniske korrelationer af antistoffer, der binder, blokerer eller modulerer humane acetylcholinreceptorer i myasthenia gravis ” Ann NY Acas Sci. 1987
- (en) SJ Bird "Kliniske manifestationer af myasthenia gravis " Opdateret, 2013
- (en) Bershad et al. “ Myasthenia gravis crisis” South Med J. 2008; 101 (1): 63-9. DOI : 10.1097 / SMJ.0b013e31815d4398
- Gaumond "Øjensygdomme i myasthenia gravis" EMC-Neurology , 2005 DOI : 10.1016 / j.emcn.2005.08.002
- (in) Pelak og When "Ocular myasthenia" Up-to-Date , 2013
- (da) Spillane J, E Higham, Kullmann DM. “ Myasthenia gravis ” BMJ 2012; 345: e8497
- (en) Jaretzki A, Barohn RJ, Ernstoff RM et al. , “ Myasthenia gravis: anbefalinger til kliniske forskningsstandarder. Task Force of the Medical Scientific Advisory Board of the Myasthenia Gravis Foundation of America ” , Neurology , bind. 55, nr . 1,2000, s. 16–23 ( PMID 10891897 , læs online )
- (in) Finnis MF Jayawant S, " Juvenile myasthenia gravis: a pædiatrisk perspektiv " , Autoimmune Dis , vol. 2011,2011, s. 404101. ( PMID 22110902 , PMCID PMC3206364 , DOI 10.4061 / 2011/404101 , læs online [html] )
- Antititin-antistof i myasthenia gravis med tidlig og sen begyndelse. Szczudlik P, Szyluk B, Lipowska M, Ryniewicz B, Kubiszewska J, Dutkiewicz M, Gilhus NE, Kostera-Pruszczyk A. Acta Neurol Scand. 2014 (juni). Doi: 10.1111 / ane.12271. [Epub inden udskrivning]
- Thymus, thymoma og myasthenia gravis Fujii Y, Surg Today 2013 maj; 43 (5): 461-6. doi: 10.1007 / s00595-012-0318-2
- Klinisk og funktionel betydning af WHO-klassificering på humane thymiske epiteloplasmer: en undersøgelse af 146 på hinanden følgende tumorer. Okumura M, Miyoshi S, Fujii Y, Takeuchi Y, Shiono H, Inoue M, Fukuhara K, Kadota Y, Tateyama H, Eimoto T, Matsuda H, Am J Surg Pathol 2001 jan; 25 (1): 103-10.
- (en) Mercelis et al. “Diagnostisk nytte af stimuleret enkeltfiberelektromyografi af orbicularis oculi muskel hos patienter med mistanke om okulær myastheni” Muscle Nerve 2011; 43 (2): 168-70.
- (en) Preston et al. Elektromyografi og neuromuskulære lidelser. Klinisk-elektrofysiologiske sammenhænge , 2 th udg., Elsevier, 2005
- (en) Taraldsen Heldan. ”Seropositive Myasthenia Gravis. En landsdækkende epidemiologisk undersøgelse » Neurologi 2009
- (en) Trakas et al. “Udvikling af et meget følsomt diagnostisk assay for muskel-specifik tyrosinkinase (MuSK) autoantistoffer i myasthenia gravis” J Neuroimmunol . 2011; 240-241: 79-86.
- (en) Vincent et al. “Acetylcholinreceptorantistof som en diagnostisk test for myasthenia gravis : resulterer i 153 validerede tilfælde og 2967 diagnostiske essays” J Neurolo Neurosurg Psych. 1985; 48 (12): 1246-52.
- (en) Witoonpanich et al. “Elektrofysiologisk og immunologisk undersøgelse i myasthenia gravis : diagnostisk følsomhed og korrelation” Clin Neurophysiol. 2011; 122 (9): 1873-7.
- (en) Zambelis et al. "Gentagen nervestimulering af ansigts- og hypothenar muskler: relativ følsomhed i forskellige myasthenia gravis-undergrupper" Eur Neurol. 2011; 65 (4): 203-7.
- (en) Lindstrom et al. "Antistof mod acetylcholinreceptor i myasthenia gravis. Prevalens, kliniske korrelater og diagnostisk værdi » Neurologi 1976.
- (in) Bird "Diagnose in myasthenia gravis " Opdateret , 2013
- Autoantistoffer mod lipoprotein-relateret protein 4 hos patienter med dobbelt-seronegativ myasthenia gravis. Zhang B1, Tzartos JS, Belimezi M, Ragheb S, Bealmear B, Lewis RA, Xiong WC, Lisak RP, Tzartos SJ, Mei L. Arch Neurol. 2012 apr; 69 (4): 445-51. doi: 10.1001 / archneurol.2011.2393. Epub 2011 12. december
- (in) Bird "Differential Diognosis of myasthenia gravis" Opdateret , 2012
- (i) Bird "Behandling af myasteni" Up-to-Date , 2013
- (i) Howard et al. Myasthenia gravis. En manual til sundhedsudbyderen , Myasthenia Gravis Foundation of America, 2008
- (en) Gold R, Schneider-Gold C, " Nuværende og fremtidige standarder til behandling af myasthenia gravis " , Neurotherapeutics , vol. 5, nr . 4,2008, s. 535-41. ( PMID 19019304 , PMCID PMC4514693 , DOI 10.1016 / j.nurt.2008.08.011 , læs online [html] )
- (en) Mandawat et al. “Sammenlignende analyse af terapeutisk mulighed anvendt til myasthenia gravis ” Ann Neurol. 2010; 68 (6): 797-805.
- " ambenonium chloride " på www.vidal.fr (tilgængelige på 1 st august 2015 )
- (en) Collongues N, O Casez, Lacour A. et al. “Rituximab i ildfast og ikke-ildfast myastheni: en retrospektiv multicenterundersøgelse ” Muscle Nerve 2012; 46: 687-91
- (i) Gil I. Wolfe, Henry J. Kaminski, Inmaculada B. Aban et al., " Randomized Trial of Myasthenia Gravis in Thymectomy " , New England Journal of Medicine (NEJM \ / MMS), bind. 375, nr . 6,11. august 2016, s. 511-522 ( ISSN 0028-4793 , DOI 10.1056 / nejmoa1602489 , læs online ).
- (i) Goldenberg, WD og Shah, AK , " Myasthenia Gravis " , eMedicine (adgang til 5. maj 2012 )
- (fr) Denne artikel er helt eller delvist taget fra Wikipedia-artiklen på engelsk med titlen " Myasthenia gravis " ( se listen over forfattere ) .