Duchenne muskeldystrofi
Duchenne muskeldystrofi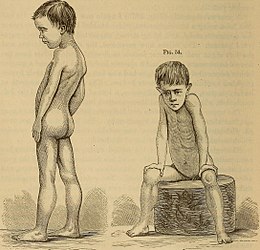 Illustration (1881) af et barn med Duchennes dystrofi
Illustration (1881) af et barn med Duchennes dystrofi
| Specialitet | Neurologi |
|---|
| OMIM | 310200 |
|---|---|
| Sygdomme DB | 3985 |
| MedlinePlus | 000705 |
| MeSH | D020388 |
| Symptomer | Muskelsvaghed ( in ) , kardiomyopati og muskelatrofi |
| Årsager | Mutation |
| Behandling | Kortikosteroid , kirurgi , kunstig ventilation , fysioterapi , genterapi og ergoterapi |
| Medicin | Eteplirsen , Déflazacort ( en ) og ataluren |
| UK patient | Duchenne-muskeldystrofi |
| Duchenne muskeldystrofi | |
| MIM-reference | 310200 |
|---|---|
| Smitte | X-recessiv |
| Kromosom | X p21.2 |
| Ubehageligt | DMD |
| Forældres aftryk | Ingen |
| Mutation | Sletning , duplikering |
| De novo mutation | 23% |
| Forventning | Ingen |
| Indvirkning | 1 ud af 3.500 fødsler af drenge - 1 ud af 100.000 fødsler af piger |
| Gennemtrængende | komplet |
| Genetisk forbundet sygdom | Nogen |
| Prænatal diagnose | Muligt |
| Liste over genetiske sygdomme med identificeret gen | |
Den Duchenne muskeldystrofi ( DMD ) er den mest alvorlige hændelser i forbindelse med et underskud på dystrofin , der får musklerne til at modstå den indsats: uden det, de muskelfibre degenerere. Det er derfor en progressiv sygdom.
Sygdommen kan påvirke nogen muskler, herunder hjertet muskler . Denne kardiomyopati er hovedårsagen til dødeligheden af denne sygdom. Når membranen er påvirket af sygdommen, forårsager den åndedrætsstop, som kan være en anden dødsårsag fra denne sygdom.
Det skylder sit navn Guillaume Duchenne , der beskrev det i 1858.
De sygdomme , der er forbundet med abnormiteter i dystrofin kaldes dystrophinopathies .
Sygdomme inkluderet
- Beckers myopati
- Kardiomyopati relateret til en abnormitet af dystrophin.
Andre navne på sygdommen
- Duchenne og Becker muskeldystrofi
- Duchenne og Becker muskeldystrofi
- Dystrofinopati
Etiologi
Sygdommen er forårsaget af en mutation i DMD- genet placeret på locus 21.2 i X- kromosomet, der koder for et protein kaldet dystrophin .
De genetiske modifikationer, der er ansvarlige for abnormiteterne i genets funktion, er sletninger (ansvarlig for 65% af Duchenne muskeldystrofi og 85% af Becker muskeldystrofi) og duplikationer (ansvarlig for 6% af Duchenne muskeldystrofi). Resten af de genetiske omlejringer inkluderer mikrodeletioner, substitutioner, der involverer et enkelt nukleotid , insertioner og mutationer under splejsning ( splejsmutationer ).
Disse genmutationer fører enten til et fuldstændigt underskud i dystrofinproduktion (Duchenne myopati) eller til en ændring af sidstnævnte bliver mindre funktionel (Becker myopati).
Imidlertid bevarer næsten 50% af Duchenne-myopatier sjældne muskelfibre, der syntetiserer dystrofin.
Indvirkning
Forekomsten estimeres til at være 1 ud af 4.000 til 1 ud af 3.500 fødsler af drenge. Kun drenge er berørt (med få sjældne undtagelser), og kvinder er sendere. De kan undtagelsesvis påvirkes (kræver at være homozygote på genet).
Beskrivelse
Det manifesteres hovedsageligt af symmetrisk muskelsvaghed, der påvirker mere proximalt end distale muskler på grund af degeneration af muskelvæv, selv på grund af en mutation i dystrofingenet.
- kropsskala: muskelsvaghed
Diagnostisk
Diagnosen stilles ofte efter en alder af 2 eller 3 år, det vil sige efter udseendet af de første kliniske tegn. Vi kan opnå:
- en muskelbiopsi
- en blodprøve (CPK-niveau)
- et elektrokardiogram.
Et af de første advarselsskilte er Gowers 'tegn : det lille barn har svært ved at stå op og er nødt til at drive sig frem ved hjælp af sine arme og jorden eller ved at læne sig på sin egen bagagerum. Dette kliniske tegn skyldes insufficiens i bækkenbunden og glutealmusklerne, såsom gluteus maximus .
Klinisk
Ofte er der en familiehistorie af X-bundet recessiv sygdom. Tilstedeværelsen af muskel fascikulationer eller forstyrrelse i følsomhed udelukker diagnosen af myopati.
Duchenne muskeldystrofi- Symptomebegyndelse inden 5 år
- Cirka 3 år: ganglidelser
- Vanskeligheder med at løbe, hoppe, gå
- Vanskeligheder med at gå op ad trapper (hjælp til øvre lemmer)
- Gowers tegn
- Måde at gå: recurvatum, ryg kastet tilbage, udvidelse af støttepolygonen (spred fødderne)
- Vanskeligheder med at stå på 1 fod
- 5-6 år: bevægelsesproblemet forværres
- Omkring 10 år gammel:
- Tab af gang, så barnet bruger en kørestol
- Deformiteter vises: hestehest, albuebøjning, knæ, hofter, skoliose
- Nedsat membran
- Kardio-myopati
- Udseende af symmetrisk muskelsvaghed, der påvirker mere proximalt end distale muskler
- Tilsyneladende forstørrelse af kalvene er ofte til stede i forbindelse med en stigning i den ikke-muskulære del af musklerne
- I sidste ende er barnet komplet quadriplegic
- Udseende af symmetrisk muskelsvaghed, der påvirker mere proximalt end distale muskler, men bevarelse af muskelaktivitet i musklerne, der er ansvarlige for at bøje nakken
- Tilsyneladende hypertrofi af kalvene ofte til stede
- Nogle gange er simpel svaghed i quadriceps-musklen i låret eller tilstedeværelsen af kramper under muskelaktivitet
- Tab af gang (hvis væsentlig svækkelse) ikke før 16 år
En kardiomyopati kan forekomme mellem 20 og 40 år og udvikler sig hurtigt til hjertesvigt . Denne DMD-afhængige kardiomyopati har ingen speciel funktion.
Økologisk
Værdien af blodkreatinkinase eller CPK øges konstant i myopatier relateret til en abnormitet af dystrofin. Afhængigt af patologien kan hastigheden variere:
- 100% af mennesker med Duchenne muskeldystrofi har i det mindste en hastighed, der er 10 gange større end normalt
- 100% af mennesker med Beckers muskeldystrofi har i det mindste en hastighed, der er 5 gange større end normalt
- De fleste kardiomyopatipatienter har en stigning i de samlede CK'er.
Elektromyografi
Den elektromyografi er ikke nyttigt til diagnosticering. Det gør det muligt at skelne mellem:
- primær muskelskade;
- sekundær skade ved læsion af motorisk nerve.
Muskelbiopsi
De biopsi viser læsioner ikke specifikke for sygdommen. Det er ikke nyttigt ved diagnosen Becker's sygdom, hvorimod anti-dystrophin-farvning viser fraværet af proteinet i sundt væv til Duchennes sygdom.
Genetisk
Det er en recessiv mutation på X-kromosomet, hvorfor sygdommen primært rammer drenge. Kvinder er bærere, men kan i sjældne tilfælde også manifestere sygdommen (se mønstre med X-bundet recessiv arv ).
Udvikling
Det forværres gradvist: næsten alle de berørte drenge er i en kørestol i en alder af 12 år. Den forventede levealder på grund af forværrede luftvejssygdomme var i gennemsnit ca. 25 år i 2002. Den er næsten fordoblet på 30 år takket være forebyggelse (tværfaglig pleje: ortopædisk, respiratorisk, ernæringsmæssig, hjerte osv. ), Information og stigningen i assisteret ventilation og trakeotomi : det gik fra 25 år i 1981 til 41 år i 2011 ifølge en undersøgelse foretaget i Frankrig. Dødsårsagerne har også ændret sig med en stigning i hjertedødsfald fra 8% til 44%. I dag er ca. 30% af dødsårsagerne hjerte, med et kraftigt fald i dødeligheden på grund af respirationssvigt takket være brugen af invasiv ventilation og respiratorisk fysioterapi. I øjeblikket er infektioner, lungeblødning og nyresvigt også dødsårsager.
Hjerteinddragelse er mulig med fibrose i hjertemusklen og detekteres ved ekkokardiografi i omkring halvdelen af avancerede tilfælde. Prognosen afhænger hovedsageligt af nedsat systolisk funktion.
Differential diagnose
Duchennes muskeldystrofi skal skelnes fra svær Becker muskeldystrofi og bælte muskeldystrofi .
Behandling
Behandling med kortikosteroider forbedrer muskelformen på mellemlang sigt (to år). Det reducerer risikoen for, at hjerteskader opstår såvel som den samlede dødelighed.
Luftvejssvækkelse kan behandles ved at sætte på mekanisk ventilation , hvilket muliggør en forlængelse af forventet levetid på flere år. Det kan hjælpes ved kirurgi for at korrigere abnormiteter i rygsøjlestatikken.
Systematisk anvendelse af perindopril , en konverterende enzymhæmmer , fra barndommen, før en hvilken som helst hjerteinddragelse, nedsætter den samlede dødelighed.
Tværfaglig pleje
En tidlig, koordineret og langsigtet tværfaglig styring af patienten muliggør en forøgelse af hans forventede levetid. De berørte områder er:
- behandling af neuromuskulære lidelser: af en neurolog eller en fysiater for at fastlægge diagnosen og overvåge sygdommen
- rehabilitering hos en fysioterapeut
- endokrinologi, især i puberteten
- ernæring
- pulmonologi for at opretholde lungefunktion
- kardiologi til forebyggelse og påvisning af mulig kardiomyopati
- ortopædi: screening for skoliose og forebyggelse af ledstivhed
- knoglesundhed af en specialist i neuromuskulære sygdomme for at overvåge knogles skrøbelighed
- psykosocial hjælp: socialrådgiver om at henvise patienten, men også familien til psykologisk hjælp, hvis det er nødvendigt
- forvaltning af primærpleje og nødsituationer: hjælper med at opretholde et godt helbred på lang sigt
- uddannelse og støtte i overgangsperioder: hjælp til uddannelse, uafhængighed, adgang til boliger eller udvikling af sociale bånd.
Forskningsstier
I genterapi er eksperimenter startet på mus, hvor forskere håber, at ved at indføre genet, der koder dystrophin i en persons krop, kan dette protein oprettes normalt af det berørte individ. Imidlertid kunne den således syntetiserede dystrofin muligvis forårsage en immunologisk reaktion fra kroppen og dermed gøre fordelen meget mindre klar.
En anden lovende rute er exon-springningsteknikken (kodende del af DNA). Den består i at splejse (eller "springe over") den muterede exon ved at tilføje tråde af antisense-oligonukleotider i cellen, som maskerer splejsningsstederne i eksonerne omkring den muterede del. Resultatet er en dystrofin krympet af nogle få aminosyrer, men alligevel funktionel.
I 2014 annoncerede franske forskere succeserne med genterapi baseret på sygdommens hundemodel.
Fire år senere, i midten af 2018, tillod en genterapi-behandling testet på tre børn i USA dem at genvinde mindst 38% af det normale niveau af dystrofin ifølge Forbes, så en af dem hurtigt kunne klatre op ad en trappe, når han har tidligere været nødt til at klatre et trin ad gangen (ifølge en video præsenteret af en investor ved Sarepta Therapeutics i Cambridge, Massachusetts). De to andre gennemgår lignende behandling, der tilbydes af to andre virksomheder (Solid Biosciences; Pfizer), og en af disse to patienter klarer sig godt ifølge Derek Lowe på bloggen In the Pipeline, udgivet af AAAS .
Den 17. marts 2021 modtager en lille dreng for første gang en første dosis GNT 0004 genterapi på Trousseau hospitalet i Paris.
Transmissionstilstand
Arvemåden siges at være recessiv og bundet til DMD-genet i X-kromosomet . Dette betyder, at sygdommen starter hos personer, der ikke har en funktionel allel til dette gen. Da mænd kun har et X-kromosom, har de kun en allel: alle mænd, der bærer en skadelig mutation af dette gen, påvirkes derfor. Kvinder har to X-kromosomer: kvinder, der bærer en mutation, påvirkes ikke, fordi de har en anden ikke-muteret allel. I meget sjældne tilfælde udvikler nogle kvinder dog sygdommen ud over at være bærere af den. Sygdommen udvikler sig ikke hos kvinder på samme måde som hos mænd.
Genetisk rådgivning
Risikovurdering
Da de mandlige bærere alle er berørt, er det umuligt for en muteret allel at blive overført fra en uskadet far til hans efterkommere. På den anden side har kvindelige bærere en 50% risiko for at overføre den muterede allel til deres afkom: Sønner af en bærer kvinde har en 50% risiko for at blive ramt, og piger har en 50% risiko for at være bærere. Bemærk, at neomutationshastigheden er høj (estimeret mellem 23% og 33%). Dette betyder, at i 2/3 af tilfældene er mødre til berørte børn bærere, og i 1/3 af tilfældene arves ikke mutationen, men opstod under produktionen af en forældrenes gamet. En mutation kan ikke overføres fra et ikke-skadet menneske, hvilket skal tages i betragtning ved vurderingen af risikoen for pårørende. For eksempel har moderens tante til et berørt barn en risiko for at være bærer, der anslås til 22%, mens farens tante har en risiko meget tæt på 0%: den for den generelle befolkning.
Noter og referencer
- (in) Barbujani G, Russo A, GA Danieli, Spiegler AW, Borkowska J PETRUSEWICZ H, " Segregationsanalyse af 1885 DMD-familier: signifikant afvigelse fra den forventede andel af sporadiske tilfælde " , Hum Genet. , Vol. 84, nr . 6,1990, s. 522-6. ( PMID 2338336 )
- (da) Emery AE., “ Befolkningsfrekvenser af nedarvede neuromuskulære sygdomme - en verdensundersøgelse ” , Neuromuscul Disord. , Vol. 1, n o 1,1991, s. 19-29 ( PMID 1822774 )
- (en) Norman A, Harper P, “ En undersøgelse af manifesterende bærere af Duchenne og Becker muskeldystrofi i Wales ” , Clin Genet. , Vol. 36, nr . 1,1989, s. 31-7 ( PMID 2766561 )
- Duchenne GB, De ataxie locomotrice progressive , Archives générale de Médecine, Paris, 1858, 5 ser., 12: 641-652; 13: 36-62, 158-1881, 417-451
- (i) Aartsma-Rus A, Van Deutekom AD Fokkema IF, Van Ommen GJ, Den Dunnen JT, "Poster i Leiden Duchenne muskelsvind mutation database: et overblik over mutation type og paradoksale bokse, der bekræftede læsning-frame regel" Muscle Nerve 2006; 34: 135-144
- (en) Aartsma-Rus A, AA Janson, Kaman WE. et al. "Antisense-induceret multiexon-springning over for Duchenne muskeldystrofi giver mere mening" Am J Hum Genet. 2004; 74: 83-92
- (in) Moser H, "Duchenne muskeldystrofi: patogenetiske aspekter og genetisk forebyggelse" Hum Genet. 1984; 66: 17-40
- (in) Gowers WR, " Klinisk aflæsning er pseudo-hypertrofisk muskellammelse " , Lancet , nr . 21879, s. 1–2, 37–39, 73–75, 113–116
- (in) Chang RF, Mubarak SJ, " pathomechanics of Gowers 'tegn: en videoanalyse af et spektrum af Gowers' manøvrer " , Clin Orthop Relat Res. , Vol. 470, nr . 7,2012, s. 1987-91. ( PMID 22203329 , PMCID PMC3369091 , DOI 10.1007 / s11999-011-2210-6 )
- Kamdar F, Garry DJ, Dystrophin-deficient cardiomyopathy , JACC, 2016; 67: 2533-2546
- (in) Eagle M, SV Baldwin, Chandler C. et al. "Overlevelse i Duchennes muskeldystrofi: forbedringer i forventet levealder siden 1967 og virkningen af hjemmeventuel ventilation" Neuromuscul Disord. 2002; 12: 926-929
- http://www.afm-france.org/ewb_pages/f/fiche_maladie_Dystrophie_musulaire_de_Duchenne.php
- (da) “ Udvikling af forventet levealder for patienter med Duchenne muskeldystrofi ved AFM Yolaine de Kepper-centret mellem 1981 og 2011 ” , Annals of Physical and Rehabilitation Medicine , bind. 56, nr . 6,1 st september 2013, s. 443–454 ( ISSN 1877-0657 , DOI 10.1016 / j.rehab.2013.06.002 , læst online , adgang til 24. marts 2021 )
- Carol A. Wittlieb-Weber , Kenneth R. Knecht , Chet R. Villa og Chentel Cunningham , ” Risikofaktorer for hjerte- og ikke-kardiale dødsårsager hos mænd med Duchenne muskeldystrofi ”, pædiatrisk kardiologi , bind. 41, nr . 4,april 2020, s. 764–771 ( ISSN 1432-1971 , PMID 32016582 , PMCID 7328368 , DOI 10.1007 / s00246-020-02309-y , læst online , adgang til 24. marts 2021 )
- Tsuyoshi Matsumura , Toshio Saito , Harutoshi Fujimura og Susumu Shinno , " [En langsigtet dødsårsagsanalyse af patienter med Duchenne muskeldystrofi] ", Rinsho Shinkeigaku = Clinical Neurology , vol. 51, nr . 10,oktober 2011, s. 743–750 ( ISSN 0009-918X , PMID 22019865 , DOI 10.5692 / clinicalneurol.51.743 , læs online , adgang til 24. marts 2021 )
- (en) Frankel KA, Rosser RJ. ”Hjertets patologi i progressiv muskeldystrofi: epimyokardiefibrose” Hum Pathol. 1976; 7: 375-386
- (i) Kermadec JM, Becane HM Chenard A Tertrain F, Weiss Y. "Udbredelsen af venstre ventrikel systolisk dysfunktion i Duchenne muskeldystrofi: en ekkokardiografisk undersøgelse" Am Heart J. 1994; 127: 618-623
- (en) Corrado G, Lissoni A, S Beretta et al. "Prognostisk værdi af elektrokardiogrammer, ventrikulære sene potentialer, ventrikulære arytmier og systolisk dysfunktion i venstre ventrikel hos patienter med Duchenne muskeldystrofi" Am J Cardiol. 2002; 89: 838-841
- INSERM US14 - ALLE RETTIGHEDER FORBEHOLDT , " Orphanet: Duchenne muskeldystrofi " , på www.orpha.net (adgang til 24. marts 2021 )
- (i) Manzur AY, Kuntzer T, M Pike, A Swan, "Glucocorticoidbaserede kortikosteroider for Duchenne muskelsvind" Cochrane Database Syst Rev. 2008 DOI : 10.1002 / 14651858.CD003725.pub3
- (in) Schram G Fournier A, Leduc H. et al. ”Dødelighed af alle årsager og kardiovaskulære resultater med profylaktisk steroidbehandling i Duchennes muskeldystrofi” J Am Coll Cardiol. 2013; 61: 948-954
- Passamano L, TAGLIA A, Palladino A et al. Forbedring af overlevelse i Duchennes muskeldystrofi: retrospektiv analyse af 835 patienter , Acta Myol, 2012; 31: 121-125
- Eagle M, Bourke J, Bullock R et al. Håndtering af Duchennes muskeldystrofi - den additive effekt af rygmarvskirurgi og natlig ventilation i hjemmet til forbedring af overlevelse , Neuromuscul Disord, 2007; 17: 470-475
- (en) Duboc D, Meune C, Peter B. et al. "Perindopril forebyggende behandling af dødelighed i Duchenne muskeldystrofi: 10 års opfølgning" Am Heart J. 2007; 154: 596-602
- (i) Maria Gieron-Korthals og Raymond Fernandez , " nye udviklinger i diagnose, behandling og forvaltning af Duchennes muskeldystrofi " , Advances in Pediatrics , bind 67, vol. 67,1 st august 2020, s. 183–196 ( ISSN 0065-3101 , DOI 10.1016 / j.yapd.2020.03.002 , læst online , adgang til 24. marts 2021 )
- (i) David J Birnkrant , Katharine Bushby , Carla M Bann og Susan D Apkon , " Diagnose og styring af Duchennes muskeldystrofi, del 1: diagnose, og neuromuskulære, rehabilitering, endokrine og gastrointestinale og ernæringsstyring " , The Lancet Neurology , vol. 17, nr . 3,1 st marts 2018, s. 251–267 ( ISSN 1474-4422 , DOI 10.1016 / S1474-4422 (18) 30024-3 , læst online , adgang til 24. marts 2021 )
- (i) David J Birnkrant , Katharine Bushby , Carla M Bann og Benjamin A Alman , " Diagnose og styring af Duchennes muskeldystrofi, del 2: respiratorisk, hjerte-, knogle sundhed, ortopædi og forvaltning " , The Lancet Neurology , vol. 17, nr . 4,1 st april 2018, s. 347-361 ( ISSN 1474-4422 , DOI 10.1016 / S1474-4422 (18) 30025-5 , læst online , adgang til 24. marts 2021 )
- (i) David J Birnkrant , Katharine Bushby , Carla M Bann og Susan D Apkon , " Diagnose og styring af Duchennes muskeldystrofi, del 3: primær pleje, beredskab, psykosocial omsorg og overgange for pleje på tværs af levetid " , The Lancet Neurology , bind. 17, nr . 5,1 st maj 2018, s. 445–455 ( ISSN 1474-4422 , DOI 10.1016 / S1474-4422 (18) 30026-7 , læst online , adgang til 24. marts 2021 )
- (in) Mendell JR, Campbell K-Rodino Klapac L. et al. “Dystrofinimmunitet i Duchennes muskeldystrofi” N Eng J Med. 2010; 363: 1429-1437
- (en) van Deutekom JC, Janson AA, Ginjaar IB. et al. "Lokal dystrofingendannelse med antisense-oligonukleotid PRO051" N Engl J Med. 2007; 357: 2677-2686
- (en) Mendell J. et al. “Eteplirsen til behandling af duchenne muskeldystrofi” Ann Neurol. 2013.
- (en) Guiner C Montus M, L Servais, Cherel Y, Voit T. et al. , " Forbenbehandling i en stor kohorte af dystrofiske hunde understøtter levering af en rekombinant AAV til Exon-springning hos Duchenne-patienter " , Mol Ther , vol. 11, nr . 22,2014, s. 1923-35. ( PMID 25200009 , DOI 10.1038 / mt.2014.151 , resumé )
- Jocelyn Kaiser (2018) Lovende tidlige resultater for genterapi for Duchenne muskeldystrofi , Science news 19. juni 2018
- AFP , " Begyndelsen af test af et lægemiddel mod Duchenne muskeldystrofi, symbol på Telethon " , på Orange News ,20. april 2021(adgang 20. april 2021 )
- http://omim.org/entry/310200
Tillæg
Bibliografi
- Historie om myopatier , Éditions Payot, Paris, 1998 af François Delaporte og Patrice Pinell
- Genetik: teoretiske og praktiske aspekter , P r D. Schorderet, IRO_EPFL, uddelingsudgave 07, s. 2c-5
eksterne links
- Orphanet
- (en) Online Mendelian Arv i mennesket, OMIM (TM). Johns Hopkins University, Baltimore, MD. MIM-nummer: 310200 [1]
- (en) Online Mendelian Arv i mennesket, OMIM (TM). Johns Hopkins University, Baltimore, MD. MIM-nummer: 300377 [2]
- (en) Online Mendelian Arv i mennesket, OMIM (TM). Johns Hopkins University, Baltimore, MD. MIM-nummer: 302045 [3]
- (en) Online Mendelian Arv i mennesket, OMIM (TM). Johns Hopkins University, Baltimore, MD. MIM-nummer: 300376 [4]
- (da) GeneTests: Medical Genetics Information Resource (database online). Ophavsret, University of Washington, Seattle. 1993-2005 [5]