Helium
| Helium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Superfluid flydende helium ( T ≤ 2 K ). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Position i det periodiske system | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbol | Hej | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Efternavn | Helium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atom nummer | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | 1 e periode | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | Bloker s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementfamilie | Ædelgas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronisk konfiguration | 1 s 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroner efter energiniveau | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementets atomare egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 4,002602 ± 0,000002 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomisk radius (calc) | 128 pm ( 31 pm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalent radius | 28 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals-radius | 140 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationstilstand | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxid | ukendt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ioniseringsenergier | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re : 24.587387 eV | 2 e : 54,417760 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mest stabile isotoper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enkle kropsfysiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Almindelig tilstand | Gas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
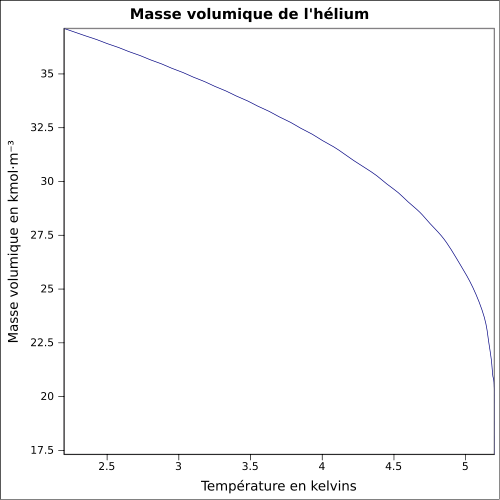
| Volumenmasse |
0,1786 g · L -1 ( 0 ° C , 1 atm ); 0,125 kg · L -1 (flydende, -268,93 ° C ) ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystal system | Kompakt sekskantet | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Farve | Farveløs | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fusionspunkt | 0,95 K ( 26 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kogepunkt | −268,93 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fusionsenergi | 5,23 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fordampningsenergi | 0,08 kJ · mol -1 ( 1 atm , -268,93 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk temperatur | −267,96 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk pres | 2.26 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molært volumen | 22,414 × 10 -3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Damptryk |
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lydens hastighed | 972 m · s -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massiv varme | Cp 20,79 J · mol -1 · K -1
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varmeledningsevne | 152,0 mW · m- 1 · K -1 ( 26,85 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forskellige | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.028.334 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EF | 231-168-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Advarsel H280 og P410 + P403 H280 : Indeholder gas under tryk; kan eksplodere ved opvarmning P410 + P403 : Beskyttes mod sollys. Opbevares i et godt ventileret område. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 PÅ, A : Kritisk komprimeret gas- temperatur = −267,9 ° C Oplysning ved 1,0% i henhold til klassificeringskriterier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1046 : KOMPRIMERET HELIUM Klasse: 2.2 Mærkat: 2.2 : Ikke-brandfarlige, ikke-giftigegasser(svarer til grupper udpeget af A eller stort O);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheder af SI & STP, medmindre andet er angivet. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den helium er det grundstof af atomnummer 2 af Han symbol. Det er en ædelgas (eller ædelgas), praktisk taget indifferent , den første af de ædelgas familien i periodiske system af elementerne . Dens kogepunkt er det laveste blandt kendte kroppe, og det eksisterer kun i fast form, når det udsættes for et tryk på mere end 25 atmosfærer .
Helium har to stabile isotoper : helium 4 ( 4 He), den mest rigelige, og helium 3 ( 3 He). Disse to isotoper adskiller sig, i modsætning til de fleste kemiske grundstoffer, i deres egenskaber, fordi forholdet mellem deres atommasser er vigtigt. På den anden side giver kvanteeffekter, følsomme ved lav energi, dem meget forskellige egenskaber. Denne artikel handler hovedsageligt om helium 4 ( 4 He). Helium 3- artiklen samler de specifikke egenskaber for 3 He- isotopen .
Ordet helium blev konstrueret af det græske Helios ( Ἥλιος / Hếlios , " Solen " ), idet dette element blev observeret for første gang i solspektret på18. august 1868, under en total solformørkelse , af astronom Jules Janssen .
Helium er efter brint det mest rigelige element i universet . Det meste af dette helium blev produceret under den primære nukleosyntese, men andre processer producerer det, især α-radioaktivitet ( se underafsnit Naturlig overflod ). På jorden , ifølge et skøn fra Bureau of Land Management i De Forenede Stater i 2006, er heliumressourcer i alt 52 milliarder kubikmeter.
Helium har forskellige anvendelser i stærk vækst, mens industriproduktionen er faldet af økonomiske årsager: dens knaphed bliver bekymrende. I 2016 er heliummarkedet imidlertid fra et økonomisk synspunkt roligt, og det er for nylig gået fra mangel til overskud.
Otte isotoper af helium er kendt. Den helium 3 (to protoner og en neutron) og helium-4 (to protoner og to neutroner) er stabile, andre er ekstremt ustabil, så godt som sikkert kun eksisterer under deres uddannelse. I jordens atmosfære er der kun et helium-3- atom for hver million helium-4- atomer . I modsætning til de fleste elementer varierer den isotopiske overflod af helium meget afhængigt af dens oprindelse på grund af forskellige dannelsesprocesser. Den mest rigelige isotop, helium 4 , produceres på Jorden af α-radioaktiviteten af tunge grundstoffer: de α-partikler, der produceres der, er fuldt ioniserede helium 4- kerner . Den helium-4 er en kerne til den usædvanlige stabilitet, fordi dets nukleoner er anbragt i hele lag .
Overalt i universet blev det meste af det tilstedeværende helium dannet (i enorme mængder, ca. 25% af alt stof) under den primære nukleosyntese . Næsten hele resten af helium produceret i universet er (eller har været) under stjernernes nukleosyntese.
Den helium-3 er til stede på Jorden kun i spormængder; de fleste stammer fra dannelsen af Jorden, skønt lidt stadig falder på den, fanget i interstellært støv . Spor produceres også stadig af tritiums β-radioaktivitet . Klipper i jordskorpen har isotopiske forhold, der varierer op til en faktor 10, og disse forhold kan bruges til at bestemme oprindelsen af klipper og sammensætningen af jordens kappe . Den helium-3 er mere rigelige i stjernerne, men det er produceret under nuklear fusion , stjerner ikke frigiver meget lidt (ligesom deuterium og lithium , eller bor ), da det n 'vises kun i en mellemliggende kæde fører til helium 4 : det "forbruges", da det produceres i stjernerne. Som et resultat er isotopforholdet i det interstellære medium ca. 100 gange højere end på Jorden. Ekstraplanetære materialer, såsom regolit fra månen eller asteroider, har spor af helium 3 fra solvinden . Månens overflade indeholder en koncentration i størrelsesordenen 10-8 . Et antal forfattere, der startede med Gerald Kulcinski i 1986, har foreslået at udforske månen, udvinde helium-3 fra regolit og bruge den til at generere energi gennem kernefusion.
Den helium-4 kan afkøles til ca. 1 K ved inddampning. Den helium-3 , som har et lavere kogepunkt, kan afkøles til 0,2 K ved den samme fremgangsmåde. Blandinger af lige dele af helium 3 og 4 adskilles, under 0,8 K , fordi de ikke længere er blandbare på grund af deres forskelle ( helium 4- atomet er et boson, mens heliumatomet 3 er en fermion , de følger to forskellige kvantestatistikker) . De udvanding køleskabe bruge denne egenskab til at opnå nogle millikelvins.
Andre isotoper af helium kan produceres ved nukleare reaktioner , som er ustabile og hurtigt henfalder til andre kerner. Isotopen med den korteste halveringstid er helium 2 (2 protoner uden nogen neutroner: diprotonet , der henfalder til to protoner i 3 × 10 −27 s ). Den helium 5 og helium 7 henfald ved emission af en neutron med en halveringstid på 7,6 × 10 -23 s og 2,9 × 10 -21 s hhv. Den helium 6 og helium 8 sønderdeles ved β radioaktivitet med en halveringstid på 0,8 s og 0,119 s henholdsvis. De Isotopes 6 og 8 har en løs struktur, hvor neutroner kredser langt fra hjertet, kaldes det nukleare halogen .
Den eneste heliumlegeme
Helium er en farveløs, lugtfri og giftfri gas. Det er praktisk taget kemisk inert , monoatomisk under alle omstændigheder. I en lang række temperaturer og tryk opfører den sig eksperimentelt som en ideel gas , hvilket gør det til et privilegeret stof til eksperimentering med fysisk-kemiske teorier. De to stabile isotoper af helium er de eneste kemiske forbindelser, der ikke har et tredobbelt punkt .
Gas
Den termiske ledningsevne for heliumgas er større end for alle gasser undtagen brint, og dens specifikke varme er usædvanlig høj. Dens Joule-Thomson-koefficient er negativ ved stuetemperatur, hvilket betyder, at den i modsætning til de fleste gasser opvarmes, når den kan slappe frit af. Joule-Thomson inversionstemperaturen er ca. 40 K eller -233,15 ° C ved et tryk på 1 atm . Når det er afkølet under denne temperatur, kan helium flydes ved afkøling på grund af dets ekspansion.
Helium er også den mindst vandopløselige gas af alle kendte gasser. På grund af den lille størrelse af dets atomer er dens diffusionshastighed gennem faste stoffer tre gange den for luft og omkring 65% af brint.
Heliums brydningsindeks er tættere på enhed end nogen anden gas. Lydens hastighed i helium er større end i nogen anden gas undtagen brint.
I modsætning til plasma er gas en fremragende elektrisk isolator.
Plasma
Mest udenjordisk helium findes i plasmatilstand , hvis egenskaber adskiller sig markant fra atomare heliums egenskaber. I plasmaet er heliumets elektroner ikke bundet til kernen, hvilket fører til en meget høj elektrisk ledningsevne, selv når ioniseringen er delvis. Ladede partikler er meget følsomme over for elektriske og magnetiske felter. For eksempel interagerer ioniseret helium og brint i solvinden med jordens magnetosfære i solvinden , hvilket giver anledning til fænomenerne Birkeland-strømme og den polære aurora .
Ligesom andre ædelgasser har helium metastabile energiniveauer, der gør det muligt at forblive ophidset i en elektrisk afladning, hvis spænding er under dets ioniseringspotentiale. Dette tillader dets anvendelse i udladningslamper .
Væske
I modsætning til andre grundstoffer forbliver helium flydende til absolut nul ved tryk under 25 atm . Dette er en direkte konsekvens af kvantemekanikken: mere præcist er atomenergien i systemets jordtilstand for høj til at tillade størkning (se underkapitel #Solid ).
Under kogepunktet ved 4,22 K og over lambda element til 2,176 8 K , den helium-4 eksisterer som en normal farveløs væske kaldet helium I . Ligesom andre kryogene væsker koger den, når den opvarmes, og trækker sig sammen, når temperaturen sænkes. Den helium Jeg har et brydningsindeks tæt på den for gas: 1,026; hvilket gør overfladen så vanskelig at se, at vi ofte bruger polystyrenskumflåder til at se dens niveau. Denne farveløse væske har en meget lav viskositet og en densitet på 0,125 = 1/8 , hvilket kun er en fjerdedel af den værdi, der er forudsagt af klassisk fysik . Man er nødt til at ty til kvantemekanik for at forklare denne egenskab, og derfor kaldes flydende helium i dens forskellige former kvantevæske , hvilket betyder, at virkningerne af kvantemekanik, normalt kun følsomme i mikroskopisk skala, manifesterer sig i makroskopisk skala, fordi helium atom 4 er et boson . Dette fortolkes som en konsekvens af det faktum, at kogepunktet er så tæt på absolut nul, at tilfældige termiske bevægelser ikke længere kan maskere atomare egenskaber.
Superfluid
Flydende helium under lambdapunktet begynder at udvise ganske usædvanlige egenskaber i en tilstand kaldet helium II .
Ved overgangen fra helium I til helium II ved lambdapunktet udvides helium. Når temperaturen falder, fortsætter helium II med at ekspandere op til ca. 1 K , hvor det begynder at trække sig sammen igen som de fleste kroppe.
Den helium II kan strømme gennem kapillærer 10 -7 til 10 -8 m uden viskositet målbare. Men når vi måler viskositeten mellem to skiver, der roterer i forhold til hinanden, finder vi en viskositet, der kan sammenlignes med den for gasformigt helium. Nuværende teori forklarer denne kendsgerning ved hjælp af en to-fluid model af László Tisza (in) til helium II . I denne model består flydende helium under lambdapunktet af en blanding af heliumatomer i jordtilstand og atomer i ophidsede tilstande, der opfører sig mere som en almindelig væske.
En illustration af denne teori er givet ved springvand-effekten . I dette eksperiment nedsænkes et lodret rør med en lille dyse ved sin øvre ende i sin nedre ende i et bad af helium II . Den er blokeret der af en sintret skive , gennem hvilken kun væsken uden viskositet kan cirkulere. Hvis vi opvarmer røret ved f.eks. At tænde det, transformerer vi superfluid-delen til almindelig væske. For at genskabe ligevægten mellem de to væsker og badet trænger supervæske gennem den sintrede prop, og for at bevare volumen vil en del af indholdet af røret blive skubbet ud gennem den øvre dyse og danne en stråle, som kan afbryde ved at ophøre med at varme.
Den termiske ledningsevne af helium II er større end for nogen anden kendt organ. Dette forhindrer helium II i at koge, da enhver varmeindgang straks bevæger sig til overfladen, hvor den simpelthen fordamper til gas. Denne ledningsevne er en million gange større end helium I og flere hundrede gange kobber. Dette skyldes det faktum, at ledning af varme finder sted ved hjælp af en ekstraordinær kvantemekanisme. De fleste materialer, der er gode varmeledere, har et valensbånd med frie elektroner, der bruges til at lede varme. Den Helium II har ikke en sådan tape endnu godt varmeledende. Den varme flow adlyder ligninger svarende til bølgeligningerne for udbredelse af lyd i luft. Når varme indføres, bevæger den sig ved 20 m s -1 ved 1,8 K i helium II . Disse bølger kaldes anden lyd .
I modsætning til almindelige væsker kryber helium II langs overflader, selv tilsyneladende mod tyngdekraften . Det vil flygte fra en ikke lukket container ved at kravle til siderne, medmindre den støder på et mindre koldt sted, hvor det fordamper. Uanset overfladen bevæger den sig i en film på ca. 30 nm . Denne film kaldes Rollins film til minde om den fysiker, der først karakteriserede den, Bernard V. Rollin. Som et resultat af denne effekt og helium II 's evne til at passere hurtigt gennem små åbninger er det vanskeligt at begrænse flydende helium. Medmindre fartøjet er klogt konstrueret, vil helium II bestige væggene og passere gennem ventilerne, indtil det når et varmere område, hvor det vil fordampe. Bølgerne, der spredes langs en Rollins-film, adlyder de samme ligninger som bølger i lavt vand, men genoprettelseskraften her er van der Waals-kraften i stedet for tyngdekraften. Disse bølger er kendt som den tredje lyd .
Solid
Helium størkner kun under virkningen af stærkt tryk. Det resulterende praktisk talt usynlige og farveløse faste stof er meget komprimerbart; laboratoriekompression kan reducere dens volumen med mere end 30%. Med en kubisk elasticitetsmodul i størrelsesordenen 5 × 107 Pa er den halvtreds gange mere komprimerbar end vand. Under normale trykforhold, og i modsætning til andre grundstoffer, størkner helium ikke og forbliver flydende til absolut nul . Den helium faststof kræver et tryk på ca. minimum 26 atm . Det er ofte ret vanskeligt at skelne fast helium fra flydende helium, hvis brydningsindeks er næsten identiske. Det faste stof har en høj latent varme (fusionsvarme) og en sekskantet krystalstruktur, som den for vand.
Kemiske egenskaber
Som alle ædelgasser har helium sit fulde valenslag, hvilket indebærer meget lav kemisk reaktivitet. Da det ikke er i stand til at reagere underlag, er det (sammen med neon ) det mindst reaktive af alle enkle kroppe .
Helium kan dog danne ustabile forbindelser ( excimerer ) med wolfram, iod, fluor, svovl og fosfor i plasmafasen ved udledning eller på anden måde. He Ne , Hg He 10 , W He 2 og molekylionerne He 2 + , He 2 ++ , HeH + , He D + blev skabt på denne måde. Denne teknik har også muliggjort produktionen af det neutrale molekyle He 2 , som har et større antal båndsystemer, og HgHe, hvis samhørighed kun synes at stole på polariseringskræfter . Teoretisk andre bestanddele, såsom helium fluorohydride (HHE F ) er også mulige. I 2013 blev lithiumheliide LiHe dannet i gasform ved laserablation ved meget lav temperatur ( 1 til 5 K ).
De første dokumenterede stabile heliumforbindelser er endohedrale fullerenkomplekser , såsom He @ C 60 , hvor et heliumatom er fanget i et bur med C 60 fulleren . Siden da er det blevet vist, at ved meget højt tryk (større end 113 GPa ) er det muligt at danne en stabil forbindelse af helium og natrium, Na 2 Han . Sådanne molekyler kan også findes i højtrykskæmpeplaneter som Jupiter og Saturn .
Fra det indre af jorden fremkommer (i lavaer og vulkanske gasser ) helium rig på helium 3 , som menes at være oprindelig (dvs. erhvervet under dannelsen af jorden for næsten 4,6 milliarder år siden ). Hvis det var i luftform eller opløst i mineraler i den nedre kappe, ville det have haft rigelig tid til at afgas næsten fuldstændigt i betragtning af dets flygtighed og temperaturerne inde i jorden. Det skal derfor opbevares som et stabilt mineral under forholdene i den nedre kappe , men ingen er kendt. 2018 Beregningen af frie entalpi af tusind hypotetiske men plausible helium forbindelser forudsagt en (og kun én) fri enthalpi forbindelse lille nok til at fange helium i kappen i stedet for at efterlade det. Gratis, jern dioxid og helium FeO 2 Han.
Biologiske egenskaber
Helium, neutralt under standardbetingelser, er ikke-toksisk, spiller ingen biologisk rolle og findes i spormængder i humant blod. Hvis der inhaleres nok, så det ilt, der er nødvendigt til normal vejrtrækning , forskydes, bliver kvælning mulig.
Indånding
| Lydfil | |
| Tekst læst med helium | |
| Brug om nødvendigt den foregående sidetast i browseren i slutningen af høringen . (da) Helium er et farveløst, lugtfrit, smagløst, ikke-toksisk, inert monatomisk kemisk element, der leder den ædle gasserie i det periodiske system, og hvis atomnummer er 2. Dens kogepunkter og smeltepunkter er de laveste blandt elementerne og den eksisterer kun som en gas undtagen under ekstreme forhold . | |
| Har du problemer med at bruge disse medier? | |
|---|---|
Stemmen til et individ, der har inhaleret helium, skifter midlertidigt tone mod høje harmoniske - helium er tre gange mindre tæt end luft, lydens hastighed bliver således højere - og da den grundlæggende frekvens d 'er et hulrum fyldt med gas proportionalt med hastigheden af lyd svarer inhalationen af helium til en stigning i resonansfrekvenser af det fonatoriske apparat, der modulerer den grundlæggende frekvens, der gives af stemmebåndene . En modsat virkning, sænkning af klangfarvet, kan opnås ved indånding af en tættere gas, såsom svovlhexafluorid .
Indånding af rent helium ved lave doser er normalt sikkert, da det er en inaktiv gas . Imidlertid kan brugen af helium, der sælges i handel, som den, der bruges til at blæse balloner, være farlig på grund af de mange forurenende stoffer, den kan indeholde, spor af andre gasser eller aerosoler af smøreolie.
Indånding af overskydende helium kan være farligt, da helium simpelthen er en kvælende , som erstatter det ilt, der kræves til normal vejrtrækning. Åndedræt rent helium forårsager kvælning inden for få minutter. Indånding af helium direkte fra cylindre under tryk er yderst farligt på grund af den høje strømningshastighed, som kan producere barotrauma, der river lungevæv og kan være dødelig. Denne ulykke er dog ret sjælden, da der kun var to dødsfald mellem 2000 og 2004 i USA.
Ved højt tryk (over 20 atm eller 2 MPa ) kan en blanding af helium og dioxygen ( heliox ) føre til højtryksnervøs syndrom , en slags modbedøvende virkning. Ved at tilsætte lidt nitrogen til blandingen kan problemet undgås. Ikke desto mindre kan dykning under højt tryk nervesyndrom kun modvirkes ved tilsætning af brint , idet tilsætningen af nitrogen er stærkt narkotisk, så snart det samlede tryk når 5 bar.
Terapeutisk anvendelse
Helium administreres i blandinger indeholdende mindst 20% dioxygen til patienter med forhindring af øvre eller nedre luftvej. Heliums lave viskositet gør det således muligt at reducere vejrtrækningsarbejdet.
sikkerhed
Sikkerhedsforanstaltninger for kryogent helium svarer til dem, der kræves for flydende nitrogen ; sin ekstremt lave temperatur kan forårsage kolde forbrændinger .
Indånding af en stor mængde på én gang producerer let kvælning , hvilket fører til et kort men farligt tab af bevidsthed . Der er også nogle tilfælde af hjerneemboli eller alvorlige lungeproblemer hos mennesker, der inhalerer helium under tryk.
Endvidere er ekspansionshastigheden mellem væskefasen og gasfasen sådan, at den kan forårsage eksplosioner i tilfælde af hurtig fordampning, hvis der ikke er installeret et trykbegrænsende udstyr.
Reservoirer af helium gas ved 5 - 10 K skal også håndteres, som om de indeholdt flydende helium på grund af den store og hurtig termisk ekspansion som finder sted, når helium under 10 K indføres ved stuetemperatur..
Anvendelser
På trods af sin høje pris bruges helium til mange anvendelser, der kræver nogle af dets unikke egenskaber, såsom dets lave kogepunkt , lave densitet , lave opløselighed , høje varmeledningsevne eller dets kemisk og biologisk inerte karakter . Det findes kommercielt i flydende eller gasform. I flydende form kan man finde små tanke kaldet dewars , som kan rumme op til 1000 l helium eller i store ISO-tanke med nominel kapacitet op til 40.000 l . På gasform, er små mængder af helium leveres i høje trykflasker indeholdende op til 8,5 m 3 standard, mens store mængder leveres i tryk tankskibe, som kan have kapacitet op til 5.000 m 3 standarder.
Industriel
På grund af sin inaktivitet, dens høje varmeledningsevne , dens gennemsigtighed over for neutroner, og fordi den ikke danner radioaktive isotoper i reaktorer, anvendes helium som varmeoverføringsfluid i visse atomreaktorer afkølet af varme .
Helium bruges som en beskyttende atmosfære under væksten af monokrystallinsk silicium til fremstilling af integrerede kredsløb og optiske fibre , til produktion af titanium og zirconium og i gaskromatografi , fordi det er inaktivt.
På grund af sin kemiske inerti, dens ideelle termodynamiske og brændende egenskaber , dens høje lydhastighed og en stor Laplace-koefficient , er den også nyttig i supersoniske vindtunneller eller til installationer, der studerer forbigående fænomener.
De samme egenskaber gør det muligt at bruge den i forseglede harddiske for at øge deres kapacitet. Da ingen forsegling er perfekt, har disse diske en detektor, der signalerer ethvert tab af helium, der er farligt for disken over tid.
Helium blandet med en tungere gas, såsom xenon, er nyttig til termoakustisk køling på grund af det store forhold mellem termisk kapacitet og lavt Prandtl-antal . Heliums kemiske inerti har miljømæssige fordele i forhold til andre kølesystemer, som bidrager til ozonhullet eller den globale opvarmning .
Da det diffunderer gennem faste stoffer tre gange hurtigere end luft, bruges helium til at detektere lækager i ultrahøjt vakuumudstyr eller højtryksbeholdere.
Det bruges også sammen med fødevareprodukter (fødevaretilsætningsstof godkendt af EU under referencen E939 ) for at gøre det muligt at kontrollere forseglingen af emballagen (se listen over tilsætningsstoffer til fødevarer ).
Forskere
Brugen af helium reducerer virkningerne af forvrængning på grund af temperaturvariationer i rummet mellem linserne på visse teleskoper eller briller på grund af dets usædvanligt lave brydningsindeks . Denne metode bruges især til solteleskoper, der udsættes for betydelige temperaturvariationer, men for hvilke et kabinet, der understøtter trykforskellen mellem atmosfære og vakuum, ville være for tungt.
Alderen af klipper og mineraler, der indeholder uran og thorium, kan estimeres ved at måle deres heliumindhold ved en proces kaldet heliumdatering .
Flydende helium bruges også til at afkøle visse metaller til de ekstremt lave temperaturer, der kræves til superledningsevne , for eksempel til superledende magneter, der især anvendes til MR- detektorer . Den LHC på CERN bruger 120 t af flydende helium for at holde temperaturen af magneterne til 1,9 K . Mere generelt anvendes lavtemperaturhelium i kryogener .
Kommerciel og fritid
På grund af dets lave opløselighed i nervevæv , helium blandinger, såsom trimix , heliox og er helium anvendes til dyb dykning at mindske virkningerne af nitrogennarkose . På dybder større end 150 m tilsættes små mængder brint til helium-dioxygenblandingen for at modvirke nervesyndromet under højt tryk .
På disse dybder reducerer den lave densitet af helium åndedrætsindsatsen betydeligt.
De He-Ne lasere har forskellige applikationer, især læsere stregkode .
Luftskibe, balloner og raketter
Da helium er lettere end luft, kan det bruges til at puste luftskibe og gratis eller bundet balloner. Selvom brint har ca. 7% mere bæreevne, har helium fordelen ved at være ubrændbart (og endda flammehæmmende).
Udforskning af atmosfæren, især for meteorologi, udføres med balloner, det meste af tiden oppustet med helium.
I raketteknologi bruges helium som et fortrængningsmedium til at styre brændstoffet og oxidatoren i mikrogravitationstanke ved tryk og sikre blandingen af brint og ilt, der føder fremdrivningsdyserne. Det bruges også til at rense disse stoffer fra jordudstyr inden lanceringen og til at forkøle flydende brint fra rumfartøjer . For eksempel forbrugte Saturn V- raketten omkring 370.000 m 3 helium til start.
Helium ressourcer og oprensning
Naturlig overflod
Helium er det næstmest forekommende element i det kendte univers efter brint og udgør 23% af dets baryoniske masse . Langt størstedelen af helium blev dannet ved primær nukleosyntese inden for få minutter efter Big Bang . Dette er grunden til, at måling af dens overflod hjælper med at fastsætte visse parametre for kosmologiske modeller. Gennem det meste af eksistensen af stjerner er det dannet af kernefusion af brint. I slutningen af deres liv bruger stjernerne helium som råmateriale til skabelse af tungere grundstoffer ved meget hurtigere, endog eksplosive processer. I sidste ende kommer helium i universet kun en meget lille del af stjernerne.
I jordens atmosfære er koncentrationen af helium 5,2 × 10 −6 i volumen. Denne lave koncentration er ret konstant over tid på grund af en balance mellem den kontinuerlige produktion af helium i klipperne og flugten til rummet ved forskellige mekanismer . I den terrestriske heterosfære er en del af den øvre atmosfære, helium og andre lette gasser de mest rigelige bestanddele.
Næsten alt helium på jorden kommer fra α radioaktivitet . Det findes hovedsageligt i uran- og thoriumforbindelser , herunder pitchblende , carnotite og monazite , fordi de udsender α-partikler , som er kerner af ioniseret helium He 2+ , som straks neutraliseres med elektroner. Det anslås, at der produceres 3.000 t helium hvert år i litosfæren . I jordskorpen er koncentrationen af helium 8 × 10 −6 i volumen. I havvand er det kun 4 × 10 −12 . Der er også små mængder i mineralvand , vulkanske gasser og meteorisk jern . Da helium fanges som naturgas af uigennemtrængelige stenlag, findes de højeste koncentrationer af helium i naturgasfelter, hvorfra det mest kommercielle helium ekstraheres. Dens volumenkoncentration i forhold til naturgas varierer fra nogle få dele pr. Million til en koncentration på 7% identificeret i San Juan County, New Mexico .
I 2016 sagde et firma kaldet "Helium", at det havde identificeret tre mulige massive felter af dette element i Tanzania , der er store nok - ifølge det - til at forsyne verden i flere årtier, og derfor søger de 40 millioner dollars i investering i at prøve at bore i Tanzania i 2017. Nogle eksperter mener ikke desto mindre, at udnyttelsen af dette depositum ikke ville være rentabelt i lang tid, fordi ifølge dem er verdensmarkedet for nylig kommet ind i en periode med overproduktion på grund af mere økonomisk brug og i største marked i USA , Qatar og Rusland .
Ekstraktion og oprensning
Til anvendelse i stor skala ekstraheres helium ved fraktioneret destillation fra naturgas, som kan indeholde op til 7%. Da helium har et lavere kogepunkt end nogen anden krop, bruges lav temperatur og højt tryk til at flyde næsten alle andre gasser (hovedsagelig dinitrogen og metan ). Det resulterende rå helium oprenses derefter ved udsættelse for lavere og lavere temperaturer, som udfælder stort set alt kvælstof og andre resterende gasser fra gasblandingen. Endelig anvendes aktivt kul til et sidste oprensningstrin for således at opnå helium med en kvalitet på 99,995%. Den største urenhed i helium af klasse A er neon . For at afslutte rensningen flydes det meste af det producerede helium ved en kryogen proces. Likvefaktion er nødvendig for programmer der bruger flydende helium og desuden tillader helium leverandører til at reducere omkostningerne ved ekstern transport, som de større flydende helium tanke har en kapacitet på mindst fem gange større end de større. Trailere bærer under tryk helium gasflasker a .
I 2005 blev ca. 160 millioner kubikmeter helium ekstraheret fra naturgas eller trukket fra reserver med ca. 83% fra USA , 11% fra Algeriet og resten hovedsageligt fra Rusland og Polen . I USA ekstraheres det meste af helium fra naturgas i Hugoton og nærliggende felter i Kansas, Oklahoma og Texas.
En anden metode til fremstilling og oprensning af helium er diffusion af rå naturgas gennem semipermeable membraner eller andre barrierer.
Det er muligt at syntetisere helium ved at bombardere lithium eller bor med højenergiprotoner, men dette er ikke en økonomisk levedygtig produktionsmetode.
Historie
Opdagelse
Den første indikation af helium observeres den 18. august 1868Som et klart gult stribe ved en bølgelængde på 587,49 nm i spektret af kromosfæren af sol . Denne linje opdages af den franske astronom Jules Janssen under en total formørkelse i Guntur (Indien) . Først menes denne linje at være natrium . Det20. oktobersamme år, den engelske astronom Norman Lockyer observeret en gul streg i solens spektrum, som han kaldte Fraunhofer linje D 3 , på grund af dets nærhed til de velkendte linjer D 1 og D 2 af natrium. Han konkluderer, at det er forårsaget af et element af solen, der er ukendt på jorden. Lockyer og den engelske kemiker Edward Frankland navngiver dette element efter det græske ord for Sun, ἥλιος ( helios ).
I 1882 lykkedes det Luigi Palmieri for første gang at demonstrere tilstedeværelsen af helium på Jorden ved spektralanalyse af lavaen fra Vesuv .
Det 26. marts 1895Britisk kemiker Sir William Ramsay isolater helium på Jorden ved behandling kleveite (en række begblende , indeholdende mindst 10% sjældne jordarter ) med mineralske syrer . Ramsay ledte efter argon , men efter at have adskilt kvælstof og ilt fra gassen frigivet af svovlsyre , bemærkede han en lysegul linje i spektroskopet, der faldt sammen med D3- linjen observeret i solspektret.
Disse prøver identificeres som helium af Lockyer og den britiske fysiker William Crookes . Uanset hvad det er isoleret fra cleveiten samme år af kemikere Per Theodor Cleve og Abraham Langlet (i) i Uppsala , der akkumulerer nok gas til at være i stand til nøjagtigt at bestemme dets atomvægt .
Helium var også blevet isoleret af den amerikanske geokemiker William Francis Hillebrand , et par år før Ramsays opdagelse, ved at bemærke usædvanlige spektrallinjer, når man undersøgte en prøve af uaninit. Men Hillebrand tilskriver disse linjer dinitrogen. Hans lykønskningsbrev til Ramsay præsenterer et interessant tilfælde af opdagelse og næsten opdagelse inden for videnskab.
I 1907, Ernest Rutherford og Thomas Royds viste, at a-partikler er helium kerner , ved at tillade partiklerne at indtaste gennem en tynd glasvindue af et rør, hvor de evakueret, derefter oprette en udladning i røret for at studere spektret af den nye gas i det. I 1908 blev helium for første gang flydende af den hollandske fysiker Heike Kamerlingh Onnes ved afkøling af gassen under 1 K . Han forsøger at størkne det ved at sænke temperaturen yderligere, men mislykkes, da helium ikke har et tredobbelt punkt . Det er en studerende af Onnes, Willem Hendrik Keesom , der formår at størkne under tryk 1 cm 3 helium i 1926.
I 1938 opdagede den sovjetiske fysiker Pyotr Leonidovich Kapitsa , at helium-4 næsten ikke havde nogen viskositet ved temperaturer tæt på absolut nul, et fænomen, der nu kaldes overflødighed. I 1972 blev det samme fænomen observeret i helium 3 , men ved en temperatur meget tættere på absolut nul, af de amerikanske fysikere Douglas D.Osheroff , David M. Lee og Robert C. Richardson . Fænomenet i helium 3 fortolkes som dannelsen af atompar, som er fermioner , for at danne bosoner , analogt med Cooper-parerne af elektroner på basis af superledningsevne .
Produktion og anvendelser
Efter en olieboring i Dexter , Kansas i 1903 , var den producerede gasstråle ubrændbar. Erasmus Haworth (in) , geologen fra staten Kansas, indsamlede nogle prøver af den producerede gas og bragt til University of Kansas , Lawrence . Ved hjælp af kemikere Hamilton Cady (en) og David McFarland blev det bestemt, at gassen, i volumen, 72% nitrat, 15% methan (en brændbar procentdel kun med mere ilt) gas og 12% ikke kunne identificeres. Yderligere analyse viser Cady og McFarland, at 1,84% af gasprøven er helium. Dette viser, at trods sin globale knaphed på jorden er helium koncentreret i store mængder under de amerikanske store sletter og tilgængelig til produktion som et biprodukt af udnyttelse af naturgas. De største reserver af helium er i Hugoton-feltet og i nærliggende felter i det sydvestlige Kansas med udvidelser til Texas og Oklahoma.
Dette tillod USA at blive verdens førende producent af helium. Efter forslag fra Sir Richard Threlfall (in) subsidierer Navy of the United States tre små eksperimentelle heliumproduktionsanlæg under første verdenskrig . Målet er at forsyne de fastbundne spærreballoner med denne ikke-brændbare gas, som er lettere end luft. I alt 5.700 m 3 af 92% helium produceres af dette program, skønt der tidligere er produceret mindre end 100 liter i alt. Noget af denne gas bruges til verdens første heliumfyldte luftskib, US Navy C-7, indviet på sin jomfrurejse fra Hampton Roads i Virginia til Bolling Field i Washington den1 st december 1921.
Selvom gas-kondensationsprocessen ved lav temperatur ikke blev udviklet tidligt nok til at spille en væsentlig rolle under første verdenskrig, vil produktionen fortsætte. Helium bruges primært til at puste balloner op . Denne anvendelse vil øge efterspørgslen under 2. verdenskrig , ligesom efterspørgslen efter lysbuesvejsning .
Den helium massespektrometer er også afgørende for Manhattan atombomben projekt.
Den amerikanske regering oprettede i 1925 en National Helium Reserve i Amarillo , Texas , med det formål at levere aerostater, militært personel i krigstid og civile i fredstid. På grund af USAs militære embargo mod Tyskland var levering af helium der begrænset, og Hindenburg måtte pumpes op med brint med de katastrofale konsekvenser, der fulgte, da det brændte ned. Forbruget af helium efter 2. verdenskrig faldt, men reserven blev øget i 1950'erne for at sikre leveringen af flydende helium til raketstart under rumløb og den kolde krig . I 1965 overskred forbruget af helium i USA otte gange det maksimale, det nåede under krigstid.
Efter Helium- lovændringerne fra 1960 ( Public Law 86-777 ) oprettede United States Bureau of Mines fem private fabrikker til udvinding af helium fra naturgas. Til dette heliumbeskyttelsesprogram konstruerer Præsidiet en 684 km rørledning fra Bushton, Kansas , til Cliffside nær Amarillo, et delvist udtømt felt. Den således leverede helium-kvælstofblanding injiceres og opbevares indtil behovet, når den ekstraheres og oprenses.
I 1995 blev der samlet en milliard kubikmeter gas, men reserven har 1,4 milliarder dollars i gæld, hvilket fører til, at USAs kongres i 1996 gradvist ophører med sin aktivitet. Den efterfølgende Helium-privatiseringslov fra 1996 (offentlig lov 104-273) instruerer det amerikanske indenrigsministerium om at begynde at tømme reserven i 2005.
Helium produceret mellem 1930 og 1945 var ca. 98,3% rent (~ 2% nitrogen), hvilket var ideelt til aerostater. I 1945 blev en lille mængde 99,9% helium produceret til brug i lysbuesvejsning. Allerede i 1949 var der kommercielle mængder på 99,995% helium af klasse A til rådighed.
I flere år producerede USA over 90% af verdens kommercielt tilgængelige helium med ekstraktionsanlæg i Canada, Polen, Rusland og andre nationer, der producerede resten. Ifølge denne undersøgelse (ifølge en undersøgelse (august 2010), vil De Forenede Staters reserver være opbrugt inden 2040 (næsten en tredjedel af verdens behov leveres af USA, hvis globale produktionskapacitet er ca. 142 millioner kubikmeter (i 2010), mens forbruget udgjorde 180 millioner kubikmeter og at helium synes "vigtigt for de fleste af dets applikationer" ).
I midten af 1990'erne begyndte en ny fabrik at producere i Arzew , Algeriet . Med 1,7 × 10 7 m 3 om året kan den dække al europæisk efterspørgsel eller omkring 16% af verdensproduktionen. I mellemtiden oversteg forbruget i USA 15.000 t i 2000. I 2004-2006 blev der bygget to yderligere anlæg, et i Ras Laffan ( Qatar ), der producerede 9,2 ton flydende helium pr. Dag, dvs. 1,88 × 10 7 m 3 om året, og den anden i Skikda (Algeriet). Algeriet blev hurtigt den næststørste producent af helium. I denne periode steg heliumforbruget og produktionsomkostningerne. Mellem 2002 og 2007, helium priserne fordoblet, og alene i 2008, store leverandører hævet deres priser med ca. 50% . Dette er knyttet til den meget lave produktion og forbrug af helium, hvilket gør det vanskeligt at matche dem, da få producenter ønsker at investere i dette " nichemarked ".
Robert Richardson ( Nobelprisen i fysik ) i 2010 advarede det internationale samfund om risikoen for mangel og argumenterede for en stigning i priserne for at afspejle knapheden på dette element og spilde det mindre .
Virksomheden 45-8 Energy med hovedkontor i Metz indgav i oktober 2019 en eksklusiv efterforskningstilladelse for helium sydvest for Nièvre- afdelingen i Frankrig. Præfekturs svar forventes i september 2020.
Noter og referencer
- (fr) Denne artikel er helt eller delvist taget fra Wikipedia-artiklen på engelsk med titlen " Helium " ( se listen over forfattere ) .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 s. , Indbundet ( ISBN 978-1-420-09084-0 )
- (i) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Reves Jorge Echeverría, Eduard Cremades, Flavia og Santiago Barragan Alvarez , " Covalent radier revisited " , Dalton Transactions ,2008, s. 2832 - 2838 ( DOI 10.1039 / b801115j )
- "Ionization Energies of Atoms and Atomic Ions," i CRC Handbook of Chemistry and Physics, 91st Edition (Internet Version 2011), WM Haynes, red., CRC Press / Taylor and Francis, Boca Raton, FL., P. 10-203
- (da) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- "Helium" i databanken for farlige stoffer , åbnet 1. maj 2010
- Chemical Abstracts database forespørges via SciFinder Web December 15, 2009 (søg resultater )
- Sigma-Aldrich ark af forbindelsen Helium ≥99,995% , konsulteret den 17. august 2018.
- " Helium " i databasen over kemiske produkter Reptox fra CSST (Quebec-organisation med ansvar for sikkerhed og sundhed på arbejdspladsen), adgang til den 25. april 2009
- Paul Depovere, elementernes periodiske system . Universets grundlæggende vidunder , De Boeck Supérieur ,2002, s. 103.
-
(da) Eric Hand, “ Massive heliumfelter fundet i kløftzone i Tanzania ” , Science , bind. 353, nr . 6295,8. juli 2016, s. 109-110 ( DOI 10.1126 / science.353.6295.109 , læst online
 , adgang til 11. juli 2016 ).
, adgang til 11. juli 2016 ).
- Audrey Chauvet, " Verdens heliumreserver tømmes " , på www.20minutes.fr ,30. august 2010(adgang til 22. juni 2019 ) .
- (en) John Emsley , Naturens byggesten: en AZ guide til elementerne , Oxford New York, Oxford University Press ,2001, 538 s. ( ISBN 978-0-19-850340-8 og 978-0-198-50341-5 , OCLC 248877093 , læs online ) , s. 175–179.
-
(i) Achim Weiss, " Elementer fra fortiden: kernesyntese og observation " , Max Planck Instituttet for Gravitational Fysik (adgang 23 juni 2009 ) ;.
(en) A. Coc et al. , “ Opdateret Big Bang-nukleosyntese konfronteret med WMAP-observationer og overflod af lyselementer ” , The Astrophysical Journal , bind. 600,2004, s. 544 ( DOI 10.1086 / 380121 ). -
(i) Don L. Anderson, GR Foulger Anders Meibom, " Helium Fundamentals " , MantlePlumes.orgMantlePlumes.org,
2006(adgang 20. juli 2008 ) .
Kun
abstrakt. Varen tilbydes til salg. - (i) Aaron Novick , " Half-Life af tritium " , Physical Review , vol. 72, 1947, s. 972 ( DOI 10.1103 / PhysRev.72.972.2 , læs online )Adgang begrænset til PROLA-abonnenter.
- (i) GN Zastenker og E. Salerno, F. Buehler, P. Bochsler, M. Bassi, YN Agafonov, NA Eismont, VV Khrapchenkov, H. Busemann , " Isotopanalyse sammensætning og tæthed Interstellar Neutral Helium baseret på direkte målinger " , Astrophysics , vol. 45, n o 2April 2002, s. 131–142 ( DOI 10.1023 / A: 1016057812964 , læs online ) Kun abstrakt . Varen tilbydes til salg.
- (in) " Lunar Mining of Helium-3 " , Fusion Technology Institute ved University of Wisconsin-Madison, 2007(adgang til 9. juli 2008 ) .
- (en) EN Slyuta AM Abdrakhimov EM Galimov, " Skøn over helium-3 sandsynlige reserver i månens regolit i Lunar and Planetary Science XXXVIII " [PDF] ,2007(adgang 23. juni 2009 ) .
- (in) Eric R. Hedman , " En fascinerende time med Gerald Kulcinski " , The Space Review ,16. januar 2006( læs online ).
- (i) Peter Häussinger1 Reinhard Glatthaar2 Wilhelm Rhode3 Helmut Kick4 Christian Benkmann5 Josef Weber6 Hans-Jörg Wunschel7 Viktor Stenke8 Edith Leicht9 Hermann Stenger10, Ædelgasser , Wiley-VCH Verlag GmbH & Co , et al. " Ullmann's Encyclopedia of Industrial Chemistry ",15. marts 2001( online præsentation ).
- (en) LW Brandt, (Clifford A. Hampel, red.) The Encyclopedia of the Chemical Elements , Reinhold Book Corporation , New York, 1968, kap. "Helium" , s. 256-268 .
- (i) Ray F. Weiss , " Opløselighed af helium og neon i vand og havvand " , J. Chem. Eng. Data , vol. 16, nr . 21971, s. 235-241 ( DOI 10.1021 / je60049a019 )Første side.
- (i) Jack A. Stone og Alois Stejskal , " Brug af helium som en standard for refraktiv " , Metrologia , Vol. 41,2004, s. 189–197 ( DOI 10.1088 / 0026-1394 / 41/3/012 ) Abstrakt .
- (i) The Encyclopedia of Chemical Elements , op. cit. , s. 261 .
- (in) F. Buhler og WI Axford, HJA Chivers, K. Martin , " Helium-isotoper i årlige aurora " , J. Geophys. Res. , Vol. 81, nr . 1,1976, s. 111–115 ( DOI 10.1029 / JA081i001p00111 ) Abstrakt .
- (en) Encyclopedia of the Chemical Elements , op. cit. s. 262 .
- (in) PC Hohenberg og PC Martin , " Microscopic Theory of superfluid Helium " , Annals of Physics , bind. 281, n knogle 1-2,Oktober 2000, s. 636–705 ( DOI 10.1006 / aphy.2000.6019 ) Abstrakt . Artikel tilgængelig for ScienceDirect-abonnenter.
- (in) Encyclopedia of the Chemical Elements , op. cit. , s. 263 .
- (in) HA Fairbank og CT Lane , " Rollin Film Rates in Liquid Helium " , Physical Review , bind. 76, nr . 8,Oktober 1949, s. 1209-1211 ( DOI 10.1103 / PhysRev.76.1209 ) Abstrakt . Varen tilbydes til salg.
- (in) BV Rollin og F. Simon , " Om" film "fænomenet flydende helium II " , Physica , bind. 6, nr . 21939, s. 219-230 ( DOI 10.1016 / S0031-8914 (39) 80013-1 ) Abstrakt . Artikel tilgængelig for ScienceDirect-abonnenter.
- (in) Fred Ellis, " Third sound " , Wesleyan Quantum Fluids Laboratory ,September 2005(adgang 23. juni 2009 ) .
- (i) D. Bergman , " Hydrodynamik og Tredje tynd lyd i Han II Film " , Physical Review , vol. 188, nr . 1,Oktober 1949, s. 370–384 ( DOI 10.1103 / PhysRev.188.370 ) Abstrakt . Fås til PROLA-abonnenter eller til salg.
- (en) " Periodisk system: Helium " (adgang til 23. juni 2009 ) .
- (i) Naima Tariq Nada Taisan, Vijay Singh og Jonathan Weinstein, " Spektroskopiske Påvisning af Lihe molekyle " , Physical Review Letters , vol. 110, nr . 15,8. april 2013, s. 153201 ( PMID 25167262 , DOI 10.1103 / PhysRevLett.110.153201 , læst online , adgang til 10. december 2017 ).
- SB " Helium binder til højtryksnatrium " For videnskab , nr . 474,april 2017, s. 10.
- (i) Xiao Dong, Artem R. Oganov et al. , " En stabil forbindelse af helium og natrium ved højt tryk " , Nature Chemistry ,6. februar 2017( læs online )
- " Heliums kemi, ukendt på Jorden, kunne eksistere i kæmpe planeter " , på futura-sciences.com ,9. februar 2017(adgang til 9. februar 2017 )
- (in) Jurong Zhang Jian Lv, Hefei Li, Feng Xiaolei Cheng Lu et al. , “ Sjælden heliumbærende forbindelse FeO 2, som han stabiliserede sig ved dybe jordforhold ” , Physical Review Letters , bind. 121, nr . 25,21. december 2018, s. 1-6, vare nr . 255703 ( DOI 10.1103 / PhysRevLett.121.255703 , læs online [PDF] ).
- (i) R. Mark Wilson, " En heliumbærende forbindelse dybt inde i jorden findes beregningsmæssigt " , Physics Today ,10. januar 2019( DOI 10.1063 / PT.6.1.20190110a ).
- (in) " Fokus: Et hjem for helium inde i jorden " , Fysik (in) , bind. 11,21. december 2018, Artikel nr . 133 ( læs online ).
- (in) J. Ackerman og G. Maitland , " Beregning af den relative lydhastighed i en gasblanding " , Undersea Biomed. Res. , Vol. 2, nr . 4,December 1975, s. 305–310 ( læs online ).
- (i) Joe Wolfe, " Fysik i tale " , phys.unsw.edu.au. (adgang 23. juni 2009 ) .
- Hvorfor ændrer helium stemmen? på futura-sciences.com .
- (da) Martin Grassberger og Astrid Krauskopf , ” Selvmordskvelning med helium: Rapport om tre tilfælde. Suizid mit Helium Gas: Bericht über drei Fälle. » , Wiener Klinische Wochenschrift , vol. 119, nr . 9-10,2007, s. 323–325 ( DOI 10.1007 / s00508-007-0785-4 )Resume på tysk. Første side tilgængelig. Varen tilbydes til salg.
- (in) Daniel Engber, " Bliv ude af den ballon! " , Slate.com,2006(adgang 23. juni 2009 ) .
- (i) JC Eostain , C. Lemaire , MC-Gardette Chauffour , J. Doucet og R. Naquet , " Skøn over menneskers modtagelighed for højtryks-nervøs syndrom " , Journal of Applied Physiology , vol. 54, nr . 4,April 1983, s. 1063-1070 ( læs online )Fås på personligt eller institutionelt abonnement.
- (in) WL Hunger Jr. og PB Bennett , " Årsagerne, mekanismerne og forebyggelsen af højtryksnervøs syndrom " , Undersea Biomedical Research , vol. 1, n o 1,1974, s. 1-28 ( ISSN 0093-5387 , OCLC 2068005 , PMID 4619860 , læs online ).
- (in) Glenn D. Considine (red.) Van Nostrand's Encyclopedia of Chemistry , Wylie-Interscience, ( ISBN 0-471-61525-0 ) , kap. "Helium" , s. 764–765 .
- (i) IE Beckwith og CG Miller III , " aerotermodynamik og Transition i High-Speed Wind Tunnel ved NASAs Langley " , Annual Review of Fluid Mechanics , bind. 22,1990, s. 419–439 ( DOI 10.1146 / annurev.fl.22.010190.002223 ).
- (in) CI Morris, stødinduceret forbrænding i højhastigheds kileflow , Stanford University-afhandling , 2001 [ læs online (adgang til 23. juni 2009)] .
- https://www.lemondeinformatique.fr/actualites/lire-un-disque-dur-helium-16-to-pour%C2%A0datacenter%C2%A0chez-toshiba-75335.html
- (i) James R. Belcher og William V. Slaton, Richard Raspet Henry E. Bass, Jay Lightfoot , " Working gasser i varme- motorer " , Journal of Acoustical Society of America , vol. 105, nr . 5,1999, s. 2677–2684 ( DOI 10.1121 / 1.426884 )Fås ved abonnement.
- (i) Arjun Makhijani Kevin Gurney, Mending ozonhullet: Videnskab, Teknologi og Politik , MIT Press , 1995 ( ISBN 0-262-13308-3 ) .
- (i) H. Jakobsson , " Simulering af dynamikken i den store Jord-baserede Solar Telescope " , Astronomisk & Astrophysical Transaktioner , Vol. 13, nr . 1,1997, s. 35–46 ( DOI 10.1080 / 10556799708208113 ) Abstrakt . Abonnementsartikel.
- (in) O. Engvold og RB Dunn RN Smartt, WC Livingston , " Tests of vacuum VS helium in a solar telescope " , Applied Optics , Vol. 22,1983, s. 10–12 ( DOI 10.1364 / AO.22.000010 , læs online ) Abstrakt . Varen tilbydes til salg.
- (in) " CERN - LHC: Fakta og tal - Vejledning til LHC-brochurer " ( Arkiv • Wikiwix • Archive.is • Google • Hvad skal man gøre ) [PDF] , CERN (adgang 23. juni 2009 ) .
- (in) " Kryogenik: Lav temperatur, høj ydeevne | CERN ” , på home.cern (adgang til 7. februar 2019 ) .
- (in) B. Fowler og KN Ackles, G. Porlier , " Effects of inert gas narcosis is behavior-A Critical Review " , Undersea Biomedical Research Journal ,1985( PMID 4082343 , læs online ).
- (in) JR Thomas , " Reversal of nitrogen narcosis in rotts by helium pressure " , Undersea Biomed. Res. , Vol. 3, n o 3,1976, s. 249–259 ( PMID 969027 , læs online ).
- (en) JC Eostain og MC-Gardette Chauffour, C. Lemaire, R. Naquet , " Effekter af en H 2 -Han-O 2blanding på HPNS op til 450 msw ” , Undersea Biomed. Res. , Vol. 15, nr . 4,1988, s. 257–270 ( ISSN 0093-5387 , OCLC 2068005 , PMID 3212843 , læs online ).
- (i) Scott J. Butcher og Richard L. Jones, Jonathan R. Mayne, Timothy C. Hartley, Stewart R. Petersen , " Nedsat motion åndedrætsbesværlig- mekanik med den selvstændige åndedrætsværn er Forbedret med heliox ' , European Journal of Anvendt fysiologi , Holland, Springer, vol. 101, nr . 6,december 2007, s. 659–669 ( DOI 10.1007 / s00421-007-0541-5 )Første side gratis, artikel begrænset til Springer-abonnenter.
- (da) Albert Stwertka, Guide to the Elements: Revised Edition , Oxford University Press , New York, 1998, ( ISBN 0-19-512708-0 ) , s. 24 .
- (in) BM Oliver og James G. Bradley, Harry Farrar IV , " Heliumkoncentration i jordens lavere atmosfære " , Geochimica og Cosmochimica Acta , vol. 48, nr . 9,1984, s. 1759–1767 ( DOI 10.1016 / 0016-7037 (84) 90030-9 ) Gratis abstrakt , artikel tilgængelig på ScienceDirect-abonnement.
- (in) " Atmosfæren: Introduktion i JetStream - Online School for Weather " , National Weather Service , 29. august 2007 (adgang 23. juni 2009 ) .
- (en) Ø. Lie-Svendsen og MH Rees , ” Helium flygter fra den jordbaserede atmosfære: ionudstrømningsmekanismen ” , Journal of Geophysical Research , bind. 101, n o A21996, s. 2435–2444 ( DOI 10.1029 / 95JA02208 ) Abstrakt , artikel efter AGU-abonnement.
- (i) Nick Strobel, " Nick Strobel s Astronomi Noter kap. Atmosfærer ' ,2007(adgang 23. juni 2009 ) .
- (i) Melvin A. Kog , " Hvor er jordens radiogen helium? » , Nature , vol. 179,1957, s. 213 ( DOI 10.1038 / 179213a0 ) Abstrakt , vare udbydes til salg.
- (i) LT Aldrich og Alfred O. Nier , " Forekomsten af Heb 3i naturlige kilder til helium ” , Phys. Rev. , Vol. 74,1948, s. 1590–1594 ( DOI 10.1103 / PhysRev.74.1590 ) Abstrakt , artikel om PROLA-abonnement.
- (i) P. Morrison og J. Pine , " radiogen Oprindelse af Helium Isotoper i Rock " , Annals of New York Academy of Sciences , vol. 62, nr . 3,1955, s. 71–92 ( DOI 10.1111 / j.1749-6632.1955.tb35366.x )Intet abstrakt , anerkendelser, artikel om abonnement på Wiley InterScience.
- (i) RE Zartman , " Helium Argon og Carbon i Natural Gases " , Journal of Geophysical Research , vol. 66, nr . 1,1961, s. 277–306 ( DOI 10.1029 / JZ066i001p00277 , læs online )På AGU-abonnement eller til salg.
- (i) Ronald F. Broadhead , " Helium i NewMexico - geologi fordeling udforskning demandand ressource muligheder " , New Mexico Geologi , vol. 27, nr . 4,2005, s. 93–10 ( læs online [PDF] ).
- (en) Hand, E (2016) Massive heliumfelter fundet i kløftområde i Tanzania ; Videnskab 8. juli 2016: bind. 353, udgave 6295 , s. 109-110 DOI : 10.1126 / science.353.6295.109 .
- (i) Mark Winter, " Helium: det væsentlige " , University of Sheffield ,2008(adgang 23. juni 2009 ) .
- (i) The Encyclopedia of Chemical Elements , op. cit. , s. 258 .
- (da) EM Smith og TW Goodwin, J. Schillinger , " Udfordringer for verdensomspændende helium i det næste årti " , Advances in Cryogenic Engineering , bind. 49A, nr . 710, 2003, s. 119–138 ( DOI 10.1063 / 1.1774674 , læs online [PDF] ).
- (in) " Mineral Commodity Summaries - Helium " [PDF] , US Geological Survey ,2004(adgang 23. juni 2009 ) .
- (en) VP Belyakov , SG Durgar'yan, BA Mirzoyan et al. , “ Membran technology - A new trend in industrial gas separation ” , Chemical and Petroleum Engineering , vol. 17, nr . 1,nitten og firs, s. 19–21 ( DOI 10.1007 / BF01245721 )Første side gratis, fortsættelsen på SpringerLink-abonnement eller betalt.
- (i) PI Dee og ETS Walton , " A Photographic Investigation of the Transmutation of Lithium and Bor by Protons and ions of lithium by of the heavy isotope of Hydrogen " , Proceedings of the Royal Society of London , vol. 141, nr . 8451933, s. 733-742 ( DOI 10.1098 / rspa.1933.0151 )Betalt eller abonnementsadgang for ikke-medlemmer af Royal Society .
- (i) RK Kochhar , " franske astronomer i Indien i det 17. - 19. århundrede " , Journal of the British Astronomical Association , vol. 101, nr . 21991, s. 95–100 ( læs online ).
- (i) The Encyclopedia of Chemical Elements , op. cit. , s. 256 .
- (i) William Thomson, Frankland og Lockyer finder de gule fremtrædende pladser til at give en meget lys linje Afgjort ikke langt fra D-mål Hidtil ikke identificeret med nogen jordisk flamme. Det ser ud til at indikere et nyt stof, som de foreslår at kalde Helium. , Rep. Brit. Assoc. xcix , 1872.
- definition af Cleveitis .
- (in) Encyclopedia of the Chemical Elements , op. cit. , s. 257 .
- (i) William Ramsay , " var gas Viser spektret af Helium, den ansete Årsag til D3 en af linjerne i den koronale Spectrum. Foreløbig note ” , Proceedings of the Royal Society of London , vol. 58,1895, s. 65–67 ( DOI 10.1098 / rspl.1895.0006 )Betalt eller på abonnement for ikke-medlemmer af Royal Society .
- (i) William Ramsay , " Helium, en gasformig bestanddel af visse mineraler. Del I ” , Proceedings of the Royal Society of London , bind. 58,1895, s. 80–89 ( DOI 10.1098 / rspl.1895.0010 )Betalt eller på abonnement for ikke-medlemmer af Royal Society.
- (i) William Ramsay , " Helium, en gasformig bestanddel af visse mineraler. Del II ” , Proceedings of the Royal Society of London , bind. 59,1895, s. 325–330 ( DOI 10.1098 / rspl.1895.0097 )Betalt eller på abonnement for ikke-medlemmer af Royal Society .
- (De) NA Langlet , " Das Atomgewicht des Heliums " , Zeitschrift für anorganische Chemie , bind. 10, n o 1,1895, s. 289–292 ( DOI 10.1002 / zaac.18950100130 )Til salg eller ved abonnement på Wiley InterScience.
- (i) ER Weaver, Industrial & Engineering Chemistry , 1919, kap. “ Bibliografi over Helium-litteratur ” .
- (i) Pat Munday, American National Biography , John A. Garraty og Mark C. Carnes (red.), Oxford University Press , 1999 " Biografisk post for WF Hillebrand (1853-1925), geokemiker og US Bureau of Standards administrator » , Vol. 10-11, s. 227–228 .
- (i) Dirk van Delft , " En lille kop helium, en stor videnskab " , fysik i dag ,2008, s. 36–42 ( læs online [PDF] ).
- (i) " Koldeste Cold " , Time Inc. ,1929(adgang 23. juni 2009 ) .
- (in) P. Kapitza , " Viskositet af flydende helium λ under punktet " , Nature , bind. 141,1938, s. 74 ( DOI 10.1038 / 141074a0 ).
- (in) DD Osheroff og RC Richardson, DM Lee , " Evidence for a New Phase of Solid Heb 3 " , Phys. Rev. Lett. , Vol. 28, nr . 14,1972, s. 885–888 ( DOI 10.1103 / PhysRevLett.28.885 ) Abstrakt . Artikel ophavsretligt beskyttet af PROLA.
- (i) DF McFarland , " sammensætning Gas fra en brønd på Dexter, Kan " , transaktioner af den Kansas Academy of Science , vol. 19,1903, s. 60–62 ( DOI 10.2307 / 3624173 , læs online )Første side. Fuld artikel under JSTOR-vilkår.
- (in) " Opdagelsen af helium i naturgas " , American Chemical Society ,2004(adgang 23. juni 2009 ) .
- (i) HP Cady og DF McFarland , " Helium i Natural Gas " , Science , vol. 24,1906, s. 344 ( DOI 10.1126 / science.24.611.344 )Intet abstrakt . Varer til salg eller AAAS-medlemmer.
- (i) HP Cady og DF McFarland , " Helium i Kansas Naturgas " , Transactions af Kansas Academy of Science , vol. 20,1906, s. 80–81 ( DOI 10.2307 / 3624645 , læs online [ arkiv af27. maj 2012] )<Intet abstrakt . Artikel under JSTOR-betingelser.
- (in) Eugene M. Emme, (red.) Aeronautics and Astronautics: An American Chronology of Science and Technology in the Exploration of Space, 1915-1960 , NASA , Washington, DC, 1961 [ læs online (adgang til 23. juni 2009 )] , kap. “ Aeronautics and Astronautics Chronology, 1920–1924 ” , s. 11–19 .
- (i) N. Hilleret, S. Turner (red.) CERN Accelerator Skole, vakuum teknologi: sag: Scanticon Conference Center, Snekersten, Danmark, 28 maj - 3 juni 1999 , CERN , Geneve, Schweiz, 1999 [ read linje ( side hørt 23. juni 2009)] , kap. " Lækagedetektion " , s. 203–212 . ”Starten af helium lækagedetekteringsmetoden skal spores tilbage til Manhattan-projektet og de hidtil usete tætningskrav for uranseparationsanlæg. Den følsomhed, der kræves til verifikation af tætheden, førte til valget af massespektrometer designet af Dr. AOC Nier og kalibreret på massen af helium. "
- (i) John G. Williamson , " Energi for Kansas ' , transaktioner af den Kansas Academy of Science , Kansas Academy of Science , vol. 71, nr . 4,vinter 1968, s. 432–438 ( læs online )Første side. Fuld artikel under JSTOR-vilkår.
- (in) - , " Conservation Helium Sale " , Federal Register , Vol. 70, nr . 193,6. oktober 2005, s. 58464 ( læs online [PDF] ).
- (i) " Resumé: virkningen af at sælge den føderale heliumreserve " , nap.edu ( ISBN 978-0-309-07038-6 , adgang 23. juni 2009 ) .
- (i) PV Mullins, RM Goodling Helium , Bureau of Mining / Minerals Yearbook 1949 1951 [ læse online (tilgås 21 juni 2009)] , s. 599–602 .
- (in) undersøgelse Selling the Nation's Helium Reserve ,august 2010.
- (in) GR Matos, JB Peterson, " Helium End User Statistic " , US Geological Survey (adgang 23. juni 2009 ) .
- (i) Karen H. Kaplan , " Helium mangel hæmmer forskning og industri " , Fysik dag , American Institute of Physics , bind. 60, n o 6,juni 2007, s. 31–32 ( DOI 10.1063 / 1.2754594 , læs online ).
- (in) Sourish Basu og Philip Yam (red.) , " Updates: Into Thin Air " , Scientific American , Scientific American, Inc. , bind. 297, nr . 4,oktober 2007, s. 18 ( læs online ).
- Ludovic Pillevesse, " Præfekturen giver eller ej i september en eksklusiv tilladelse til heliumforskning i Nièvre ", Le journal du Centre ,31. august 2020( læs online )
Se også
Bibliografi
på. (en) Z. Cai, R. Clarke, N. Ward, WJ Nuttall, BA Glowacki, " Modelling Helium Markets " [PDF] , University of Cambridge ,2007(adgang til 22. juni 2009 ) .
Relaterede artikler
- Overflødighed
- Kryogenik
- Ædelgas kemi
- Kalefaktion eller Leidenfrost-effekt
- Konservering af kød
- Lækagedetektion
-
Metastabelt helium

eksterne links
- ” Opdagelsen af flydende helium i 1908 af Kamerlingh ” , BibNum (hørt 21. juni 2009 ) , kommenterede tekst.
- (da) " Tekniske data for Helium " (adgang til 23. april 2016 ) med de kendte data for hver isotop på undersider
- Myndighedsregistreringer :
- Meddelelser i generelle ordbøger eller leksikon :
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | Hej | |||||||||||||||||||||||||||||||
| 2 | Li | Være | B | VS | IKKE | O | F | Født | |||||||||||||||||||||||||
| 3 | Ikke relevant | Mg | Al | Ja | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Det | Sc | Ti | V | Cr | Mn | Fe | Co | Eller | Cu | Zn | Ga | Ge | Es | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | CD | I | Sn | Sb | Du | jeg | Xe | |||||||||||||||
| 6 | Cs | Ba | Det | Det her | Pr | Nd | Om eftermiddagen | Sm | Havde | Gd | TB | D y | Ho | Er | Tm | Yb | Læs | Hf | Dit | W | Re | Knogle | Ir | Pt | På | Hg | Tl | Pb | Bi | Po | På | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Kunne det | Er | Cm | Bk | Jf | Er | Fm | Md | Ingen | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
alkali metaller |
Alkalisk jord |
Lanthanider |
overgangsmetaller metaller |
Dårlige metaller |
Metal- loids |
Ikke- metaller |
halo -gener |
Ædle gasser |
Varer uklassificeret |
| Actinides | |||||||||
| Superactinider | |||||||||